पर अंतर आणविक बल, सामान्य रूप से कहा जाता है वैन डेर वाल्स फोर्सेस, वहा तीन है: प्रेरित द्विध्रुवीय-प्रेरित द्विध्रुवीय, हाइड्रोजन बांड और स्थायी द्विध्रुवीय-स्थायी द्विध्रुवीय। इस पाठ में, हम इन तीन बलों में से केवल अंतिम पर विचार करेंगे:
शक्ति स्थायी द्विध्रुव-स्थायी द्विध्रुव, या केवल, द्विध्रुवीय-द्विध्रुवीय में ही होता है ध्रुवीय अणु, अर्थात्, जिनकी सतह पर समान भार वितरण नहीं होता है। उदाहरण के लिए, एचसीएल (हाइड्रोक्लोरिक गैस) के अणु में इलेक्ट्रॉनिक बादल क्लोरीन परमाणु की ओर अधिक विस्थापित होता है, क्योंकि यह हाइड्रोजन की तुलना में अधिक विद्युतीय है।
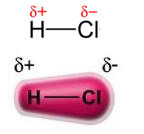
ध्यान दें कि क्लोरीन परमाणु के चारों ओर इलेक्ट्रॉनों का संचय होता है, जिससे a. का निर्माण होता है नकारात्मक ध्रुव, जो ग्रीक अक्षर डेल्टा द्वारा दर्शाया गया है (-δ). परिणामस्वरूप, हाइड्रोजन परमाणु के आसपास के क्षेत्र में a सकारात्मक ध्रुव (+δ), क्योंकि इसका इलेक्ट्रॉनिक घनत्व कम होता है। एचसीएल अणु तब बनता है a विद्युत द्विध्रुव और, इसलिए, अन्य पड़ोसी एचसीएल अणुओं के संपर्क में आने पर, अणुओं के विपरीत ध्रुवों के बीच एक आकर्षण बल होता है, जैसा कि नीचे देखा जा सकता है:
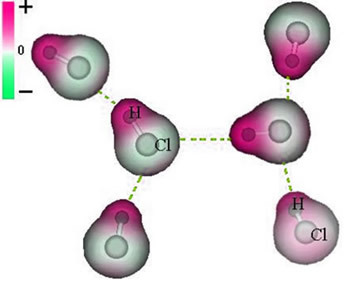
यह आकर्षक बल, जो एक अणु के द्विध्रुव के ऋणात्मक सिरे और दूसरे अणु के द्विध्रुव के धनात्मक सिरे के बीच स्थापित होता है, द्विध्रुव-द्विध्रुवीय बल का निर्माण करता है।.
इसलिए, जैसा कि नाम से पता चलता है, द्विध्रुवीय स्थायी है, इसलिए यह केवल ध्रुवीय यौगिकों में होता है। और एक अणु की ध्रुवता जितनी अधिक होती है, पदार्थ में द्विध्रुवीय-द्विध्रुवीय अंतःक्रिया उतनी ही तीव्र होती है।
यदि यह ठोस चरण में है, तो स्थायी द्विध्रुव का निर्माण अंतरिक्ष में प्रत्येक अणु की स्थिति का मार्गदर्शन करता है द्विध्रुवीय क्रिस्टल; जैसा कि नीचे सचित्र हाइड्रोजन ब्रोमाइड के मामले में है:
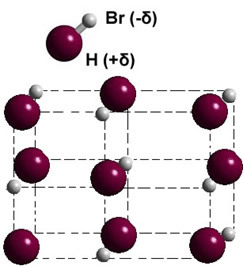
ध्रुवीय पदार्थों के अन्य उदाहरण जिनके अणुओं के बीच द्विध्रुवीय-द्विध्रुवीय शक्ति होती है: H2एस, सीओ, एचसीसीएल3, केवल2.
यह अंतर-आणविक बल का है मध्यम तीव्रता, क्योंकि यह प्रेरित द्विध्रुवीय-प्रेरित द्विध्रुवीय आकर्षण बल से अधिक मजबूत है, लेकिन हाइड्रोजन बंधन से कम तीव्र है। यही कारण है कि उनके गलनांक और क्वथनांक उन पदार्थों की तुलना में अधिक होते हैं जिनमें एक प्रेरित द्विध्रुवीय शक्ति होती है। जैसा कि स्थायी द्विध्रुवीय बल अधिक मजबूत होता है, इसके अणुओं के अंतःक्रियाओं को तोड़ने के लिए अधिक ऊर्जा की आपूर्ति करना आवश्यक है।
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/quimica/forca-intermolecular-dipolo-dipolo.htm


