हे अमोनियम नाइट्रेट आणविक सूत्र NH. का एक ठोस पदार्थ है4पर3 और सफेद उपस्थिति (जब शुद्ध)। गठित से आयनों राष्ट्रीय राजमार्ग4+ (अमोनियम) और NO3- (नाइट्रेट)ज्वलनशील नहीं है, लेकिन अत्यधिक ऑक्सीकरण और प्रतिक्रियाशील है। इसकी अपघटन प्रतिक्रिया उत्पाद के रूप में गैसों की एक बड़ी मात्रा उत्पन्न करती है, जो इस उत्पाद के अनुचित भंडारण को एक गंभीर समस्या बनाती है, क्योंकि विस्फोट हो सकता है। और भी कृषि में व्यापक रूप से उपयोग किया जाता है एक उर्वरक के रूप में।
यह भी पढ़ें: प्राकृतिक पदार्थ - अणु प्रकृति से उत्पन्न होते हैं
अमोनियम नाइट्रेट क्या है?

अमोनियम नाइट्रेट यह एक नमक है NH आयनों द्वारा गठित4+ (अमोनियम) और NO3- (नाइट्रेट)। यह एक ठोस यौगिक है कि, जब शुद्ध, यह सफेद रंग का होता है। इसका व्यापक रूप से कृषि उर्वरक के रूप में उपयोग किया जाता है, लेकिन इसका उपयोग विस्फोटकों के निर्माण में भी किया जा सकता है, जैसे यह एक बहुत ही ऑक्सीकरण पदार्थ है, फिर ऑक्सीकरण। अमोनियम नाइट्रेट की भगोड़ा प्रतिक्रिया एक उच्च रिलीज उत्पन्न करती है गैसों, कारण विस्फोटक प्रभाव.
अमोनियम नाइट्रेट के लक्षण
दाढ़ द्रव्यमान: ८०.०४३३६ g/mol.
आयनों से बना नमक: अमोनियम (NH .)4+) और नाइट्रेट (NO .)3-).
सूरत: सफेद ठोस।
यह मजबूत ऑक्सीकरण है।
अन्य पदार्थों के साथ आसानी से प्रतिक्रिया करता है।
यह ज्वलनशील नहीं है।
सामान्य तापमान और दबाव की स्थिति के लिए:
- घनत्व: 1.73 ग्राम/सेमी³;
- क्वथनांक: २१० डिग्री सेल्सियस;
- गलनांक: 169.6 डिग्री सेल्सियस;
- पानी में घुलनशीलता की डिग्री: 216 ग्राम/100 मिली;
- पीएच: 5.5 (0.2M)।
अमोनियम नाइट्रेट फॉर्मूला
इस यौगिक का आणविक सूत्र NH. है4पर3.
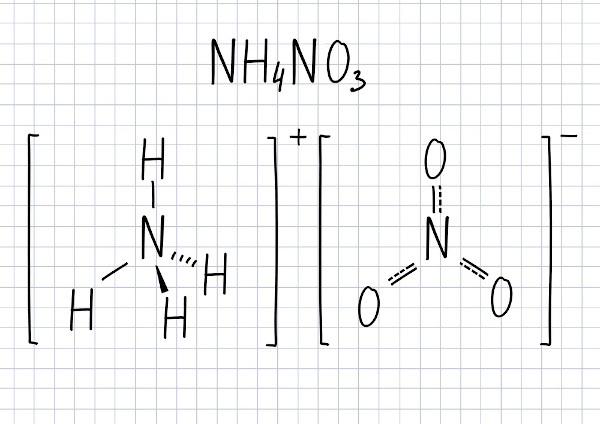
अमोनियम नाइट्रेट का अपघटन
एक होने के लिए उच्च प्रतिक्रियाशीलता और उच्च ऑक्सीकरण क्षमता वाले पदार्थ, अमोनियम नाइट्रेट, जब उच्च तापमान के अधीन होता है, तो ट्रिगर करता है a अपघटन प्रतिक्रिया, और मुख्य उत्पाद गैसें, नाइट्रोजन, ऑक्सीजन और जल वाष्प। अपघटन दो चरणों में दिया जाता है:
→ पहला कदम:
२एनएच4पर3 (एस) → 2N2ओ (जी) + 4 एच2ओ (जी)
→ दूसरा चरण:
२एन2ओ → 2एन2(जी) + ओ2(छ)
→ वैश्विक समीकरण:
२एनएच4पर3 (एस) → 2N2(जी) + ओ2(जी) + 4H2ओ (जी)
ध्यान दें कि, पहले समीकरण में,उत्पादों में से एक अपघटन में प्राप्त होता है नाइट्रस ऑक्साइड (एन2ओ), के रूप में भी जाना जाता है हंसाने वाली गैस. इसका उपयोग ईंधन जलाने के लिए ऑटोमोटिव इंजन की शक्ति को बढ़ाने के लिए और मुख्य रूप से दंत चिकित्सकों द्वारा एक संवेदनाहारी के रूप में किया जाता है। यह भी है के लिए जिम्मेदार मुख्य गैसों में से एक ग्रीनहाउस प्रभाव.
यह भी देखें: रासायनिक अभिक्रिया कितने प्रकार की होती हैं?
अमोनियम नाइट्रेट उत्पादन
अमोनियम नाइट्रेट द्वारा प्राप्त किया जा सकता है अमोनियम सल्फेट (NH4) के बीच अभिक्रिया2केवल4 और कैल्शियम नाइट्रेट Ca (NO .)3)2. निचे देखो:
(एनएच4)2केवल4 + सीए (नहीं3)2 → 2 एनएच4पर3+ केस4
इसे गैसीय अमोनिया से भी बनाया जा सकता है, जो एक नाइट्रिक एसिड समाधान में बुदबुदाया जाता है, एक प्रतिक्रिया उत्पाद के रूप में जलीय अमोनियम नाइट्रेट होता है। देखो:
राष्ट्रीय राजमार्ग3 (जी) + एचएनओ3 (एक्यू) → राष्ट्रीय राजमार्ग4पर3(यहां)
अमोनियम नाइट्रेट के मुख्य इस्तेमाल

- उर्वरक निर्माण
- खदानों, खदानों और निर्माण में विस्फोटक
- शाकनाशी और कीटनाशक
- औद्योगिक अनुप्रयोग के लिए नाइट्रस ऑक्साइड प्राप्त करना
- ऑक्साइड के लिए अवशोषक
- रॉकेट प्रणोदक के लिए ऑक्सीडेंट
- इज़ोटेर्मल बैग का निर्माण
- मधुमक्खी पालन में पित्ती के प्रबंधन के लिए संवेदनाहारी धुएं का उत्पादन
साथ ही पहुंचें: आग से कैसे लड़ें?
अमोनियम नाइट्रेट के खतरे
अमोनियम नाइट्रेट से जुड़े मुख्य जोखिमों में से एक है अपर्याप्त भंडारण. चूंकि यह एक बहुत ही ऑक्सीकरण पदार्थ है और यह कई अन्य यौगिकों के साथ प्रतिक्रिया करता है, यह ट्रिगर करता है a गैस की एक बड़ी मात्रा की रिहाई के साथ प्रतिक्रिया. अनुचित भंडारण ज्वलनशील उत्पादों के साथ संदूषण के अधीन है, गर्मी या गैस प्रतिधारण के संपर्क में है, विस्फोट का कारण क्या हो सकता है.
यह संयुक्त राज्य अमेरिका के टेक्सास में पहले ही हो चुका है, उदाहरण के लिए, एक मालवाहक जहाज जो फ्रांस से 2,086 टन अमोनियम नाइट्रेट लेकर आया था। दुर्घटना घटी १९४७ में और टेक्सास सिटी आपदा के रूप में जाना जाने लगा। इस त्रासदी में 581 लोगों की मौत हुई थी और यह अमोनियम कार्गो तक पहुंचने वाले जहाज में आग नहीं लगने के कारण हुआ, जिससे विस्फोट हुआ।
एक और उदाहरण था विस्फोट क्रम जो 4 अगस्त, 2020 को के बंदरगाह पर हुआ था बेरूत शहर, लेबनान, जिसमें 100 से अधिक लोग मारे गए और 5,000 घायल हो गए। विस्फोट की तीव्रता वहां संग्रहीत अमोनियम नाइट्रेट के 2,750 टन चार्ज की एक श्रृंखला प्रतिक्रिया के प्रज्वलन के कारण थी।
यह भी ध्यान देने योग्य है कि अमोनियम नाइट्रेट पैदा कर सकता है त्वचा और आंखों में जलन और, अगर साँस ली जाए, साँस लेने में तकलीफ. रक्तप्रवाह में, पदार्थ में जहरीली शक्ति होती है, क्योंकि यह शरीर के तरल पदार्थों के साथ प्रतिक्रिया करता है, और इस प्रतिक्रिया के उत्पाद, जैसे नाइट्रेट, स्वास्थ्य को नुकसान पहुंचा सकते हैं, जैसे कि ब्लू बेबी रोग, इन्फेंटाइल मेथेमोग्लोबिनेमिया (निम्न रक्त हीमोग्लोबिन) के रूप में भी जाना जाता है। कृषि क्षेत्र में जल निकायों के उर्वरकों में मौजूद अमोनियम नाइट्रेट से दूषित होने के कारण ग्रामीण क्षेत्रों में परिवारों में यह रोग बार-बार होता है।
लेसा बर्नार्डेस द्वारा
रसायन विज्ञान शिक्षक
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/quimica/nitrato-de-amonio.htm
