ऑस्मोस्कोपी है संयुक्त स्वामित्व (अन्य हैं टोनोस्कोपी, एबुलियोस्कोपी तथा क्रायोस्कोपी) जो की घटना का अध्ययन करता है असमस विभिन्न सांद्रता के दो समाधानों के बीच, जिनमें से एक दूसरे की तुलना में अधिक केंद्रित है।
नोट: कोलिगेटिव गुण तब होते हैं जब एक गैर-वाष्पशील विलेय को विलायक में मिलाया जाता है।
जैसे कि ऑस्मोस्कोपी ऑस्मोसिस का अध्ययन, जानना जरूरी है क्या है यह घटना। इसके लिए, हम नीचे दिए गए समाधानों का उपयोग करेंगे, जो एक अर्ध-पारगम्य झिल्ली द्वारा अलग किए गए हैं:
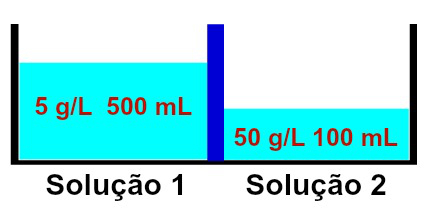
विभिन्न सांद्रता वाले समाधानों का प्रतिनिधित्व
यह देखा गया है कि घोल 1 में 5 g/L की सांद्रता और 500 mL का आयतन होता है, जबकि घोल 2 में 50 g/L की सांद्रता और 100 mL का आयतन है, जो एक झिल्ली द्वारा अलग किया गया है अर्धपारगम्य। समाधान 2 समाधान 1 की तुलना में अधिक केंद्रित है और इसलिए उनके बीच परासरण होना चाहिए।
ऑस्मोसिस अनिवार्य रूप से समाधान 1 से समाधान 2 तक होना चाहिए, क्योंकि समाधान 1 कम केंद्रित है। इस घटना के दौरान, विलायक का हिस्सा अर्ध-पारगम्य झिल्ली को पार कर जाता है, जिससे घोल का आयतन 2 हो जाता है वृद्धि और समाधान 1 की मात्रा घट जाती है, जब तक कि दोनों समाधानों में समान सांद्रता न होने लगे, अर्थात, आइसोटोनी।

परासरण की घटना के कारण समाधान 1 और 2 की ऊंचाई में संशोधन
नोट: आइसोटोनिक मीडिया वे हैं जिनकी एकाग्रता समान है।
के अनुसार ऑस्मोस्कोपीपरासरण होता है क्योंकि कम सांद्र विलयन में विलायक का अधिकतम वाष्प दाब अधिक सांद्र विलयन में विलायक के वाष्प दाब से अधिक होता है। अब, यदि हम परासरण की घटना को रोकना चाहते हैं, तो बस सबसे अधिक केंद्रित घोल पर दबाव डालें:
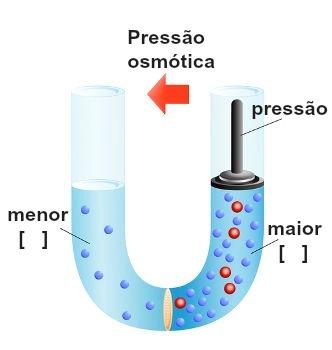
सबसे केंद्रित समाधान पर दबाव के निष्पादन का प्रतिनिधित्व
यह दबाव, जो ऑस्मोसिस को अवरुद्ध करने या यहां तक कि रिवर्स ऑस्मोसिस के लिए सबसे अधिक केंद्रित समाधान पर लगाया जाता है, कहलाता है परासरण दाब और प्रतीक द्वारा दर्शाया गया है। यह घोल की सांद्रता के सीधे आनुपातिक होना चाहिए।
आसमाटिक दबाव की संभावित व्याख्या
के निष्कर्षों के अनुसार ऑस्मोस्कोपी, प्रत्येक समाधान में एक आसमाटिक दबाव होता है, क्योंकि यह एकाग्रता से संबंधित होता है, प्रत्येक समाधान में मौजूद एक विशेषता।
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
एक माध्यम या एक समाधान की दूसरे से तुलना करते समय, हम निम्नलिखित शब्दों का उपयोग कर सकते हैं:
हाइपरटोनिक: जब एक माध्यम दूसरे की तुलना में अधिक आसमाटिक दबाव प्रस्तुत करता है;
हाइपोटोनिक: जब एक माध्यम का आसमाटिक दबाव दूसरे की तुलना में कम होता है;
आइसोटोनिक: जब दो माध्यमों या विलयनों का परासरण दाब समान होता है।
इस प्रकार, दो समाधान ए और बी के आसमाटिक दबावों की तुलना करते समय, द्वारा दर्शाया गया है π औरख, हम कह सकते हैं कि :
यदि ए और बी के आसमाटिक दबाव बराबर हैं, तो साधन या समाधान आइसोटोनिक होंगे:
π = πख
यदि ए का आसमाटिक दबाव बी के आसमाटिक दबाव से अधिक है, तो बी के संबंध में माध्यम ए हाइपरटोनिक होगा:
π> πख
यदि बी का आसमाटिक दबाव ए के आसमाटिक दबाव से कम है, तो बी के संबंध में माध्यम बी हाइपोटोनिक होगा:
πख< π
आसमाटिक दबाव की गणना के लिए सूत्र
= एम.आर.टी
इस सूत्र में:
π = आसमाटिक दबाव है
एम = है mol/L. में एकाग्रता
R = सामान्य गैस स्थिरांक है (0.082 atm में दाब के लिए; ६२.३ mmHg में दबाव के लिए)
टी = केल्विन में तापमान
जैसा कि mol/L में सांद्रता का एक विशेष सूत्र है, जैसा कि नीचे दिखाया गया है:
एम = म1
म1.वी
हम इसे आसमाटिक दबाव सूत्र में बदल सकते हैं:
π = म1.आर.टी
म1.वी
नोट: यदि विलयन में मौजूद विलेय आयनिक है, तो हमें इसका उपयोग करना चाहिए वैंट हॉफ सुधार कारक (i) आसमाटिक दबाव गणना की अभिव्यक्ति में:
= एम.आर.टी.आई
आसमाटिक दबाव गणना का उदाहरण
उदाहरण: (यूएफ-पीए) 25 डिग्री सेल्सियस पर 10 एमएल पानी में 2 मिलीग्राम एक नया एंटीबायोटिक युक्त एक समाधान 0.298 मिमीएचजी का एक आसमाटिक दबाव पैदा करता है। तो, इस एंटीबायोटिक का आणविक द्रव्यमान लगभग है:
ए) 3000
बी) 5200
ग) 7500
घ) 12500
ई) 15300
अभ्यास द्वारा प्रदान किए गए डेटा थे:
= ०.२९८ mmHg
टी = 25 हेसी या 298 के (273 के साथ जोड़ने के बाद)
म1 = 2 मिलीग्राम या 0.002 ग्राम (1000 से विभाजित करने के बाद)
वी = 10 एमएल या 0.01 एल (1000 से विभाजित करने के बाद)
आर = ६२.३ एमएमएचजी
इस अभ्यास को हल करने के लिए, आसमाटिक दबाव की गणना के लिए बस उपलब्ध डेटा को निम्नानुसार लागू करें:
π = म1.आर.टी
म1.वी
0,298 = 0,002.62,3.298
म1.0,01
0.298.एम981.0,01 = 37,1308
0.00298.एम1 = 37,1308
म1 = 37,1308
0,00298
म1 = १२४६० यू
मेरे द्वारा। डिओगो लोपेज डायस
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
DAYS, डिओगो लोपेज। "ऑस्मोस्कोपी क्या है?"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-osmoscopia.htm. 28 जून, 2021 को एक्सेस किया गया।