हे परमाणु कणों की संख्या की गणना किसी भी परमाणु या आयन में मौजूद प्रोटॉन (नाभिक में), इलेक्ट्रॉनों (इलेक्ट्रोस्फीयर में) और न्यूट्रॉन (नाभिक में) की मात्रा को इंगित करने के लिए उपयोग किया जाता है। ऐसा करने के लिए, परमाणुओं की कुछ विशेषताओं को जानना आवश्यक है:
1- परमाणु संख्या (जेड)
यह एक गणितीय कोड है, जो एक परमाणु के संक्षिप्त नाम के निचले बाएँ तरफ स्थित बड़े अक्षर Z द्वारा दर्शाया गया है:
जेडएक्स
यह नाभिक में प्रोटॉन (p) की संख्या और परमाणु के इलेक्ट्रोस्फीयर में इलेक्ट्रॉनों (e) की संख्या को इंगित करता है। तो, सामान्य शब्दों में:
जेड = पी = ई
2- मास संख्या (ए)
यह एक गणितीय कोड है जो किसी भी परमाणु के नाभिक में मौजूद प्रोटॉन (पी) और न्यूट्रॉन (एन) की संख्या के योग से मेल खाता है। द्रव्यमान संख्या का प्रतिनिधित्व करने वाला समीकरण निम्न द्वारा दिया गया है:
ए = पी + एन
चूँकि प्रोटॉनों की संख्या परमाणु संख्या के बराबर होती है, इसलिए हम द्रव्यमान संख्या की गणना के लिए समीकरण इस प्रकार लिख सकते हैं:
ए = जेड + एन
यदि हम परमाणु की द्रव्यमान संख्या और परमाणु संख्या जानते हैं, तो हम न्यूट्रॉन की संख्या निम्नानुसार निर्धारित कर सकते हैं:
एन = ए - जेड
3- आयनों
वे परमाणु हैं जो इलेक्ट्रॉनों को खो देते हैं या प्राप्त करते हैं। उनके पास उनके प्रतिनिधित्व के शीर्ष दाईं ओर स्थित एक सकारात्मक या नकारात्मक चिन्ह है, जैसा कि निम्नलिखित मॉडल में है:
एक्स+ या एक्स-
धनात्मक आयन: इसे धनायन कहा जाता है और धनात्मक चिह्न इंगित करता है कि इसने इलेक्ट्रॉनों को खो दिया है।
ऋणात्मक आयन: इसे ऋणायन कहते हैं और ऋणात्मक चिह्न यह दर्शाता है कि इसने इलेक्ट्रॉन ग्रहण किया है।
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
4- परमाणु समानताएं
ए) आइसोटोप
परमाणु जिनकी परमाणु संख्या समान और द्रव्यमान संख्या भिन्न होती है। उदाहरण:
7एक्स14 तथा 7यू16
परमाणु X और Y की परमाणु संख्या समान है (संक्षिप्त नाम के बाईं ओर), यानी 7 के बराबर। परमाणु X की द्रव्यमान संख्या (संक्षिप्त नाम के दाईं ओर) 14 के बराबर है, और परमाणु Y की द्रव्यमान संख्या 16 के बराबर है।
बी) आइसोबार
परमाणु जिनकी द्रव्यमान संख्या समान होती है और परमाणु क्रमांक भिन्न होते हैं। उदाहरण:
15एक्स31 तथा 13यू31
परमाणु X और Y की द्रव्यमान संख्या (संक्षिप्त नाम के दाईं ओर) 31 के बराबर है। दूसरी ओर, परमाणु X का परमाणु क्रमांक 15 है और परमाणु Y का परमाणु क्रमांक 13 है।
ग) आइसोटोन्स
परमाणु जिनकी द्रव्यमान संख्या और परमाणु संख्या भिन्न होती है, लेकिन न्यूट्रॉन की संख्या समान होती है।
डी) आइसोइलेक्ट्रॉनिक्स
जिन परमाणुओं में इलेक्ट्रॉनों की संख्या समान होती है। उदाहरण:
12एक्स+2 तथा 7यू-3
एटम एक्स की परमाणु संख्या 12 के बराबर है और यह एक धनायन है (धनात्मक आवेश +2 के साथ), इसलिए यह दो इलेक्ट्रॉनों को खो देता है, इस प्रकार इसके इलेक्ट्रोस्फीयर में 10 इलेक्ट्रॉन होते हैं। दूसरी ओर, परमाणु Y की परमाणु संख्या 7 के बराबर है और यह एक आयन है (ऋणात्मक आवेश -3 के साथ), इसलिए यह तीन इलेक्ट्रॉनों को प्राप्त करता है, इस प्रकार इसके इलेक्ट्रोस्फीयर में 10 इलेक्ट्रॉन होते हैं।
माइंड मैप: परमाणु कण
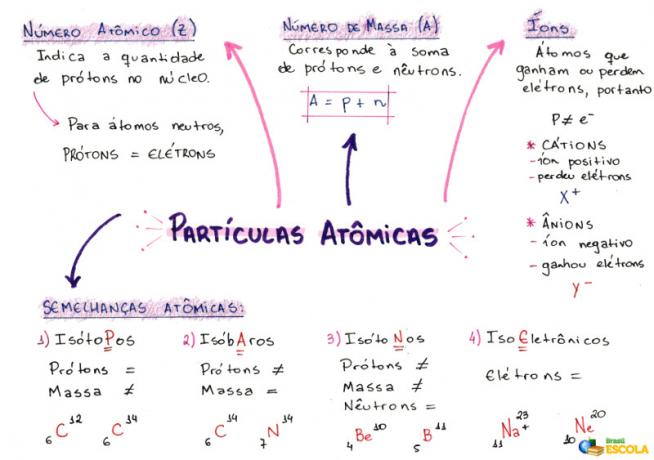
* माइंड मैप को पीडीएफ में डाउनलोड करने के लिए, यहाँ क्लिक करें!
परमाणु कणों की संख्या की गणना के उदाहरण
उदाहरण 1: परमाणु में प्रोटॉन, न्यूट्रॉन और इलेक्ट्रॉनों की संख्या निर्धारित करें 14एक्स29.
परमाणु X के लिए निम्नलिखित मान दिए गए थे:
द्रव्यमान संख्या (ऊपरी दाएं) = 29
परमाणु क्रमांक (नीचे बाएँ) = 14
प्रोटॉन की संख्या निर्धारित करने के लिए:
प्रोटॉन की संख्या हमेशा परमाणु संख्या के बराबर होती है, इसलिए X परमाणु में 14 प्रोटॉन होते हैं।
इलेक्ट्रॉनों की संख्या निर्धारित करने के लिए:
चूंकि परमाणु X एक आयन नहीं है, इसलिए इलेक्ट्रॉनों की संख्या प्रोटॉन की संख्या के बराबर है, अर्थात 14.
न्यूट्रॉन की संख्या निर्धारित करने के लिए:
न्यूट्रॉन की संख्या निम्न सूत्र में द्रव्यमान और प्रोटॉन की संख्या का उपयोग करके निर्धारित की जाती है:
ए = पी + एन
29 = 14 + एन
२९ - १४ =n
एन = 15
उदाहरण 2: आयन X. के प्रोटॉन, न्यूट्रॉन और इलेक्ट्रॉनों की संख्या निर्धारित करें+3, यह जानते हुए कि उनकी द्रव्यमान संख्या और परमाणु क्रमांक क्रमशः 51 और 23 हैं।
आयन X के लिए निम्नलिखित मान दिए गए थे:
द्रव्यमान संख्या = 51
परमाणु क्रमांक (नीचे बाएं) = 23
प्रोटॉन की संख्या निर्धारित करने के लिए:
प्रोटॉन की संख्या हमेशा परमाणु संख्या के बराबर होती है, इसलिए X परमाणु में 23 प्रोटॉन होते हैं।
इलेक्ट्रॉनों की संख्या निर्धारित करने के लिए:
आयन X धनात्मक (+3) है, इसलिए यह एक धनायन है जिसने तीन इलेक्ट्रॉनों को खो दिया है। अतः इसके इलेक्ट्रॉनों की संख्या 20 है।
ध्यान दें: इलेक्ट्रॉनों की संख्या में कमी या वृद्धि हमेशा परमाणु संख्या के संबंध में होती है।
न्यूट्रॉन की संख्या निर्धारित करने के लिए:
न्यूट्रॉन की संख्या निम्न सूत्र में द्रव्यमान और प्रोटॉन की संख्या का उपयोग करके निर्धारित की जाती है:
ए = पी + एन
51 = 23 + एन
51 - 23 =एन
एन = 28
उदाहरण 3: एक परमाणु W का परमाणु क्रमांक और द्रव्यमान क्रमशः 29 और 57 के बराबर होता है, जो a. का समद्विभाजक होता है परमाणु Y, जिसका परमाणु क्रमांक 30 है, जो एक परमाणु B का समस्थानिक है, जिसका द्रव्यमान संख्या है 65. इस जानकारी से परमाणु B में प्रोटॉन, न्यूट्रॉन और इलेक्ट्रॉनों की संख्या ज्ञात कीजिए।
अभ्यास द्वारा प्रदान किया गया डेटा:
परमाणु W
परमाणु क्रमांक (नीचे बाएँ) = 29
द्रव्यमान संख्या (ऊपरी दाएं) = 57
वाई आइसोबार, यानी वाई का द्रव्यमान भी 57 है।
वाई परमाणु
परमाणु क्रमांक = 30
द्रव्यमान संख्या = 57
इन दो मूल्यों के साथ, हमें इसकी न्यूट्रॉन संख्या निर्धारित करनी चाहिए क्योंकि यह तत्व बी का आइसोटोन है:
ए = जेड + एन
57 = 30 + एन
57 - 30 = एन
एन = 27
एक मक़बरा:
द्रव्यमान संख्या = 65
न्यूट्रॉनों की संख्या = 27
इन आंकड़ों के साथ, हमें इसकी परमाणु संख्या निर्धारित करनी चाहिए, क्योंकि इसके साथ, हम इसके प्रोटॉन की संख्या और इसके इलेक्ट्रॉनों की संख्या निर्धारित करेंगे (क्योंकि यह आयन नहीं है):
ए = जेड + एन
65 = जेड +27
65 - 27 = Z
जेड = 38
इसलिए, परमाणु B में 38 प्रोटॉन, 38 इलेक्ट्रॉन और 27 न्यूट्रॉन हैं।
* विक्टर रिकार्डो फरेरा द्वारा माइंड मैप Map
रसायन विज्ञान शिक्षक
मेरे द्वारा। डिओगो लोपेज डायस


