आयनीकरण वह रासायनिक परिघटना है जिसमें एक अम्लीय पदार्थ (जिसका सामान्य सूत्र HX है) पानी में घुलने पर दो आयनों को जन्म देता है: एक हाइड्रोनियम धनायन (H)3हे+ या हो+) और कोई भी आयन (X .)-). घटना को एक समीकरण से दर्शाया गया है। देखो:
एचएक्स + एच2ओ → एच3हे+ + एक्स-
एक आयनीकरण के दौरान, से केवल आयनीकरण योग्य हाइड्रोजन अम्ल वे हाइड्रोनियम केशन में बदल जाते हैं, एक ऐसा कारक जो इस एसिड की आयनीकरण क्षमता पर भी निर्भर करता है, यानी आयनीकरण (α) की डिग्री पर। इस प्रकार, सभी हाइड्रोजन हाइड्रोनियम नहीं बनाते हैं, जब तक कि एसिड में 100% के बराबर आयनीकरण की डिग्री न हो।
हालाँकि, जब हम एक आयनीकरण समीकरण का निर्माण, हम एसिड के आयनीकरण की डिग्री को ध्यान में नहीं रखते हैं, लेकिन मात्रा आयनीकृत हाइड्रोजन्स कि वह प्रस्तुत करता है।
एक नियम के रूप में, हम आयनीकरण योग्य हाइड्रोजन को एक हाइड्रोसिड में मौजूद सभी हाइड्रोजन मानते हैं। ऑक्सी अम्लों के मामले में, कार्बन परमाणुओं से बंधे हुए केवल हाइड्रोजन ही आयनीकृत होते हैं, जैसा कि नीचे दिखाए गए संरचनात्मक सूत्र में देखा जा सकता है:
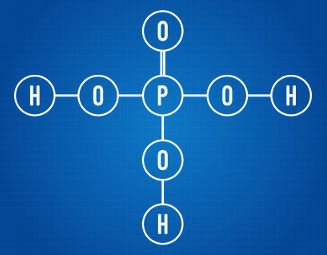
फॉस्फोरिक एसिड में तीन आयनीकरण योग्य हाइड्रोजेन होते हैं
ऊपर दिए गए संरचनात्मक सूत्र का विश्लेषण करते हुए, हम देख सकते हैं कि एसिड में तीन हाइड्रोजन परमाणु ऑक्सीजन परमाणुओं से बंधे होते हैं। इस प्रकार, इसमें कुल तीन आयनीकरण योग्य हाइड्रोजन होते हैं।
कुछ विधानसभा उदाहरण देखें कुछ अम्लों के आयनीकरण समीकरण का:
उदाहरण 1: हाइड्रोब्रोमिक एसिड (एचबीआर)
एचबीआर + एच2ओ → एच3हे+ + भाई-
हाइड्रोब्रोमिक एसिड इसकी संरचना में केवल एक हाइड्रोजन के साथ एक हाइड्रासिड है। चूंकि एक हाइड्रासिड में सभी हाइड्रोजन को आयनित किया जा सकता है, यह तब बनता है, जब यह पानी में घुल जाता है, केवल हाइड्रोनियम केशन का एक मोल यह है ब्रोमाइड आयन (Br-).
उदाहरण 2: हाइड्रोजन सल्फाइड (H .)2एस)
एच2वाई+ 2 एच2ओ → 2 एच+ + एस-2
हाइड्रोजन सल्फाइड इसकी संरचना में दो हाइड्रोजन के साथ एक हाइड्रासिड है। चूंकि एक हाइड्रासिड में सभी हाइड्रोजन को आयनित किया जा सकता है, यह पानी में घुलने पर बनता है, हाइड्रोनियम धनायनों के दो मोल यह है सल्फाइड आयन (S .)-2). इसके लिए हमने इस्तेमाल किया पानी के दो मोल।
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
उदाहरण 3: मैंगनिक अम्ल (H .)2एमएनओ4)
एच2एमएनओ4 + 2 एच2ओ → 2 एच3हे+ + एमएनओ4-2
मैंगनिक एसिड एक ऑक्सीएसिड है जिसकी संरचना में दो हाइड्रोजेन होते हैं। जैसा कि ऑक्सीएसिड में केवल ऑक्सीजन से बंधा हाइड्रोजन आयनित होता है - मैंगनिक एसिड के मामले में, दो हाइड्रोजेन होते हैं -, यह पानी में घुलने पर बनेगा, हाइड्रोनियम धनायनों के दो मोल यह है मैंगनेट आयन (MnO .)4-2). इसके लिए हमने इस्तेमाल किया पानी के दो मोल।
उदाहरण 4: फास्फोरस अम्ल (H Acid)3धूल3)
एच3धूल3 + 2 एच2ओ → 2 एच3हे+ + एचपीओ3-2
फॉस्फोरस एसिड एक ऑक्सीएसिड है जिसकी संरचना में तीन हाइड्रोजन होते हैं। जैसा कि ऑक्सीएसिड में केवल ऑक्सीजन से बंधी हाइड्रोजन आयनित होती है - फॉस्फोरस एसिड के मामले में, दो हाइड्रोजेन होते हैं -, यह पानी में घुलने पर बनेगा, हाइड्रोनियम धनायनों के दो मोल यह है फॉस्फेट आयन (HPO3-2). इसके लिए हमने इस्तेमाल किया पानी के दो मोल।
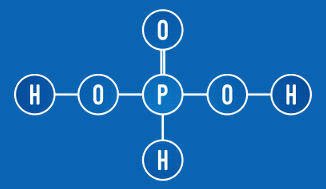
फॉस्फोरस अम्ल में दो आयनीकृत हाइड्रोजन (OH समूह) होते हैं।
उदाहरण 5: बोरिक एसिड (एच3बो3)
एच3बो3 + 3 एच2ओ → 3 एच+ + बीओ3-3
बोरिक एसिड एक ऑक्सीएसिड है जिसकी संरचना में तीन हाइड्रोजेन होते हैं। जैसा कि ऑक्सीएसिड में केवल ऑक्सीजन से बंधे हाइड्रोजन आयनित होते हैं - बोरिक एसिड के मामले में, तीन हाइड्रोजेन होते हैं -, यह पानी में घुलने पर बनेगा, हाइड्रोनियम धनायनों के तीन मोल यह है बोरेट आयन (BO .)3-3). इसके लिए हमने इस्तेमाल किया तीन मोल पानी।
उदाहरण 6: पाइरोफॉस्फोरिक एसिड (H .)4पी2हे7)
एच4पी2हे7 + 4 एच2ओ → 4 एच3हे+ + पी2हे7-4
पाइरोफॉस्फोरिक एसिड इसकी संरचना में चार हाइड्रोजन के साथ एक ऑक्सीएसिड है। जैसे ऑक्सीएसिड में केवल ऑक्सीजन से बंधी हाइड्रोजन आयनित होती है - बोरिक एसिड के मामले में, चार हाइड्रोजेन होते हैं -, यह पानी में घुलने पर बनेगा, हाइड्रोनियम धनायनों के चार मोल यह है ऋणायनपाइरोफॉस्फेट (पी2हे7-4). इसके लिए हमने इस्तेमाल किया चार मोल पानी।
मेरे द्वारा। डिओगो लोपेज डायस
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
DAYS, डिओगो लोपेज। "एसिड आयनीकरण समीकरण"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/quimica/equacoes-ionizacao-dos-acidos.htm. 28 जून, 2021 को एक्सेस किया गया।