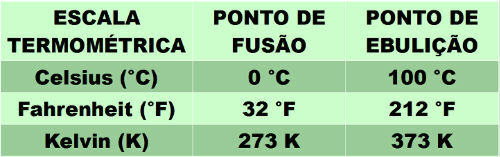
Chaleurlatent est le montant de énergiethermique qui est absorbé ou abandonné par un corps ou un système thermodynamique, lors d'un changement de son état physique, dans Température constante.
Lorsqu'une substance pure atteint sa température de La fusion ou alors ébullition, pendant votre échauffement, votre état physique commence à changer. Dans ce processus, il continue d'absorber de la chaleur, cependant, son Températurerestesconstant. Cela se produit parce que, en atteignant ces températures, dans lesquelles des changements d'état physique se produisent, toute la chaleur absorbée par le système thermodynamique est utilisée pour surmonter le énergiepotentiel qui maintient ses molécules ensemble. Dès que le système thermodynamique absorbe toute l'énergie nécessaire pour briser ses molécules, l'interaction entre elles diminue, indiquant que leur état d'agrégation a changé. Après le changement d'état physique, la chaleur absorbée isotherme continue d'être absorbée par les molécules, leur fournissant
énergiecinétique. Ce type de chaleur qui augmente l'énergie cinétique des molécules est appelé chaleur sensible.Voirégalement: Sept conseils « en or » pour une étude de physique plus efficace
O Chaufferlatent mesure la quantité de chaleur, par unité de masse, nécessaire pour tout changement de état physique du corps, donc, son unité de mesure, selon le système international (SI), est le Jouleparkilogramme (J/kg). Cependant, l'utilisation d'autres unités telles que le caloriepargramme (cal/g), est assez courant dans l'étude de la calorimétrie.
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
Types de chaleur latente
Il existe deux types de chaleur: o Chauffersiniveau C'est le Chaufferlatent. La chaleur sensible est celle qui est transférée entre les corps lorsqu'il y a des changements de température. La chaleur latente, à son tour, se produit lorsqu'il y a des transferts de chaleur sans changements de température.
La chaleur latente est altérée pour différents changements d'état physique. Découvrez les différents types de chaleur latente :
chaleur latentedansfusion (LF): c'est la chaleur qui est absorbée ou cédée par les corps au cours du processus de fusion: du liquide au solide et vice versa, à température constante.
chaleur latentedansvaporisation (LV): est celui qui est transféré lors des transformations solide-liquide ou liquide-solide, dans Température constante.
Voirégalement: Qu'est-ce que la capacité thermique ?
ExemplesdansChaufferlatent
Découvrez quelques situations du quotidien dans lesquelles il y a des échanges thermiques latents :
Lorsque nous chauffons l'eau, jusqu'à une température de 100°C, elle démarre le processus d'évaporation. Tant que toute l'eau ne se transforme pas en vapeur, sa température ne change pas.
Lorsque nous versons de l'eau sur une surface très chaude, toute l'eau se vaporise presque instantanément. Ce processus est appelé chauffage et implique l'absorption de chaleur latente.
Il y a échange de chaleur latente lorsque l'on touche une bouteille de soda à basse température et tout son contenu gèle rapidement à température constante, grâce à sa température inférieure au point de fusion de l'eau.
formule de chaleur latente
La chaleur latente est calculée par le rapport de la quantité de chaleur transférée lors de la transformation isotherme :
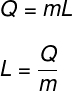
Q - quantité de chaleur transférée
m - masse corporelle
L - chaleur latente
Changements de phase et chaleur latente
Des changements de phase dans les substances pures se produisent dansTempératureconstant, en absorbant ou en libérant de la chaleur latente. Toutes les substances pures ont un courbe de chauffe similaire à l'image ci-dessous:
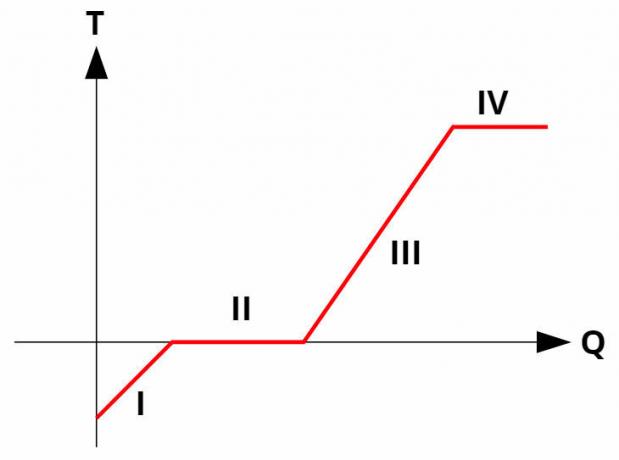
À courbesdanschauffage ils relient la température (axe des y) à la quantité de chaleur donnée ou reçue (axe des x). Dans les changements de phase (processus II et IV), la température reste constante, bien qu'il y ait toujours un échange de chaleur.
Voir aussi: Fondamentaux de la calorimétrie
table de chaleur latente
Dans des conditions normales de Température et pression, ô Chaufferlatent de l'eau, pour ses différents changements d'état physique, est indiqué dans le tableau ci-dessous :
Transformation |
Chaleur latente (cal/g) |
Fusion (0°C) |
80 |
Solidification (0°C) |
-80 |
Vaporisation (100°C) |
540 |
Condensation (100°C) |
-540 |
D'après le tableau ci-dessus, 80calories geler 1 grammed'eau à la température de fusion (0 °C). Les signes négatifs dans le processus de solidification et condensation indiquent que de la chaleur a été libérée en eux, donc ces deux transformations sont exothermique. Le tableau ci-dessous montre la chaleur latente dans J/kg, pour les mêmes procédés :
Transformation |
Chaleur latente (J/kg) |
Fusion (0°C) |
333.103 |
Solidification (0°C) |
-333.103 |
Vaporisation (100°C) |
2,2.106 |
Condensation (100°C) |
-2,2.106 |

exercices de chaleur latente
1) Un récipient contient 500 g d'eau liquide. Sans changement de température de l'eau, tout son contenu est soudainement évaporé. Déterminez la quantité de chaleur transférée au contenu de ce récipient.
Données: LF = 540 cal/g
Résolution:
Pour calculer la quantité de chaleur nécessaire à l'évaporation de cette masse d'eau, nous utiliserons la formule suivante :
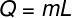
En utilisant les données fournies par l'exercice, nous ferons le calcul suivant :
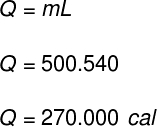
Par moi Rafael Helerbrock
Souhaitez-vous référencer ce texte dans un travail scolaire ou académique? Voir:
HELERBROCK, Rafael. "Chaleur latente"; École du Brésil. Disponible en: https://brasilescola.uol.com.br/fisica/calor-latente.htm. Consulté le 27 juin 2021.