O point de fusion et d'ébullition sont respectivement les températures auxquelles les matériaux passent du solide au liquide et du liquide. pour le gaz ou la température maximale à laquelle le liquide peut rester dans cet état physique dans un pression.
Les points de fusion et d'ébullition des éléments chimiques du tableau périodique varient en fonction de leurs numéros atomiques, ce qui signifie alors qu'ils sont des propriétés périodiques.
Dans le tableau périodique, l'ordre de croissance des températures de fusion et d'ébullition des éléments chimiques suit le schéma de flèche suivant :
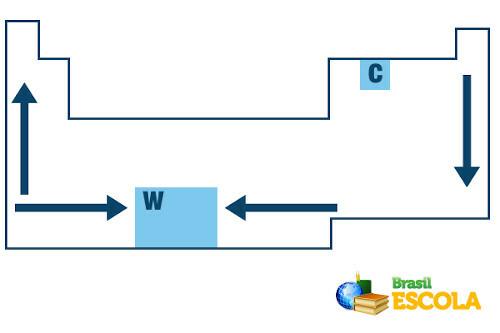
Croissance du point de fusion et d'ébullition dans le tableau périodique
Notez que lorsque l'on considère les éléments appartenant à la même famille sur le côté gauche du tableau, le les points de fusion et d'ébullition diminuent à mesure que le numéro atomique de l'élément augmente, c'est-à-dire de bas en en haut. Cela peut être vu dans les valeurs de point de fusion et d'ébullition à 1 atm pour les éléments de la famille 1 indiqués ci-dessous :

Points de fusion et d'ébullition des éléments de la famille 1
Du côté droit du tableau périodique, c'est l'inverse qui se produit, le sens de croissance du point de fusion et d'ébullition des éléments appartenant à la même famille augmente de haut en bas. Par conséquent, les éléments ayant les températures de fusion et d'ébullition les plus basses sont situés en haut du tableau. La seule exception est le carbone, qui a un point de fusion de 3550 °C et un point d'ébullition de 4287 °C.
Sinon, la plupart de ceux qui ont des points de fusion et d'ébullition bas sont soit des gaz, soit des liquides à température ambiante au niveau de la mer. Comme c'est le cas pour les gaz rares, l'azote, l'oxygène, le fluor et le chlore, qui se trouvent dans la partie supérieure droite du tableau.
Or, lorsqu'il s'agit d'éléments appartenant à la même période (même rangée dans le Tableau), on constate que les points de fusion et d'ébullition augmentent des côtés vers le centre du Tableau. Voir l'exemple pour les éléments de la deuxième période :
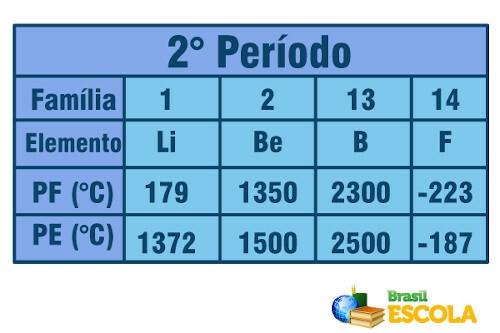
Point de fusion et point d'ébullition pour les éléments de la deuxième période du tableau périodique
Le tungstène (W) est un élément qui se trouve au centre du tableau périodique et son point de fusion est le plus élevé parmi les métaux, étant égal à 3422 °C. C'est pourquoi il est utilisé dans les filaments des ampoules à incandescence, car il peut résister à des températures élevées sans fondre.
Par Jennifer Fogaça
Diplômé en Chimie
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/ponto-fusao-ebulicaopropriedades-periodicas.htm
