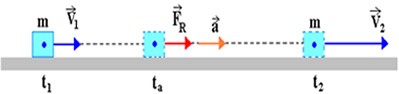
Que veut dire dire qu'un gaz a subi une transformation gazeuse ?
Pour répondre à la question initiale, il est important de rappeler que l'état du gaz ou l'état gazeux est déterminé par les variables d'état: pression, volume et température. Bientôt, un transformation de gaz ce n'est rien de plus qu'une situation dans laquelle une certaine quantité de gaz subit une variation dans l'une de ses trois variables d'état. Chaque fois qu'une variable subit un changement, une autre changera par conséquent de valeur.
Au XVIIe siècle, plusieurs scientifiques ont mené des expériences afin de découvrir les particularités des transformations des gaz. Parmi eux, on peut citer: Torriceli, Robert Boyle, Mariotte, Guericke, entre autres. Dans ses études, la procédure consistait à changer l'une des variables d'état et à observer le comportement des autres. Ce faisant, ils ont observé que pour déterminer de manière significative la relation entre une variable et un autre, il fallait faire en sorte que le troisième ne change pas, c'est-à-dire qu'il reste constant. Ainsi, les investigations ont été menées de trois manières différentes, chacune avec ses particularités, il s'agit de:
transformation isotherme, transformation isobare et transformation isovolumétrique.Avant de détailler les trois transformations évoquées ci-dessus, rappelons ce que Loi générale sur les gaz parfaits: D'après cette loi, une masse de gaz initialement définie par des variables d'état (p1,V1 et T1), lors d'une transformation gazeuse, il a les variables d'état (p2,V2 et T2) qui caractérisent l'état final du gaz. Ces variables suivent la relation suivante :
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)

À partir de l'équation ci-dessus, nous pouvons voir que la pression, le volume et la température varient au cours de la transformation du gaz.
Transformation isotherme ouLa loi de Boyle-Mariotte: est la transformation dans laquelle la température T du gaz reste constant, faisant varier sa pression P et son volume V. La liste suivante est valide :

Transformation isobare ouLoi Gay-Lussac : est la transformation dans laquelle la pression P du gaz reste constant, variant son volume V et la température T. La liste suivante est valide :
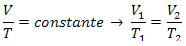
Transformation isovolumétrique ou loi de Charles: également connu sous le nom de transformation isométrique, est la transformation dans laquelle le volume V du gaz reste constant, faisant varier sa pression P et la température T. La liste suivante est valide :

Par Nathan Augusto
Diplômé en Physique
Souhaitez-vous référencer ce texte dans un travail scolaire ou académique? Voir:
FERREIRA, Nathan Augusto. « Transformations gazeuses »; École du Brésil. Disponible en: https://brasilescola.uol.com.br/fisica/as-transformacoes-gasosas.htm. Consulté le 27 juin 2021.