Les amines sont des composés organiques résultant du remplacement d'un ou plusieurs hydrogènes de l'ammoniac (NH3) par des groupes organiques. Symbolisant ces radicaux par R, nous avons que leur groupe fonctionnel peut être identifié des trois manières ci-dessous :
R ─ NH2 ou alors R NH R’ ou alors RN─R’
│
R"
Les composés appartenant à cette fonction organique sont très importants dans notre vie quotidienne et dans notre propre organisme, remplissant des fonctions biologiques très importantes, telles qu'elles apparaissent dans les acides aminés qui forment les protéines fondamentales pour êtres vivants.
Industriellement, ils sont également largement utilisés, comme dans la vulcanisation du caoutchouc, dans la production de savons, de médicaments et dans d'innombrables synthèses organiques. Beaucoup, malheureusement, sont utilisés comme médicaments.
En tant que telles, de nombreuses amines sont souvent connues sous des noms communs. Voir quelques exemples :
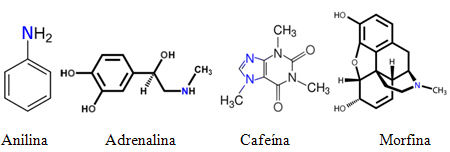
Cependant, il n'est pas possible pour toutes les amines connues d'être appelées uniquement par des noms communs similaires à ceux mentionnés. Des règles de nommage sont nécessaires pour que n'importe qui dans le monde puisse effectuer des expériences avec la même substance, que sa structure est facilement identifiable par son nom et vice versa.
Ainsi, l'IUPAC a établi que la nomenclature des amines doit respecter la règle suivante :
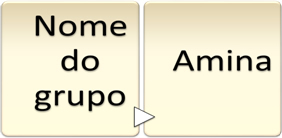
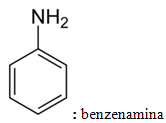
Cette règle ne s'applique qu'aux amines primaires, c'est-à-dire dans laquelle un seul atome d'hydrogène d'ammoniac a été remplacé par un radical ayant le groupe fonctionnel suivant: R ─ NH2.
Exemples:
H3C NH2: méthanamine
H3C CH2 NH2: éthanamine
H3C CH2 CH2 CH2 NH2: butane-1-amine
Lorsqu'il y a des branches ou des insaturations dans la chaîne, il est nécessaire de numéroter la chaîne en commençant par l'extrémité la plus proche du groupe NH2 et montrer dans quel carbone il se produit:
NH2
│
H3C CH ─ CH2 CH2 CH2 CH3: hexane-2-amine
NH2
│
H3C CH2 CH2 C ═ CH ─ CH3: hex-2-en-3-amine
CH3 NH2
│ │
H3C CH CH CH2 CH3: 2-méthyl-pentan-3-amine
CH3 NH2
│ │
H3C CH ─ CH2 CH─CH3: 4-méthyl-pentan-2-amine
En cas de amines secondaires et tertiaires (qui ont respectivement deux et trois hydrogènes du groupe ammoniac substitués), la règle est différente :

Le nom de ces amines est précédé de la lettre N pour indiquer que le substituant est attaché à un atome d'azote et les substituants dans la chaîne carbonée sont généralement indiqués par des nombres.
Exemples:
H3C CH2 CH2 NH ─ CH2: N-méthyl-propanamine
CH3 CH3
│ │
H3C CH ─ CH2 NON ─ CH2 CH3: N-éthyl-2,N-diméthyl-propanamine
H3C─N─CH2 CH3: N-diméthyl-éthanamine
│
CH3
H3C─N─CH2 CH3: N-méthyl-éthan-1-amine
│
H
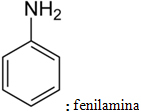
Il existe deux types de nomenclature usuelle pour les amines. La première suit le schéma suivant :

Exemples:
H3C NH2: méthylamine
H3C CH2 NH2: éthylamine
H3C CH2 CH2 CH2 NH2: butylamine
H3C─N─CH2 CH3: éthyl-diméthylamine
│
CH3
H3C─N─CH2 CH3: éthylméthylamine
│
H
H3C─N─CH3: triméthylamine
│
CH3
La triméthylamine est le principal composant de l'odeur nauséabonde du poisson pourri.
L'autre nomenclature usuelle considérer le groupe NH2 comme étant une branche de la chaîne carbonée et est indiqué par le préfixe “aminé”. La chaîne la plus longue est la principale et le reste est la branche. Voir les exemples :
CH3 CH3
│ │
H3Ç1 C2 C3H C4H2 C5H3: 2-amino-2,3-diméthyl-pentane
│
NH2
CH2 CH2 CH2 CH2 : 1,4-diamino-butane
│ │
NH2 NH2
CH2 CH2 CH2 CH2 CH2 : 1,5-diaminopentane
│ │
NH2 NH2
Ces deux derniers composés sont connus dans la vie courante respectivement sous le nom de putrescine et de cadavérine, des amines qui se forment lors de la décomposition des cadavres humains.
Par Jennifer Fogaça
Diplômé en Chimie
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/nomenclatura-das-aminas.htm
