Lorsque le cycle benzénique a déjà un substituant, ce radical influencera toutes les autres substitutions H sur le cycle. Ce substituant peut être ortho et para-directeur ou méta-directeur. Mais les questions se posent :
| Qu'est-ce qui fait que le groupe attaché au cycle benzénique influence la direction et la réactivité de la réaction de substitution ? |
| Qu'est-ce qui fait que certains groupes ciblent des conseillers (désactivants) et d'autres des ortho-para (activants) ? |
Ces deux questions sont répondues par la compréhension des appels. effets électroniques que ces groupes exercent sur le ring. Cet effet se produit en raison de la différence d'électronégativité entre les éléments, car le substituant polariser les liaisons du noyau aromatique, induisant alternativement un caractère positif à certains carbones du cycle, tandis que d'autres restent avec un caractère négatif.
| Une nouvelle substitution se produira dans les atomes de carbone qui ont le caractère négatif. |
Voyons comment ces effets électroniques se produisent dans le cycle aromatique, en gardant à l'esprit l'ordre d'électronégativité des éléments: F > O > N > Cl > Br > S > C > I > H.
1er cas: Radical activateur ou ortho-directeur:
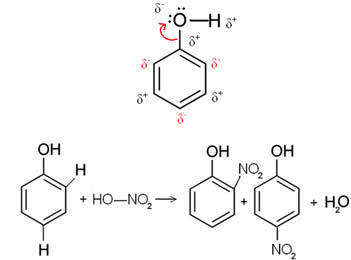
Par exemple, dans le cas situé sous la molécule de benzol (phénol), l'oxygène est l'élément le plus électronégatif, donc il attire les électrons sur lui-même, ce qui fait que le carbone a une charge partiellement positive, ce qui induit polarisation en anneau alterné. Les positions négatives sont exactement les positions ortho et para. C'est pourquoi le groupe -OH est un radical activateur ou ortho-à-directeurs. Ceci peut être vu dans la réaction de nitration du phénol ci-dessous, donnant naissance à l'o-nitrophénol et au p-nitrophénol en tant que produits :
2ème cas: désactiver radical ou méta-leader:
Considérons maintenant le cas du nitrobenzène :
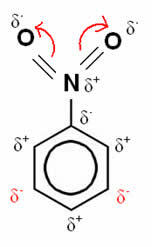
Dans cet exemple, l'oxygène reste l'élément le plus électronégatif, il attire donc vers lui les liaisons faites avec l'azote, qui est partiellement chargée positivement, induisant l'atome de carbone qui y est attaché à devenir polarisé négativement et ainsi successivement. Ainsi, la position qui devient négative et la plus susceptible de substitution est la position but, étant donc un désactiver.
Voyez maintenant plus en détail cet effet électronique, qui s'appelle effet de résonance.
| effet de résonance c'est l'attraction ou la répulsion des électrons sur les liaisons π (pi) des liaisons doubles ou triples, lorsqu'elles entrent en résonance avec le cycle benzénique lui-même. |
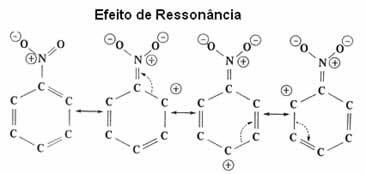
Comme on le voit, le groupe NO2 désactive l'anneau, car il en retire des électrons et diminue sa densité électronique. Ainsi, le groupe qui va attaquer et faire la substitution (électrophile) est positif, il va donc attaquer préférentiellement la position méta qui a reçu une charge négative.
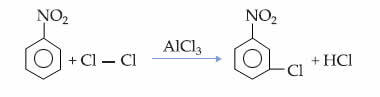
Ce fait peut être vu dans la réaction de monochloration du nitrobenzène, dans laquelle la substitution ne se produit qu'en position méta :
Par Jennifer Fogaça
Diplômé en Chimie
Équipe scolaire du Brésil
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/efeitos-eletronicos-radicais-meta-orto-para-dirigentes.htm