diffusion et épanchement sont deux lois proposées par le chimiste écossais Thomas Graham, au XIXe siècle, sur la base de ses études sur mélanges de gaz et le comportement de des gaz en traversant les parois d'un conteneur.
Parmi les observations faites par Thomas Graham sur le comportement des gaz vis-à-vis de la diffusion et de l'effusion, on peut souligner les suivantes :
Un gaz a toujours tendance à traverser de petits trous présents dans la matière à l'état solide ;
Plus le masse moléculaire gaz, plus sa difficulté à passer à travers les trous de la matière solide est grande;
Plus la densité du gaz est faible, plus sa vitesse de déplacement est grande ;
Plus la température à laquelle est soumis un gaz est élevée, plus la vitesse à laquelle il se répand dans l'environnement ou passe par un orifice est élevée ;
- Un gaz ne reste jamais statique à un endroit particulier.
La diffusion
La diffusion c'est un phénomène physique qui consiste en la capacité d'un gaz à se diffuser (c'est-à-dire à se répandre) dans l'espace d'une zone ou à l'intérieur d'un conteneur. Pour cette raison, on peut dire qu'à l'intérieur d'un espace, un gaz n'est jamais confiné à un seul endroit.

Représentation de la survenance d'une diffusion
De plus, nous pouvons définir la la diffusion toujours comme étant la capacité qu'un gaz a de se mélanger avec un autre, lorsqu'il est placé dans le même récipient, formant un mélange gazeux homogène.
Un exemple est lorsque des gaz sortent des échappements des véhicules. Aussi toxiques soient-ils, ils ne causent pas de dommages à court terme à l'homme, car ils se répandent dans l'air atmosphérique, réduisant ainsi leur concentration.
Effusion
Effusion c'est un phénomène physique qui consiste en le passage d'un gaz à travers des trous existant dans les parois d'un certain récipient, c'est-à-dire qu'il consiste en la sortie d'un gaz d'un environnement à un autre.

Représentation de la survenance d'un épanchement
Un exemple est lorsque les ballons sont gonflés pour une fête et, le lendemain, ils sont tous dégonflés, tout cela à cause de l'air s'échappant par les trous contenus dans les ballons.
Calculs liés à la diffusion et à l'épanchement
On peut calculer, selon les équations proposées par Graham, la vitesse à laquelle un gaz s'exécute diffusion ou épanchement. Selon Graham, les vitesses de diffusion et d'effusion de deux gaz mélangés dans un récipient sont toujours inversement proportionnelle au carré de leurs densités relatives ou de leurs masses molaires.
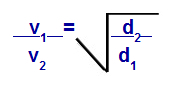
La loi de Graham concernant la densité
v1 = vitesse (effusion ou diffusion) du gaz 1 dans le mélange ;
v2 = vitesse (effusion ou diffusion) du gaz 2 dans le mélange ;
ré1 = densité du gaz 1 du mélange ;
ré2 = densité du gaz 2 du mélange ;
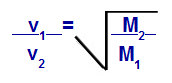
La loi de Graham concernant la masse molaire
v1 = vitesse (effusion ou diffusion) du gaz 1 dans le mélange ;
v2 = vitesse (effusion ou diffusion) du gaz 2 dans le mélange ;
M1 = masse molaire du gaz 1 du mélange ;
M2 = masse molaire du gaz 2 dans le mélange.
Par moi Diogo Lopes Dias
La source: École du Brésil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-difusao-efusao.htm

