Oxydation de l'énergie dans alcynes est une réaction organique qui se produit lorsqu'un alcyne (un hydrocarbure qui a une triple liaison entre deux carbones) est ajouté à une solution acide avec le réactif de baeyer (Permanganate de potassium - KMnO4).
REMARQUE: une réaction de oxydation énergétique peut être réalisé avec du bichromate de potassium (K2Cr2O7), et pas seulement le permanganate de potassium.
Chaque fois qu'une réaction de l'oxydation énergétique dans les alcynes est effectuée, les produits qui peuvent être générés sont acides carboxyliques, l'eau (le seul élément qui apparaît dans l'un d'eux) et le dioxyde de carbone (CO2).
Réactif Baeyer en milieu acide
Lorsque le réactif de Baeyer est mélangé à de l'eau, en présence d'un acide (substance capable de libérer des ions H+), la formation de deux oxydes (oxyde de potassium et oxyde de manganèse II) et les oxygènes naissants ([O]).

Mécanismes d'oxydation de l'énergie dans les alcynes
1er mécanisme : rompre la triple liaison.
Initialement, la triple liaison est attaquée par les oxygènes naissants formés par le réactif de Baeyer. Cette attaque provoque la rupture complète de la triple liaison.
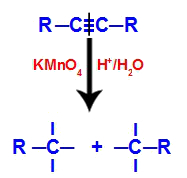
Perturbation de la triple liaison par l'attaque des oxygènes naissants
Lorsque la triple liaison est rompue, l'alcyne est divisé en deux parties. Sur chacun des carbones qui formaient une triple liaison, trois valences libres apparaissent.
2ème mécanisme : Interaction des groupes hydroxyles
Chacune des valences libres sur les carbones où se trouvait la triple liaison est occupée par des groupes hydroxyle (OH), formant un polyol (de l'alcool avec plusieurs hydroxyles).
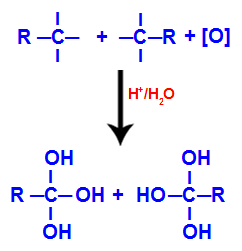
Formation de polyol avec des groupes hydroxyle après clivage de la triple liaison
REMARQUE: Si le carbone où se trouvait la triple liaison a un atome d'hydrogène qui lui est attaché, cet atome d'hydrogène recevra un oxygène naissant et formera également un autre hydroxyle.
3ème Mécanisme: Formation de molécules d'eau
Lorsqu'un carbone a deux groupes OH ou plus, il devient une structure très instable en raison de la présence d'éléments extrêmement électronégatifs. Ainsi, en raison de l'instabilité, la molécule subit une auto-déshydratation, c'est-à-dire qu'un hydroxyle se lie à l'hydronium (H+) à partir d'un autre hydroxyle et forme de l'eau.

Formation de molécules d'eau à partir de deux hydroxyles présents dans le polyol formé
4ème Mécanisme : Formation du produit
Après la formation de molécules d'eau, le carbone perd une liaison en raison de la sortie d'un hydroxyle, et l'oxygène de l'autre hydroxyle perd également une liaison qui se faisait avec un hydrogène. Par conséquent, entre ce carbone et l'oxygène, une double liaison apparaît, qui forme un carbonyle (C=O) et stabilise les deux.
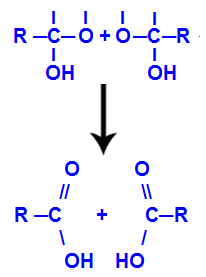
Formation de carbonyle dans les deux structures obtenues à partir d'alcyne
Exemple d'équation d'oxydation de l'énergie dans les alcynes
Exemple: Oxydation énergétique du But-1-ino
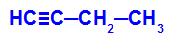
Formule développée du but-1-yne
Lorsque le but-1-yne est placé dans un milieu contenant le réactif de Bayer, de l'eau et de l'acide, la liaison se rompt. triple existant entre les carbones 1 et 2, en raison de l'attaque des oxygènes naissants existant au milieu, comme dans l'équation mugissement:
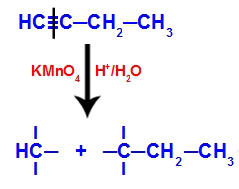
Rupture des connexions but-1-yne
Après la rupture de la triple liaison, les carbones 1 et 2 reçoivent trois hydroxyles, mais le carbone 1 en aura un de plus car il avait un atome d'hydrogène (qui se lie à un oxygène naissant), formant deux polyols (fragment 1 et 2).

Équation représentant la formation de polyols
Peu de temps après, comme les polyols sont instables, nous avons la formation de molécules d'eau à partir des hydroxyles. Dans le fragment 1, une molécule d'eau apparaît (car il y a trois hydroxyles) et, dans le fragment 2, deux molécules apparaissent (car il y a quatre hydroxyles).
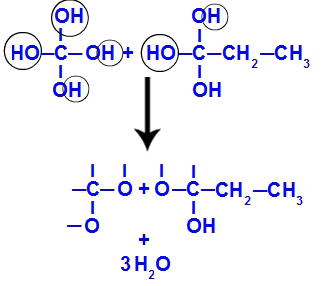
Formation de molécules d'eau à partir de fragments but-1-yne
Enfin, on a la formation d'une double liaison entre les carbones qui ont perdu de l'hydroxyle et les oxygènes qui ont perdu de l'hydrogène, ce qui donne naissance à des carbonyles.

Formation de carbonyles dans les fragments but-1-yne
Avec l'équation ci-dessus, nous pouvons voir que le but-1-yne a donné naissance à un acide carboxylique et à du dioxyde de carbone (CO2).
Par moi Diogo Lopes Dias
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/oxidacao-energetica-alcinos.htm

