O Diagramme de phases est un graphique utilisé pour indiquer les conditions de température et pression nécessaire pour obtenir un substance dans un certain état physique (solide, liquide ou gazeux).
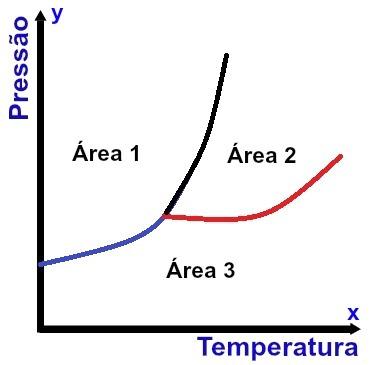
Représentation d'un diagramme de phase
L'axe x (horizontal) contient les valeurs de température et l'axe y (vertical) contient les valeurs de pression. De plus, il existe trois courbes reliées à un seul point (appelé point triple), divisant le graphique en trois zones bien définies, comme on peut le voir sur le schéma ci-dessus.
En plus d'indiquer les conditions pour que la substance soit dans un état physique spécifique, la Diagramme de phases indique les conditions pour que tout changement d'état physique se produise.
Les changements d'état physique sont :
La fusion: passage de l'état solide à l'état liquide ;
Solidification: passage de l'état liquide à l'état solide ;
Vaporisation: passage de l'état liquide à l'état gazeux ;
Condensation: passage de l'état gaz à l'état liquide ;
Sublimation: passage de l'état solide à l'état gazeux ;
Resublimation: passage de l'état gazeux à l'état solide.
a) Régions
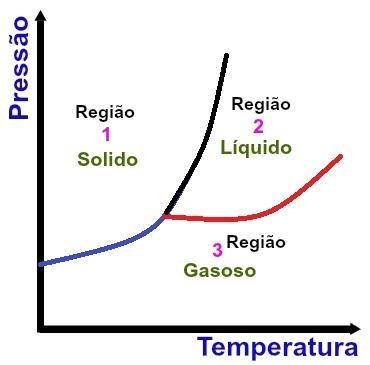
Régions fondamentales d'un diagramme de phase
Région 1
La région 1 indique les conditions de température et de pression dans lesquelles on retrouve la substance à l'état solide.
Région 2
La région 2 indique les conditions de température et de pression dans lesquelles on retrouve la substance à l'état liquide.
Région 3
La région 3 indique les conditions de température et de pression dans lesquelles on retrouve la substance à l'état gazeux.
b) Courbes

Courbes présentes dans un diagramme de phase
Courbe A (courbe violette)
C'est la courbe qui divise la région solide et gazeuse du diagramme de phase et est communément appelée la courbe de resublimation. Chaque point situé sur la courbe 1 indique que nous avons une certaine substance coexistant à l'état solide et gazeux.
En plus d'indiquer la coexistence, la courbe 2 indique également les conditions de température et de pression pour la transformation d'une substance d'un état liquide à un état gazeux.
Courbe B (courbe noire)
C'est la courbe qui divise la région solide et liquide du diagramme de phases et est communément appelée la courbe de solidification. Chaque point situé sur la courbe 2 indique que nous avons une certaine substance coexistant à l'état solide et gazeux.
En plus d'indiquer la coexistence, la courbe 2 indique également les conditions de température et de pression pour la transformation d'une substance à l'état liquide en un état solide.
Courbe C (courbe rouge)
C'est la courbe qui divise la région solide et gazeuse du diagramme de phases et est communément appelée la courbe de condensation. Chaque point situé sur la courbe 3 indique que nous avons une certaine substance coexistant à l'état solide et gazeux.
En plus d'indiquer la coexistence, la courbe 3 indique également les conditions de température et de pression pour la transformation d'une substance d'un état solide à un état gazeux et vice versa.
c) Le point triple
Le point où les trois courbes du diagramme de phase se rencontrent est appelé le point triple. A ce stade, on a la valeur de température et la valeur de pression à laquelle on retrouve la substance à la fois à l'état solide, liquide et gazeux.

d) Changements d'état physique dans le diagramme de phase
Dans le diagramme de phase ci-dessous, nous avons 6 flèches qui indiquent la direction des changements d'états physiques d'une substance.

Flèche 1: indique la fusion
Flèche 2: indique la solidification
Flèche 3: indique la vaporisation
Flèche 4: indique la condensation
Flèche 5: indique la sublimation
Flèche 6: indique la resublimation
Par moi Diogo Lopes Dias
La source: École du Brésil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-diagrama-fases.htm
