UN nomenclature des hydrocarbures se caractérise principalement par la présence du suffixe « -o ». Ces règles de nomenclature sont définies par l'Union internationale de chimie pure et appliquée, à travers un livre populairement connu sous le nom de "The Blue Book".
Les hydrocarbures (fonction organique qui n'a que du carbone et de l'hydrogène dans sa structure), cependant, varient l'infixe, car ils peuvent être saturés (comme les alcanes et les cycloalcanes) et insaturés (comme les alcènes, les alcynes et les cycloalcènes). Les aromatiques (comme le benzène) ont également un système de nomenclature spécifique, peu différent cependant des chaînes fermées.
A lire aussi: Comment connaître la nomenclature des composés à fonctions mixtes ?
Résumé sur la nomenclature des hydrocarbures
Tous les hydrocarbures ont le suffixe "-o".
Les règles de dénomination sont définies par l'Union internationale de chimie pure et appliquée, IUPAC.
Bien qu'ils ne varient pas dans le suffixe, les hydrocarbures varieront dans l'infixe, étant "-an-" pour ceux qui ont chaîne saturée, "-en-" pour ceux avec une double liaison et "-in" pour ceux avec une double liaison tripler.
Les aromatiques, comme le benzène, ont leur propre système de nomenclature, un peu différent des autres. hydrocarbures, mais avec des similitudes par rapport au système de nomenclature des composés de la chaîne fermé.
Cours vidéo sur la nomenclature des hydrocarbures
Quelle est la règle de dénomination des hydrocarbures ?
Les Hydrocarbures, ainsi que tous les autres composés de la Chimie Organique, ont leurs noms officiels (ou systématiques) déterminés par l'IUPAC (en portugais, Union internationale de chimie).
Ces règlements sont mis à jour de temps à autre et sont inclus dans le livre Nomenclature de la chimie organique: recommandations IUPAC et noms préférés, dont la traduction libre peut être Organic Chemistry Nomenclature: IUPAC Recommendations and Preferred Names. Un tel livre est communément appelé "The Blue Book" de l'IUPAC.
Hydrocarbures, selon la réglementation en vigueur, doit toujours avoir le suffixe "-o".
nomenclature des alcanes
les alcanes sont des hydrocarbures qui ont une chaîne ouverte et saturée. Par conséquent, ont, en plus du suffixe "-o" d'hydrocarbures, l'infixe "-an-", indiquant uniquement des liaisons simples entre les atomes de carbone.
Exemples:
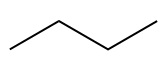
Le préfixe "mais-" est utilisé pour indiquer 4 atomes de carbone dans la chaîne.
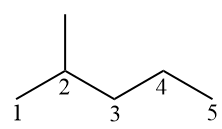
S'il y a des ramifications dans l'alcane, celles-ci doivent avoir le moins de ramifications possible.. Ainsi, la chaîne principale (pentane) doit commencer sa numérotation à partir de l'extrémité la plus à gauche, de sorte que le méthyle ait le numéro le plus bas possible (2).
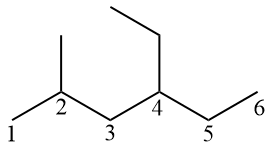
La chaîne principale doit être numérotée de gauche à droite, de sorte que les branches soient aux carbones 2 et 4. Si elles étaient numérotées de droite à gauche, les branches seraient sur les carbones 3 et 5, qui seraient plus longs.
Bien que le méthyle reçoive le numéro le plus bas, dans la nomenclature officielle, les branches (ou radicaux) doivent être dans l'ordre alphabétique. Par conséquent, l'éthyle (qui commence par E) vient avant le méthyle (qui commence par M). En portugais, un trait d'union doit être utilisé avant les mots commençant par la lettre H. Ainsi, nous utilisons un trait d'union dans « méthylhexane » mais pas dans « méthylpentane ».
Voir aussi: Quelle est la nomenclature des alcanes à plus de dix carbones ?
nomenclature des alcènes
Les alcènes sont des hydrocarbures qui ont également une chaîne ouverte, mais qui ont une double liaison entre les atomes de carbone, ce qui les rend insaturés. Cela entraîne un changement de nom par rapport aux alcanes, qui est le remplacer l'infixe "-an-" des alcanes par "-en-". De plus, les doubles liaisons, selon Iupac, doivent également être numérotées. Les doubles liaisons doivent également être aussi peu nombreuses que possible et avoir la priorité sur les branches.
Exemples:
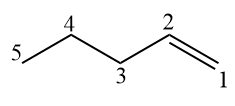
Pour les alcènes à plus de 3 carbones, la double liaison doit être numérotée à côté de l'infixe "-en-" au nom officiel.
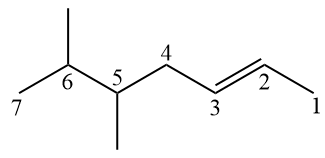
Entre une branche et une double liaison, la priorité est donnée à la double liaison pour en avoir le moins possible.
nomenclature des alcadiènes
Les Alcadiens sont des hydrocarbures qui ont deux doubles liaisons. L'infixe reste "-en-", mais avec le ajout du descripteur numérique "di-" précédant "-en-" pour indiquer qu'il y a deux doubles liaisons. En termes de phonétique, la lettre "a" est ajoutée après le préfixe de la chaîne principale.
Exemple:
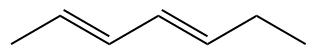
nomenclature des alcynes
les alcynes sont des hydrocarbures qui ont les mêmes particularités que les règles des alcènes, à la différence près qu'ils possèdent une triple liaison au lieu d'une double liaison. Cela apporte également une différence dans l'infixe, avec remplacer l'infixe "-en-" par "-in-".
Exemples:
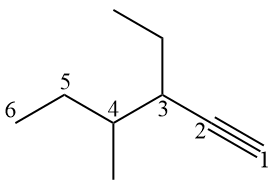
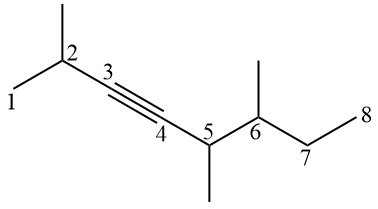
Étant donné que le carbone sp a une géométrie linéaire, il est courant de représenter l'alcyne avec une géométrie linéaire dans la triple liaison, ce qui rend difficile le comptage des carbones au début. L'idée est de visualiser les liaisons π, qui limitent les carbones qui y sont présents.
Nomenclature des cycloalcanes
Les cycloalcanes sont des hydrocarbures à chaîne fermée et saturés. Ainsi, dans son nom officiel, aura le préfixe "ciclo-" devant le nom de la chaîne principale, ainsi que l'infixe "-an-", chaînes saturées traditionnelles.
Exemples:

Les cycloalcanes monosubstitués (avec une branche) ne doivent pas avoir de numérotation pour la branche dans le nom officiel, car elle est redondante (après tout, la branche doit être en position 1).
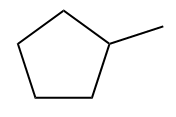
Cependant, s'il y a plus de deux succursales, celles-ci doivent être numérotées normalement au nom officiel, avec le numéro 1 prioritaire par ordre alphabétique. Ensuite, la numérotation doit tourner dans le sens des aiguilles d'une montre ou dans le sens inverse des aiguilles d'une montre afin que les autres branches aient le plus petit nombre possible.
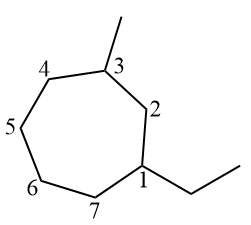
Notez que la branche éthyle porte le numéro 1, car la lettre E précède la lettre M, pour le méthyle, dans l'alphabet. Ensuite, la numérotation du cycle tournait dans le sens inverse des aiguilles d'une montre, de sorte que la branche méthyle avait le numéro le plus bas possible (3).
Nomenclature des cycloalcènes
Les cycloalcènes sont des hydrocarbures qui ont une chaîne insaturée et, par conséquent, avoir l'infixe "-en-". Étant ramifiés, la priorité sera donnée aux insaturations, tout comme les alcènes.
Exemples:
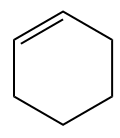
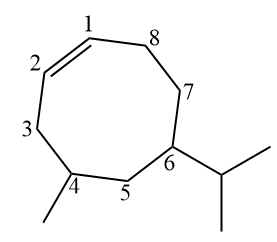
Dans le cas de la structure ramifiée précédente, les carbones 1 et 2 seront toujours ceux du double, mais ils seront numérotés de manière à ce que les branches aient le plus petit nombre possible. L'isopropyle, cependant, est en avance sur le méthyle en termes d'ordre alphabétique et s'écrit donc en premier (I vient avant M).
Nomenclature des aromatiques
Les hydrocarbures aromatiques ont des structures qui ont obligatoirement des cycles ou des cycles hexagonaux contenant trois doubles liaisons alternées. Au lycée, une bonne partie de l'étude des hydrocarbures aromatiques est retenue benzène (C6H6). Le benzène suit les recommandations de l'IUPAC pour les hydrocarbures à chaîne fermée, mais le nom « benzène » est accepté pour la chaîne principale.
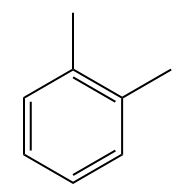
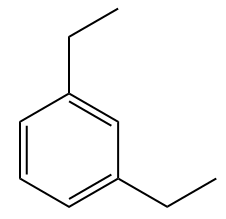
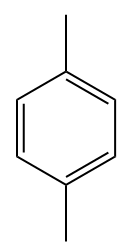
Pour les composés benzéniques disubstitués, Iupac ne recommande plus officiellement l'utilisation des descripteurs d'emplacement ortho (o), meta (m) et para (p), mais ces localisateurs sont encore largement utilisés dans les tests et les concours et seront donc cités ici.
Exemples:

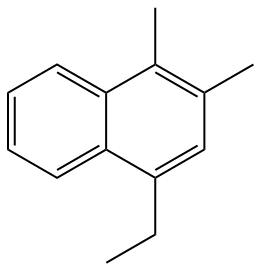
Le naphtalène, qui se compose de deux cycles benzéniques condensés, a un nombre fixe, selon l'IUPAC :
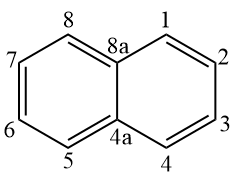
Par conséquent, la structure suivante doit être nommée selon la numérotation fixe.
A savoir aussi: Quelles sont les principales fonctions organiques ?
Exercices résolus sur la nomenclature des hydrocarbures
question 1
(IME) L'isoprène est un composé organique toxique qui est utilisé comme monomère pour la synthèse d'élastomères, par des réactions de polymérisation. Compte tenu de la structure de l'isoprène, quelle est sa nomenclature Iupac ?

A) 1,3-butène
B) 2-méthylbutadiène
C) 2-méthylbutène
D) pentadiène
E) 3-méthyl-butadiène
Résolution:
Variante B.
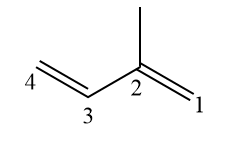
La numérotation de la structure est représentée dans l'image précédente. Avec la ramification au carbone 2 (les ramifications doivent avoir le plus petit nombre possible), l'insaturation ne peut être qu'aux carbones 1 et 3, sans autre position possible. Par conséquent, ils sont omis du nom officiel, car il est redondant de dire buta-1,3-diène.
Par conséquent, le nom reste le 2-méthylbutadiène.
question 2
(UEG) L'hydrocarbure ci-dessous, selon les règles de nomenclature IUPAC (International Union of Pure and Applied Chemistry), est le
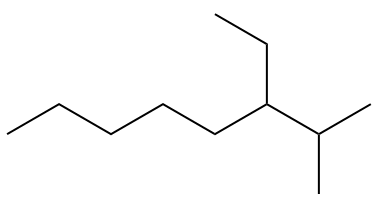
A) 3-éthyl-2-méthyloctane.
B) 6-éthyl-7-méthyloctane.
C) 3-isopropyloctane.
D) 2-méthyl-3-éthyloctane.
Résolution:
Variante A.
Notez la numérotation de l'hydrocarbure en question dans l'image ci-dessous.
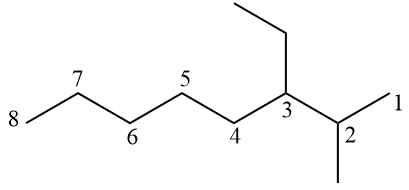
Les succursales doivent être aussi peu nombreuses que possible, donc la numérotation commence à l'extrême droite. Lors de l'écriture du nom officiel, les branches doivent être placées par ordre alphabétique: 3-éthyl-2-méthyloctane.
Source
FAVRÉ, H. UN.; POWELL, W. H.; MOUSS, G. P Nomenclature de la Chimie Organique. Recommandations IUPAC et noms préférés 2013. Londres: Société royale de chimie, 2013.
Par Stefano Araujo Novais
Professeur de chimie
Source: École du Brésil - https://brasilescola.uol.com.br/quimica/nomenclatura-dos-hidrocarbonetos.htm
