LA distillation fractionnée est un procédé utilisé pour séparer des mélanges homogènes formés par au moins deux liquides miscibles. La séparation par cette méthode est basée sur les différents points d'ébullition des composants du mélange.
Ce type de séparation est généralement appliqué aux mélanges qui ont des composants avec une différence de point d'ébullition d'environ 25 °C.
L'appareil principal du processus est le colonne de fractionnement, également appelée colonne de distillation, qui comporte une série d'obstacles à l'intérieur pour empêcher tous les composants du mélange de se volatiliser en même temps.
Fondamentalement, le mélange est chauffé dans un ballon de distillation jusqu'à ce que l'état physique du composant avec le point d'ébullition le plus bas change. Ensuite, la vapeur passe à travers une colonne fractionnée, qui sépare les fractions, puis le condenseur fait revenir la substance à l'état liquide afin qu'elle soit dirigée vers le récipient de collecte.
La distillation fractionnée est largement utilisée dans les industries et les laboratoires, ayant une grande importance commerciale. Exemples d'applications: purification de l'eau, séparation des composants pétroliers et séparation de l'air liquéfié.
Le pétrole, par exemple, est un mélange d'hydrocarbures, comme le butane (PE 20 °C), l'essence (PE 150 °C) et le kérosène (PE 300 °C). Par conséquent, l'ordre de séparation des composants dans la distillation fractionnée du point d'ébullition le plus bas au plus élevé est: le butane, l'essence et le kérosène.
Équipement de distillation fractionnée
Dans la distillation fractionnée, un système composé des parties suivantes est utilisé :
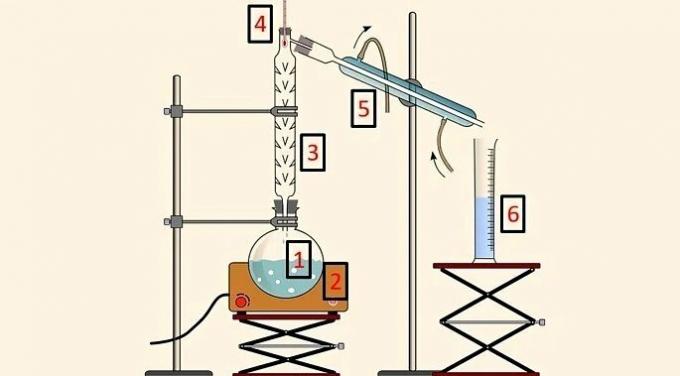
- Ballon de distillation (1), qui contient le mélange ;
- Couverture chauffante (2), qui fournit de la chaleur au mélange ;
- Colonne de distillation (3), qui permet la séparation en fonction de la température ;
- Thermomètre (4), pour suivre l'évolution de la température ;
- Condenseur (5), pour refroidir le composant évaporé ;
- Bécher (6), pour recueillir le composant séparé à l'état liquide.
Processus de séparation dans la distillation fractionnée
Tout d'abord, le mélange est placé dans le ballon de distillation avec les granulés anti-collision pour éviter une évaporation rapide.
La colonne fractionnée est reliée au ballon de distillation. Au fur et à mesure que le mélange est chauffé, la vapeur monte dans la colonne, dont l'intérieur est tapissé d '«obstacles», généralement en billes de verre ou de porcelaine.
Le contact du fluide à l'intérieur de la colonne fait perdre de la chaleur aux substances du mélange lors de leur passage dans l'équipement et seul le composant ayant le point d'ébullition le plus bas monte en tête de colonne.
La vapeur qui atteint le condenseur est alors refroidie jusqu'à ce qu'elle se liquéfie, c'est-à-dire qu'elle revienne à l'état liquide et soit recueillie dans le ballon récepteur.
A lire aussi: Qu'est-ce que la distillation ?
Distillation fractionnée du pétrole
L'huile est un mélange complexe de composés organiques et les différents composants séparés dans le processus de distillation sont appelés fractions. Les fractions de pétrole sont formées d'hydrocarbures, tels que l'essence, le diesel, le kérosène et le bitume.
Les fractions sont séparées dans le tour de distillation, une colonne en acier remplie de plateaux qui présentent des "obstacles" pour le passage de l'huile.
Initialement, l'huile est chauffée dans un four et le mélange chauffé est introduit au fond d'une tour de distillation. La température de la tour est plus élevée en bas et plus basse en haut pour éviter que les fractions les plus lourdes ne s'évaporent avec les composants les plus légers.
Les hydrocarbures à chaîne carbonée plus longue sont condensés et éliminés au bas de la tour. Ces fractions sont sombres, visqueuses et plus difficiles à évaporer. Ceux à chaîne unique, en revanche, ont des points d'ébullition plus bas et, par conséquent, se condensent à des températures plus proches du sommet de la tour, où ils sont collectés.
en savoir plus sur raffinage de pétrole.
Différence entre distillation simple et fractionnée
La distillation simple est appliquée lorsque l'on veut séparer un solide dissous dans un liquide. Pour cela, on chauffe le mélange jusqu'à évaporation du solvant. Ce processus est plus rapide et nécessite moins d'énergie que la distillation fractionnée.
Un exemple de mélange qui peut être séparé par simple distillation est l'eau et le sel. L'eau, ayant un point d'ébullition très inférieur au sel de table, s'évapore lorsque le mélange est chauffé et, après avoir traversé un condenseur, elle est recueillie dans un autre récipient.
La distillation fractionnée est appliquée à la séparation de liquides miscibles entre eux, tels que l'eau et l'acétone.
Acquérir plus de connaissances avec le contenu :
- Distillation simple et fractionnée
- Séparation du mélange
- Exercices de séparation des mélanges
Références bibliographiques
BRUN, T. L.; LEMAY JR., H. ET.; BURSTEN, B. ET.; BURGE, J. R La chimie la science fondamentale. 9e éd. Pearson Prentice Hall do Brasil, 2008.
USBERCO, J.; SALVADEUR, E. Chimie générale. 12e éd. São Paulo: Saraiva, 2006.
RUSSEL J B Chimie générale. vol. 1. Makron, 1996.
- Distillation
- Distillation simple et fractionnée
- raffinage de pétrole
- Exercices de séparation des mélanges
- Séparation des mélanges
- Matériaux utilisés au laboratoire de Chimie
- verrerie de laboratoire
- Exercices sur la chimie organique avec corrigés