Lorsqu'une substance est chauffée, elle reçoit de l'énergie de telle sorte que ses molécules s'agitent, commencent à occuper un plus grand volume, c'est-à-dire qu'elles se dilatent. L'inverse se produit lorsqu'une substance est refroidie, car elle perd de l'énergie et ses molécules ont tendance à être très proches les unes des autres, provoquant une contraction de volume. Ceci amène, normalement, la matière à l'état solide à occuper moins de volume que lorsqu'elle est à l'état liquide.
Contrairement à ce qui se passe avec la plupart des substances, l'eau a un comportement anormal: lorsqu'elle est chauffée, entre les intervalles de 0 et 4º C, elle souffre contraction puis elle commence à se dilater, c'est-à-dire que lorsque l'eau est à l'état solide, elle a un volume plus important qu'à l'état liquide dans cet intervalle de Température. Ce comportement irrégulier de l'eau peut être représenté par le graphique suivant :
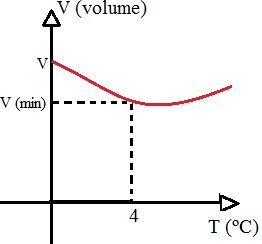
Le volume d'eau diminue entre 0 et 4°C puis commence à augmenter
Si le volume d'eau diminue pendant cet intervalle et que sa masse est maintenue constante, par conséquent le
densité d'eau, qui est le rapport entre la masse et le volume, sera maximale lorsque l'eau est à 4ºC. Regardez le graphique :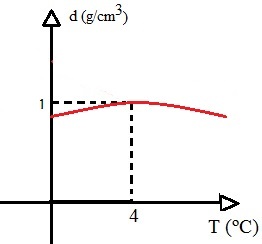
Ce graphique montre que la densité de l'eau est maximale lorsque la température est de 4°C
Mais quelle est la raison de la dilatation anormale de l'eau? Cette explication se trouve dans leur composition moléculaire. Les molécules d'eau sont liées par des liaisons chimiques appelées Liaisons hydrogène.
Lorsque la température de l'eau augmente, au-dessus de 0 °C, les liaisons hydrogène commencent à se rompre, provoquant un rapprochement entre les molécules. Cet effet surmonte l'agitation thermique moléculaire, qui provoque l'écartement des molécules et leur fait occuper un volume plus important de telle sorte que leur volume rétrécit.
Lorsque la température dépasse 4 °C, le nombre de liaisons hydrogène est déjà très faible. De cette façon, la distanciation moléculaire commence à prévaloir, avec, par conséquent, une augmentation de son volume.
Ce comportement irrégulier de l'eau explique plusieurs phénomènes naturels, dont le fait que la glace flotte sur l'eau, ce qui est ce qui se passe dans les régions très froides, où la surface des lacs est gelée alors qu'au fond l'eau reste liquide. Comme l'eau a une densité maximale à 4°C, elle reste au fond, créant une convection thermique, qui est un échange de chaleur en raison de la différence de densité.
Par Mariane Mendès
Diplômé en Physique
La source: École du Brésil - https://brasilescola.uol.com.br/fisica/a-agua-seu-comportamento-irregula.htm

