Les molécules des substances ne sont pas toutes droites, comme si elles étaient dans un seul plan. Après tout, ils sont dispersés dans l'espace et leurs atomes prennent des arrangements ou des arrangements différents. Ainsi, il existe différentes formes géométriques pour les molécules de chaque type de substance.
L'une des façons les plus simples de déterminer la géométrie d'une molécule est basée sur la théorie de répulsion des paires d'électrons de la couche de valence (RPECV). Selon cette théorie, les paires d'électrons de l'atome central fonctionnent comme nuages électroniques qui se repoussent. De cette façon, ils sont orientés aussi loin que possible les uns des autres. La géométrie moléculaire dépendra du nombre de paires électroniques autour de l'atome central.
Ce nuage électronique peut être composé d'électrons qui participent à des liaisons (simples, doubles ou triples) et aussi qui n'y participent pas. Nous avons donc:
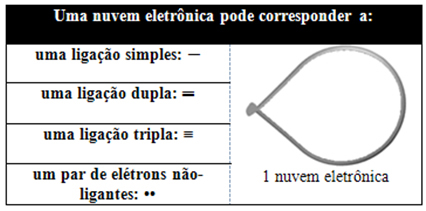
Il est utile de penser à ce nuage comme à un ou plusieurs ballons captifs, avec l'atome central au centre d'eux. Par exemple, dans une molécule qui n'a que deux nuages d'électrons autour de l'atome central, le plus grand distance possible entre eux est un angle de 180º et, par conséquent, la géométrie de la molécule sera linéaire.
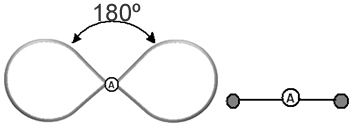
Par conséquent, nous pouvons déduire à quoi ressemblera la géométrie moléculaire de la plupart des molécules si nous prenons en compte le nombre d'atomes dans les molécules, et les liaisons que l'atome central fait, en vérifiant s'il a ou non des paires de électrons.
Voir les exemples ci-dessous :
- Molécules à 2 atomes: seront toujours linéaire
Par exemple:
H H, H Cl, F F, O O, C ≡ O.
- Molécule à 3 atomes: angulaire ou triangulaire
si l'atome central posséder une paire d'électrons non-liants la géométrie sera angulaire, comme dans le cas de la molécule SO2:
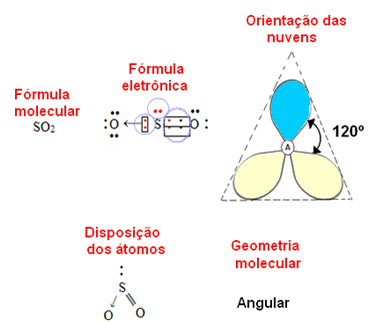
Considérez le nuage d'électrons bleu pour représenter des paires d'électrons qui ne participent pas aux liaisons, et le jaune pour représenter des paires d'électrons qui participent aux liaisons.
- Molécule à 4 atomes: plan trigonal (ou triangulaire) ou pyramidal (ou pyramide trigonale)
Si l'atome central n'a pas de paire d'électrons non appariés (non liés), la géométrie moléculaire est trigonale plate (ou triangulaire). Regardez l'exemple BF3:

Si l'atome a des paires d'électrons non liantes, la géométrie de la molécule sera pyramidale (ou pyramide trigonale), comme dans le cas de l'ammoniac :

- Molécule à 5 atomes: tétraédrique
Exemple de géométrie du méthane :
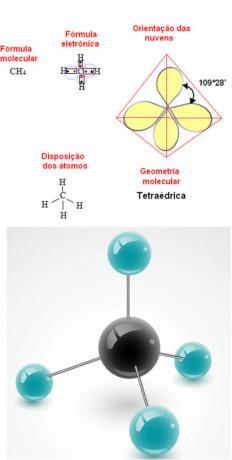
- Molécule à 6 atomes: bipyramide trigonale ou pyramide triangulaire.
Un exemple est le pentachlorure de phosphore (PCl5), qui a des connexions entre le phosphore et le chlore à un angle de 90º et d'autres de 120º, formant une bipyramide à base triangulaire :
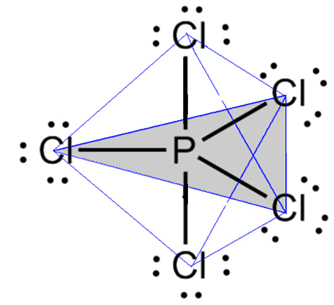
- Molécule à 7 atomes: octaédrique
Exemple: hexafluorure de soufre (SF6), dont les angles sont de 90º.

Par Jennifer Fogaça
Diplômé en Chimie
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/determinacao-geometria-das-moleculas.htm

