Les hydrocarbures sont des composés formés uniquement de carbone et d'hydrogène, de formule générale: CXHoui.
Il s'agit d'une quantité importante de substances, dont les plus connues sont des constituants du pétrole et du gaz naturel.
Le squelette d'un hydrocarbure est constitué de carbone et, à son tour, les atomes d'hydrogène se lient par une liaison covalente.
Ils sont largement utilisés dans l'industrie chimique, étant essentiels dans la production de dérivés du pétrole: carburants, polymères, paraffines, entre autres.
Propriétés des hydrocarbures
| interaction moléculaire | Ce sont des composés pratiquement non polaires et leurs molécules sont reliées par un dipôle induit. |
|---|---|
| Point de fusion et d'ébullition | Ils sont faibles par rapport aux composés polaires. |
| états d'agrégation |
|
| Densité | Ils ont une densité inférieure à celle de l'eau. |
| Solubilité | Ils sont insolubles dans l'eau et solubles dans les substances non polaires. |
| Réactivité |
|
Classification des hydrocarbures
Quant à la forme de la chaîne carbonée principale, les hydrocarbures sont classés en :
hydrocarbures aliphatiques
Formé par des chaînes carbonées ouvertes ou acycliques, qui ont des carbones terminaux.
- alcanes
- alcènes
- Alcynes
- Alcadiènes
Exemple:
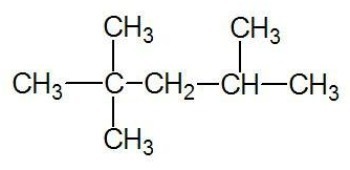
Voir aussi: chaînes de carbone
Hydrocarbures cycliques
Formé par des chaînes carbonées fermées ou cycliques qui n'ont pas de carbones terminaux.
- Cyclanes
- Cycles
- cyclistes
- Aromatiques
Exemples:
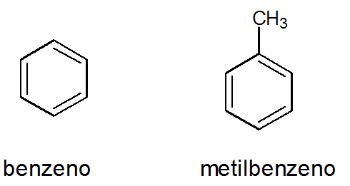
Voir aussi: benzène
Quant aux liaisons des chaînes carbonées, qu'elles soient simples, doubles ou triples :
Hydrocarbures saturés
Les composés sont formés par des liaisons simples entre les atomes de carbone et d'hydrogène.
- alcanes
- Cyclanes
Exemple:
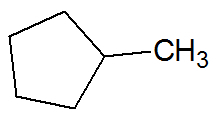
hydrocarbures insaturés
Les composés formés ont des doubles ou triples liaisons entre les atomes de carbone et d'hydrogène.
- alcènes
- Alcynes
- Alcadiènes
- Cycles
- cyclistes
- Aromatiques
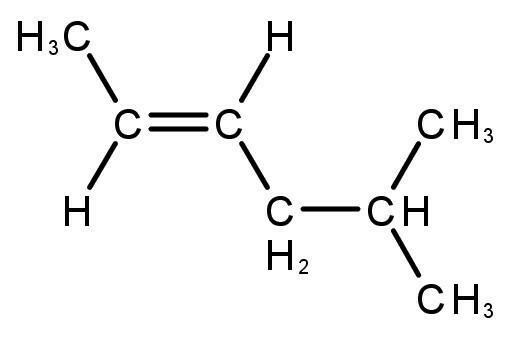
Lisez aussi sur:
- Liaisons chimiques
- Chimie organique
- Fonctions organiques
Nomenclature
La nomenclature des hydrocarbures est définie par les termes suivants :
| PRÉFIXE | INTERMÉDIAIRE | SUFFIXE |
|---|---|---|
| Indique le nombre de carbones présents dans la chaîne. | Type de lien trouvé dans la chaîne. | Identification du groupe fonctionnel. |
| PRÉFIXE | INTERMÉDIAIRE | SUFFIXE | ||
|---|---|---|---|---|
| 1C | RENCONTRÉ | Lien unique seulement | UN | O |
| 2C | HE | |||
| 3C | SOUTENIR | une double liaison | FR | |
| 4C | MAIS | |||
| 5C | PENT | deux doubles liaisons | DIEN | |
| 6C | HEX | |||
| 7C | HEPT | un triple lien | DANS |
|
| 8C | OCT | |||
| 9C | NON | Deux triples maillons | DIIN | |
| 10C | DÉC |
Exemples
Suivez la formation des noms d'hydrocarbures :
| Éthane |
- Préfixe: HE, ce qui correspond à 2 carbones.
- Intermédiaire: UN, qui correspond à des liens simples.
- Suffixe: O, qui correspond à la fonction hydrocarbonée.
Regardez les autres exemples :
| Propane | |
| Éthène | |
| Etino | |
| propadiène |
Dans certains cas, il est nécessaire d'indiquer la position de la double ou triple liaison. La numérotation doit commencer à l'extrémité la plus proche de ce lien.
| 1,3-butadiène | |
| 1-butyne |
En savoir plus sur:
- Butane
- Méthane
Types d'hydrocarbures
Découvrez les principaux types d'hydrocarbures, leurs caractéristiques et les composés utilisés :
alcanes
Ce sont des hydrocarbures à chaîne ouverte avec des liaisons simples entre les atomes de carbone et d'hydrogène, dont la formule générale est ÇnonH2n+2.
Caractéristiques des alcanes
- On les appelle aussi paraffines ou paraffines.
- On les trouve dans la nature dans le gaz naturel et le pétrole.
- Sont utilisés comme combustibles: gaz de cuisine, essence, gasoil, etc.
Exemples d'alcanes

alcènes
Ce sont des hydrocarbures à chaîne ouverte et ont une double liaison, dont la formule générale est ÇnonH2n.
Caractéristiques des alcènes
- Ils sont également appelés oléfines, alcènes ou hydrocarbures éthyléniques.
- Ils sont obtenus industriellement à partir du craquage d'alcanes présents dans le pétrole.
- Ils sont utilisés comme matière première dans l'industrie: plastiques, colorants, explosifs, etc.
Exemples d'alcènes

Alcynes
Ce sont des hydrocarbures à chaîne ouverte avec présence d'une double liaison, dont la formule générale est ÇnonH2n-2.
Caractéristiques des alcynes
- Ils sont plus réactifs que les alcanes et les alcènes en raison de la triple liaison.
- Les alcynes avec plus de 14 atomes de carbone sont solides.
- L'alcyne le plus utilisé est l'acétylène, couramment utilisé dans la production de caoutchoucs synthétiques, de fibres textiles et de plastiques.
Exemples d'alcynes

Alcadiènes
Ce sont des hydrocarbures à chaîne ouverte et la présence de deux doubles liaisons, dont la formule générale est ÇnonH2n-2
Caractéristiques des alcadiènes
- Aussi appelés diènes ou dioléfines
- On les trouve dans la nature dans les terpènes, qui sont extraits des huiles essentielles de fruits.
- Le composé le plus connu est l'isoprène, présent dans le caoutchouc naturel et les huiles essentielles.
Exemples d'alcadiènes

Cyclanes
Ce sont des hydrocarbures à chaîne fermée avec des liaisons simples entre les atomes de carbone et d'hydrogène, dont la formule générale est ÇnonH2n.
Caractéristiques des cyclanes
- Ils sont également appelés cycloalcanes ou cycloparaffines.
- Ils sont instables lorsqu'ils sont soumis à une pression élevée.
- Les chaînes de plus de 6 carbones sont stables, tandis que les chaînes de moins de 5 carbones sont réactives.
Exemples de cyclanes

Cycles
Ce sont des hydrocarbures à chaîne fermée avec la présence d'une double liaison, dont la formule structurelle est ÇnonH2n-2.
Caractéristiques des cyclènes
- On les appelle aussi cycloalcènes.
- Les composés de 3 à 5 carbones sont instables.
- On les trouve généralement dans le gaz naturel, le pétrole et le pétrole.
Exemples de cyclènes
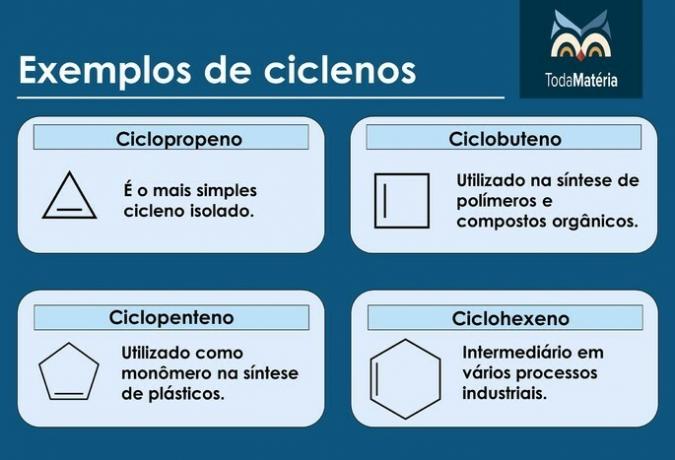
cyclistes
Ce sont des hydrocarbures à chaîne fermée avec la présence d'une triple liaison, dont la formule structurelle est ÇnonH2n-4.
Caractéristiques du cyclisme
- Ils sont également appelés cycloalcynes ou cycloalcynes.
- Ce sont des hydrocarbures cycliques et insaturés.
- Ils sont instables en raison de la triple liaison et ne se trouvent pas dans la nature.
Exemples de cyclines

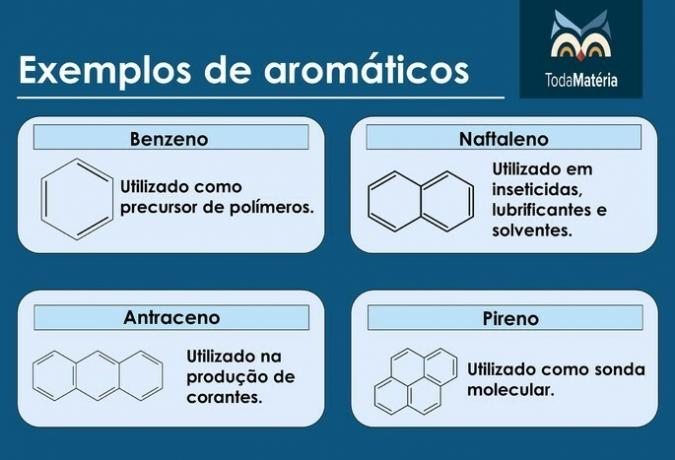
Aromatiques
Ce sont des hydrocarbures à chaîne fermée avec des liaisons simples et doubles alternées.
Caractéristiques des aromatiques
- On les appelle aussi arènes.
- Ce sont des composés insaturés, car ils ont 3 doubles liaisons.
- Ils sont constitués d'au moins un cycle aromatique.
Exemples d'aromatiques
- Pétrole
- raffinage de pétrole
- Acétylène
Résumé des hydrocarbures
| Occupation | Formule générale |
Caractéristiques |
|---|---|---|
| hydrocarbure | Chaîne ouverte à maillons simples. |
|
| alcène | Chaîne ouverte avec double liaison. | |
| alcyne | Chaîne ouverte avec triple liaison. | |
| alcadiène | Chaîne ouverte avec deux doubles liaisons. | |
| Cyclanes | Chaîne fermée avec des connexions simples. | |
| Cycles | Chaîne fermée avec double liaison. | |
| cyclistes | Chaîne fermée à triple maillon. | |
| Aromatique | Variable | Chaîne fermée avec alternance de liaisons simples et doubles. |
Exercices sur les Hydrocarbures
1. (UEMA) Le GPL (Gaz de Pétrole Liquéfié), également connu sous le nom de gaz de cuisine, est un combustible fossile non renouvelable qui peut s'épuiser du jour au lendemain s'il n'est pas utilisé avec planification et sans excès. Il est composé, entre autres gaz, de propane C3H8, butane C4H10 et de petites quantités de propylène C3H6 et butène C4H8. Ces composés organiques sont classés comme des hydrocarbures qui présentent des similitudes et des différences entre eux. Sur la base du type de liaison entre les carbones et de la classification de la chaîne carbonée des composés ci-dessus, on peut affirmer que :
a) les composés insaturés sont le propane et le butane.
b) les composés insaturés sont le propène et le butène.
c) les composés insaturés sont le propène et le butane.
d) les composés ont des chaînes homocycliques.
e) les composés ont des chaînes hétérocycliques.
Alternative b) les composés insaturés sont le propène et le butène.
Un tort. Ces composés n'ont pas d'insaturations, leurs liaisons sont simples.
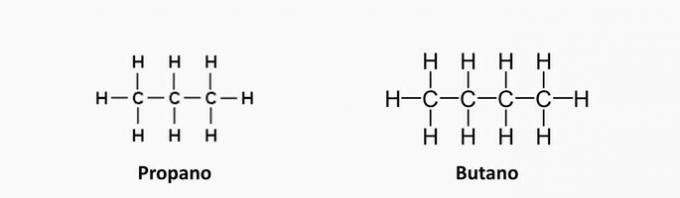
b) CORRECT. Le terme "en" indique la présence de doubles liaisons dans les composés.

c) FAUX. Le butane n'a pas d'insaturations.

d) FAUX. Ces chaînes sont fermées et les atomes de carbone sont liés par des liaisons simples.
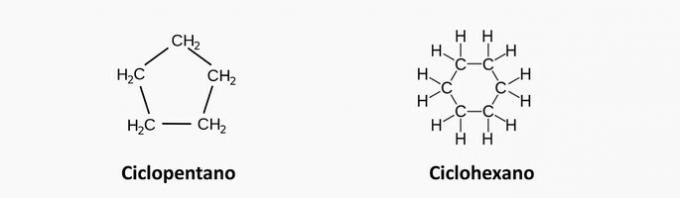
e) FAUX. Ces chaînes ont un hétéroatome, tel que l'oxygène et l'azote.

2. (Uel) Un des hydrocarbures de formule C5H12 peut avoir une chaîne carbonée :
a) cyclique saturé.
b) acyclique hétérogène.
c) cyclique ramifié.
d) ouvert non saturé.
e) ouvert ramifié.
Alternative e) ouvert ramifié.
Un tort. Un composé cyclique saturé correspond à un cyclane, dont la formule est CnonH2n.
Exemple:
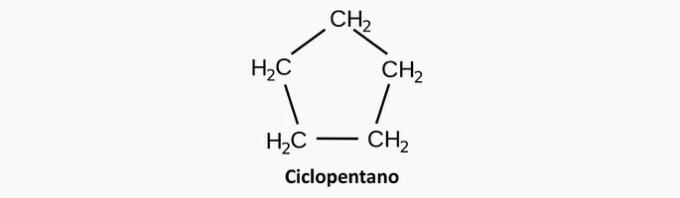
b) FAUX. Un composé acyclique hétérogène a la présence d'un autre élément en plus du carbone intercalé dans la chaîne.
Exemple:
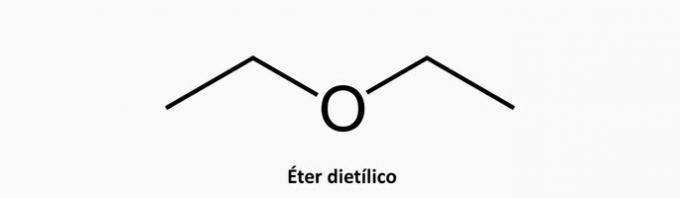
c) FAUX. Un composé cyclique ramifié a la formule CnonH2n.
Exemple:
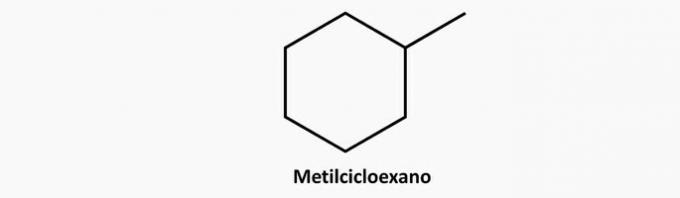
d) FAUX. Un composé insaturé à chaîne ouverte peut être un alcène ou un alcyne dont la formule est respectivement C.nonH2n et CnonH2n-2.
Exemples:
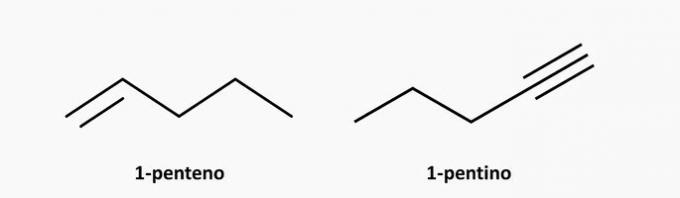
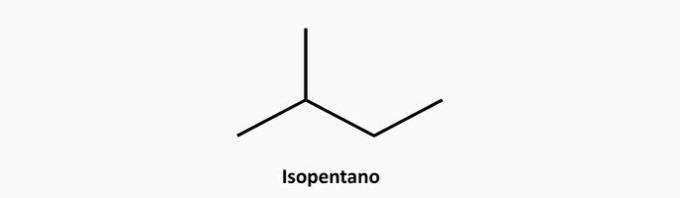
e) CORRECT. Un composé ramifié à chaîne ouverte est un alcane dont la formule est CnonH2n+2. Un composé de 5 carbones et 12 hydrogènes pourrait être l'isopentane.
Exemple:
3. (PUC) Les alcynes sont des hydrocarbures :
a) aliphatiques saturés.
b) les alicycliques saturés.
c) aliphatiques insaturés à double liaison.
d) les alicycliques insaturés à triple liaison.
e) aliphatiques insaturés à triple liaison.
Alternative e) aliphatiques insaturés à triple liaison.
Un tort. Les composés à chaîne ouverte et à liaison simple sont des alcanes.
Exemple:

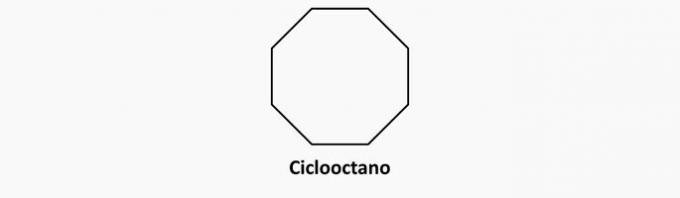
b) FAUX. Les composés cycliques avec des liaisons simples sont des cyclanes.
Exemple:
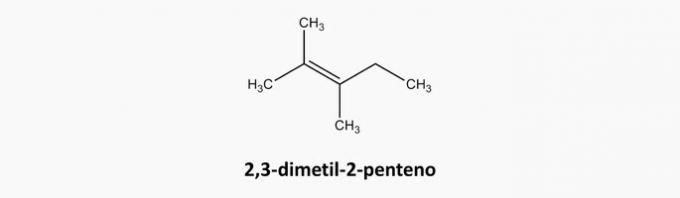
c) FAUX. Les composés à chaîne ouverte et à double liaison sont des alcènes.
Exemple:
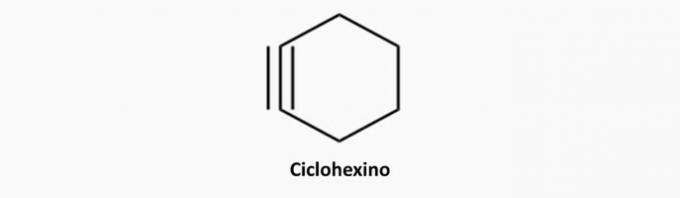
d) FAUX. Les composés cycliques et à triple liaison sont des cyclines.
Exemple:
e) CORRECT. Les alcynes sont des composés à chaîne ouverte et à triple liaison.

Vous souhaitez continuer à tester vos connaissances? N'oubliez pas de consulter ces listes :
- Exercices sur les Hydrocarbures
- Exercices sur la chimie organique
- Exercices sur les fonctions organiques


