Les substances simples sont constituées d'un seul élément chimique; lorsque vous avez deux ou plusieurs éléments dans la composition, les substances sont composées.
L'étude des réactions de décomposition chimique a été importante dans le développement de la chimie, car elles ont permis la classification des substances.
Les scientifiques ont noté que toutes les substances ne pouvaient pas être décomposées, ils ont donc utilisé cette observation pour déterminer si les substances pures étaient simples ou composites.
Pour eux, les substances composées se divisaient en substances nouvelles, tandis que les substances simples ne subissaient pas de décomposition.
Bien que ce concept ne soit plus accepté aujourd'hui, les recherches menées dans ce domaine étaient importantes pour l'avancement de la science.
substances simples
Les substances simples sont formées par juste un élément chimique, mais la façon dont atomes organiser pour les produire peut varier comme suit :
- Il y a des atomes qui restent isolés.
- Il existe des atomes qui se regroupent de différentes manières et peuvent former différentes substances.
Exemple:
| atome isolé | plus d'un atome | |
|---|---|---|
| il | O2 | O3 |
| Hélium représentant à la fois l'élément chimique et une molécule d'hélium. | L'union de deux atomes d'oxygène forme l'oxygène moléculaire et l'union de trois atomes forme la molécule d'ozone. |
Atomicité
Le nombre d'atomes dans une substance simple représente son atomicité. Il existe donc le classement suivant :
- Molécules monoatomiques: formé par un seul atome.
- Molécules diatomiques: formé de deux atomes.
- molécules triatomiques: formé de trois atomes.
Exemples de substances simples

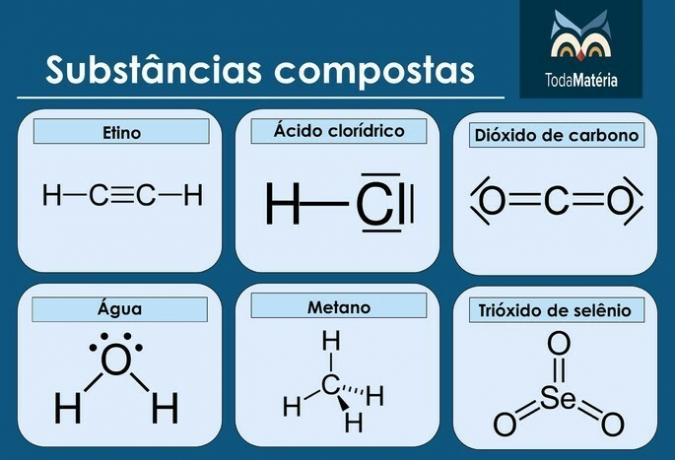
substances composées
Les substances composées sont également appelées composés chimiques, qui sont formés lors de réactions chimiques par des atomes ou des ions de différents éléments.
Exemple:
| Atomes | ions |
|---|---|
| Deux substances simples (N2 et H2) réagissent et forment une substance composée (NH3). | Un cation (Na+) et un anion (Cl-) réagissent et forment une substance composée (NaCl). |
Comme pour les substances simples, les composés chimiques peuvent être constitués d'atomes dans des proportions différentes.
C'est ce qui se passe avec l'eau (H2O) et le peroxyde d'hydrogène (H2O2). Les deux ne sont formés que d'hydrogène et d'oxygène, mais le nombre d'atomes dans les substances est différent et, par conséquent, rend ces composés différents.
En savoir plus sur: hydrogène et oxygène.
Exemples de substances composées
Exercices avec retours commentés
1. (Cesgranrio) Identifiez l'alternative qui présente, dans la séquence, les termes corrects qui comblent les lacunes de l'énoncé suivant :
"Une substance _____ est formée par _____, ne contenant que _____ du même _____ ."
a) composite; molécules; éléments; atome.
b) composites; molécules; atomes; élément.
c) la chimie; éléments; molécules; atome.
d) simple; atomes; molécules; élément.
C'est simple; molécules; atomes; élément.
Alternative correcte: e) simple; molécules; atomes; élément.
Un tort. Une substance composée est une molécule lorsque dans sa composition il y a des atomes d'éléments chimiques différents.
b) FAUX. Une substance composée est formée d'atomes d'éléments chimiques différents et non du même élément.
c) FAUX. Les molécules sont des groupes d'atomes d'éléments reliés par des liaisons covalentes.
d) FAUX. Les molécules sont formées par des atomes d'éléments chimiques.
e) CORRECT. "Une substance Facile est formé par molécules, ne contenant que atomes du même élément.”
1) L'air est un matériau homogène composé de substances simples.
2) Parmi les substances alcool, or, diamant et acétone, seul l'or est une substance simple.
3) En mesurant les températures de fusion et d'ébullition, il est possible de faire la distinction entre les substances simples et composites.
4) Les procédés de séparation des matériaux sont utilisés pour obtenir des substances simples à partir de substances composites.
1) FAUX. L'air est un mélange de gaz, mais tous ne sont pas de simples substances.
Les substances simples présentes dans l'air sont: l'azote, l'oxygène et les gaz rares. Cependant, il existe également de la vapeur d'eau et du dioxyde de carbone, qui sont des substances composites.
2) FAUX. L'alcool et l'acétone sont tous deux des substances composites, classées comme composés organiques. L'or et le diamant sont des substances simples.
L'alcool est un composé chimique dont la formule générale est R-OH. L'acétone est le nom commercial de la propanone, un composé de formule CH3(CO)CH3.
L'or représente l'élément chimique avec le symbole Au et est un métal de grande valeur que l'on trouve dans la nature sous forme de pépites. Le diamant est un cristal composé uniquement d'atomes de carbone.
3) FAUX. Les points de fusion et d'ébullition sont des propriétés physiques de la matière, utilisées pour distinguer un matériau d'une substance.
4) FAUX. Dans un processus de séparation, des substances simples et composites peuvent être obtenues.
Exemple:
La pyrolyse de l'eau produit deux substances simples: l'hydrogène et l'oxygène.
La photolyse du peroxyde d'hydrogène produit un composé et une substance simple: l'eau et l'oxygène.
Voir aussi: Fonctions organiques
3. (Mackenzie) Le nombre de substances simples parmi les substances de formule: O3, H2O, Na, P4, CH4, CO2 et Co est :
a) 2.
b) 3.
c) 4.
d) 5.
e) 7.
Alternative correcte: c) 4.
Au total, quatre substances simples apparaissent dans l'énoncé, tandis que les autres sont composées.
Substances simples :
- O3: Molécule d'ozone formée par des atomes de l'élément oxygène.
- Na: atome isolé de l'élément sodium.
- P4: Molécule de phosphore composée de quatre atomes de l'élément.
- Co: atome isolé de l'élément cobalt.
Substances composées :
- H2O: L'eau est composée d'atomes de deux éléments: l'hydrogène et l'oxygène.
- CH4: Le méthane est formé d'atomes de deux éléments: le carbone et l'hydrogène.
- CO2: Le dioxyde de carbone est formé d'atomes de deux éléments: le carbone et l'oxygène.
Voir aussi: Liaisons chimiques
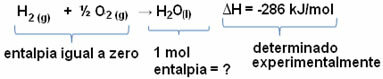
4. (UFPA) Considérant la réaction :
Parmi les réactifs et produits sont présents :
a) 2 substances simples et 2 composés.
b) 1 substance simple et 3 composés.
c) 3 substances simples et 1 composé.
d) 4 substances simples.
e) 4 substances composées.
Alternative correcte: a) 2 substances simples et 2 composés.
substances simples:
- C: atome isolé de l'élément carbone.
- H2: Molécule formée par des atomes de l'élément hydrogène.
substances composées:
- H2O: L'eau est composée d'atomes de deux éléments: l'hydrogène et l'oxygène.
- CO: Le monoxyde de carbone est formé par les atomes de deux éléments: le carbone et l'oxygène.
Voir aussi: Mélanges
5. (UFRGS) Le granit est constitué de quatre minéraux: le feldspath, la magnétite, le mica et le quartz. Si l'un de ces minéraux peut être séparé des autres, on peut dire que le granit est :
a) un élément
b) une substance simple
c) une substance composée
d) un composé ionique
e) un mélange
Alternative correcte: e) un mélange.
Un tort. Le granit est formé de composés chimiques appelés oxydes. Les oxydes ont différents éléments chimiques, tels que le silicium et l'aluminium, combinés à l'oxygène.
b) FAUX. Une substance simple est constituée d'atomes d'un seul élément. Le granit est formé de la combinaison d'éléments dans des proportions différentes.
c) FAUX. La composition du granit est variable et comporte plusieurs substances composites. Les plus courants sont: SiO2, Al2O3,K2sur un2O, CaO, FeO et Fe2O3.
d) FAUX. Les composés ioniques ont leurs atomes reliés par des liaisons ioniques. Les oxydes, une fonction inorganique présente dans le granite, sont des composés binaires formés par des liaisons covalentes, dans lesquelles les électrons sont partagés.
e) CORRECT. Le granit est un mélange de minéraux en forme de roche. Ses constituants sont :
- Feldspath: minéral composé de silicate d'aluminium qui contient différentes proportions de calcium, potassium et sodium. Sa formule chimique est: (K, Na, Ca) (Si, Al)4O8.
- Magnétite: minéral formé par les oxydes de fer II et de fer III: Sa formule chimique est: FeO.Fe2O3.
- Mica: minéral formé de silicates hydratés d'aluminium, de potassium, de sodium, de fer, de magnésium et de lithium. Un exemple de mica est: KAl2[Si3Bonjour10](OH, F2)).
- Quartz: minéral formé par le dioxyde de silicium. Sa formule chimique est: SiO2.
Vous pouvez également être intéressé par: Sujet: qu'est-ce que c'est, composition et exemples.