Les fonctions oxygénées sont l'un des 4 groupes fonctionnels des composés organiques. Les composés qui appartiennent à cette fonction sont formés par l'oxygène, à savoir les aldéhydes, les cétones, les acides carboxyliques, les esters, les éthers, les phénols et les alcools.
alcools
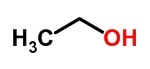
Toi alcools ils sont formés d'hydroxyles liés à des carbones qui n'effectuent que des liaisons simples.
Les alcools peuvent être primaires, secondaires ou tertiaires.
- Amorces lorsqu'il est attaché à un seul atome de carbone
- Secondaires lorsqu'il est lié à deux atomes de carbone
- tertiaire lorsqu'il est attaché à trois atomes de carbone.
Les principaux alcools sont l'éthanol, présent dans les boissons alcoolisées et les carburants, et le méthanol, qui est utilisé comme solvant.
Sa nomenclature suit l'IUPAC (Union Internationale de Chimie Pure et Appliquée, en portugais) :
- préfixe - nombre de carbones
- intermédiaire - type de liaison chimique
- suffixe - ol, d'alcool
esters

Toi esters sont très similaires aux acides carboxyliques. C'est parce que la seule différence entre eux est que les esters ont un radical carbone, tandis que les acides carboxyliques ont de l'hydrogène.
Ces composés organiques ne peuvent être dissous que dans l'alcool, l'éther et le chloroforme.
Les esters sont aromatisants, ce qui signifie qu'ils sont utilisés pour aromatiser des substances telles que les bonbons, les jus et les sirops.
Le nom des esters est formé comme suit :
- le préfixe indique le nombre de carbones
- l'intermédiaire indique le type de liaison chimique
- le suffixe -oato est ajouté, ainsi que l'élément "from"
- suit la fin -ila
Aldéhydes
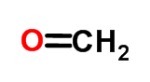
Toi aldéhydes ils sont constitués de composés organiques aliphatiques ou aromatiques. Ils ont une composition carbonyle (double CO), qui se situe aux extrémités de la structure moléculaire.
Comme aldéhydes présents dans la vie quotidienne, on peut citer les désinfectants, les médicaments, les plastifiants, les résines et les parfums.
Les principaux sont le méthanal (formaldéhyde), l'éthanal (acétaldéhyde), le propanal (propionaldéhyde), le butanal (butyraldéhyde), le pentanal (valéraldéhyde), le phényl-méthanal (benzaldéhyde) et la vanilline.
Selon l'IUPAC, -al est son suffixe utilisé pour nommer les composés. Ce suffixe indique la fonction organique des aldéhydes.
Cétones

À cétones ils sont composés de carbone en double liaison avec l'oxygène, le carbonyle, qui se trouve au milieu de la molécule.
Les cétones peuvent être symétriques (radicaux identiques) ou asymétriques (radicaux différents).
Ils sont classés selon le nombre de carbonyles: monocétones (1 carbonyle), polycétones (2 carbonyles ou plus).
Les cétones sont utilisées comme solvants, notamment pour enlever le vernis à ongles.
Selon l'IUPAC, -one est son suffixe, qui indique la fonction organique des cétones.
Phénols
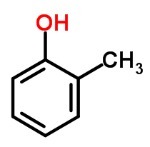
Toi phénols ils sont composés de carbone et d'hydrogène liés à des hydroxyles.
Ils se dissolvent dans l'alcool et l'éther et la plupart d'entre eux sont corrosifs et toxiques. Ils sont classés selon le nombre d'hydroxyles qu'ils présentent: monophénols (1 hydroxyle), diphénols (2 hydroxyles) et triphénols (3 hydroxyles).
Ils sont utilisés dans la fabrication d'explosifs, de bactéricides, de fongicides et de créoline.
éthers
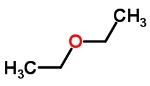
Toi éthers sont des composés très inflammables formés par oxygène entre deux chaînes carbonées. Ils peuvent être trouvés à l'état liquide, solide et gazeux et ont une odeur très forte.
Ils peuvent être symétriques (radicaux identiques) ou asymétriques (radicaux différents).
Les éthers sont utilisés comme solvants.
Le préfixe indique le nombre de carbones, tout comme le reste des composés. Cependant, le côté oxygène qui a le moins de suffixe de carbone est -oxy, tandis que le côté oxygène qui a le plus de suffixe de carbone est -year.
Acides carboxyliques
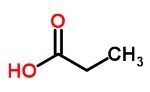
Acides faibles formés par le carboxyle, qui ont souvent une odeur désagréable.
Il est présent dans le vinaigre (acide éthanolique), dans la transpiration, dans les fruits (acide ascorbique).
Toi acides carboxyliques ils peuvent être aliphatiques, lorsque sa chaîne est ouverte, ou aromatiques, lorsqu'il existe un cycle aromatique.
Ils sont classés selon le nombre de carboxyles qu'ils possèdent: monocarboxylique (1 carboxyle), dicarboxylique (2 carboxyle) et tricarboxylique (3 carboxyle).
Selon l'IUPAC, -oic est son suffixe, qui indique la fonction organique des acides carboxyliques.
Lire aussi Fonctions organiques.
Exercices d'examen d'entrée avec rétroaction
1. (Mackenzie-SP) À propos de l'éthanol, dont la formule structurelle est H3C CH2 OH, identifiez la mauvaise alternative :
a) a une chaîne carbonée saturée.
b) est une base inorganique.
c) est soluble dans l'eau.
d) est un monoalcool.
e) présente une chaîne carbonée homogène.
Alternative b
2. (UFRN) Le composé qui est utilisé comme essence d'orange a une formule :
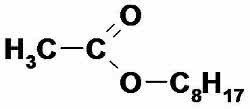
a) le butanoate de méthyle.
b) le butanoate d'éthyle.
c) l'éthanoate de n-octyle.
d) éthanoate de n-propyle.
e) l'hexanoate d'éthyle.
Alternative c
3. (UFU-MG) Le nom correct du composé ci-dessous, selon l'IUPAC, est :
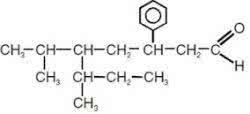
a) 3-phényl-5-isopropyl-6-méthyl-octanal
b) 3-phényl-5-sec-butyl-6-méthyl-heptanal
c) 3-phényl-5-isopropyl-6-méthyl-octanol
d) 2-phényl-4-isopropyl-5-méthyl-octanal
e) 4-isopropyl-2-phényl-5-méthyl-heptanal
Alternative à
4. (U. Católica de Salvador – BA) La cétone est un composé carbonylé avec 3 atomes de carbone et une chaîne saturée. Sa formule moléculaire est :
a) C3H6O
avant JC3H7O
c) C3H8O
d) C3H8O2
e) C3H8O3
Alternative à
5. (PUC-PR) À propos de l'acide 3-phényl propanoïque, il est correct d'affirmer que :
a) a la formule moléculaire C9H10O2.
b) a un atome de carbone quaternaire.
C) a 3 atomes d'hydrogène ionisables.
d) n'est pas un composé aromatique.
e) est un composé saturé.
Alternative à



