Substances sont des matériaux qui ont des propriétés constantes (densité, point de fusion, point d'ébullition, etc.). déjà le mélanges sont des matières qui ont des propriétés variables. Un moyen qui peut être utilisé pour les identifier est le graphique qui les représentent.
Les graphismes de mélanges et substances ont toujours la même composition, c'est-à-dire :
En abscisse, on a la présence de la variable temps ;
Sur l'axe des y, nous avons la présence de la température variable ;
Ils ont toujours cinq niveaux (droits);
Le premier plateau fait toujours référence à l'état physique solide ;
Le deuxième palier fait toujours référence au point de fusion, c'est-à-dire au passage de l'état solide à la liquide;
Le troisième plateau fait toujours référence à l'état physique liquide ;
La quatrième étape fait toujours référence au point de fusion, c'est-à-dire au passage d'un état liquide à un état gazeux ;
Le cinquième plateau fait toujours référence à l'état gazeux physique.

Composants d'un graphique sur les mélanges et les substances
Nous avons, en général, quatre graphiques utilisés pour représenter des substances et des mélanges, dont trois sont exclusifs aux mélanges.
→ Graphique d'une substance

Représentation graphique de toute substance
Le graphique d'une substance (simple ou composé) présente les paramètres suivants :
Les premier, troisième et cinquième niveaux sont toujours variables, ce qui peut être prouvé par le fait qu'ils sont toujours dans le diagonale par rapport aux axes x et y (temps et température), c'est-à-dire qu'au fil du temps, la température fait de même augmente;
Le deuxième plateau (point de fusion) est constant, ce qui peut être prouvé en analysant l'intervalle de temps de x à y. Dans cet intervalle, on a le niveau toujours horizontal (constant) par rapport à la température PF ;
Le quatrième plateau (point d'ébullition) est constant, ce qui peut être prouvé en analysant l'intervalle de temps de z à w. Dans cet intervalle, on a le niveau toujours horizontal (constant) par rapport à la température PE.
→ Graphique d'un mélange commun
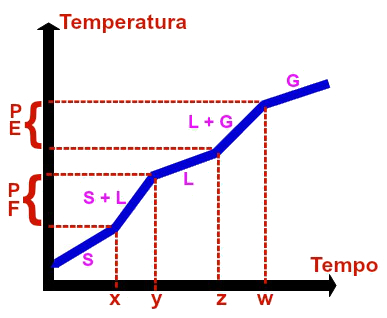
Représentation graphique de tout mélange commun
Un mélange commun est l'union de deux ou plusieurs substances dans le même récipient. Un exemple classique est le mélange entre l'eau et le sel. Le graphique d'un mélange commun a toujours les paramètres suivants :
Les premier, deuxième, troisième, quatrième et cinquième niveaux sont toujours variables, ce qui peut être prouvé par le fait qu'ils sont toujours en diagonale par rapport aux axes x et y (temps et température), c'est-à-dire que plus le temps passe, plus la température augmente.
→ Graphique d'un mélange eutectique
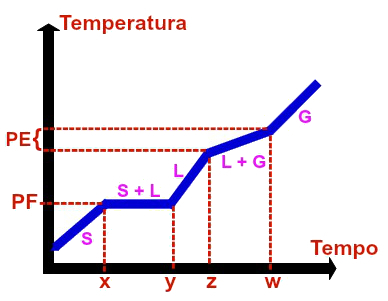
Représentation graphique de tout mélange eutectique
Le mélange eutectique est un mélange exclusivement homogène formé de matériaux à l'état solide en quantités bien précises. Le mélange homogène appelé soudure, par exemple, qui est composé de 67 % de plomb et de 33 % d'étain, est un mélange eutectique.
Le graphique d'un mélange azéotropique a toujours les paramètres suivants :
Les premier, troisième, quatrième et cinquième niveaux sont toujours variables, ce qui peut être prouvé par le fait qu'ils sont toujours en diagonale par rapport aux axes x et y (temps et température), c'est-à-dire qu'au fur et à mesure que le temps passe, la température fait de même augmente.
Le deuxième plateau (point de fusion) est constant, ce qui peut être prouvé en analysant l'intervalle de temps de x à y. Dans cet intervalle, on a le niveau toujours horizontal (constant) par rapport à la température PF.
→ Graphique d'un mélange azéotropique

Représentation graphique de tout mélange azéotropique
Le mélange azéotrope est un mélange exclusivement homogène et formé de matériaux à l'état liquide en quantités bien déterminées. Le mélange homogène formé de 95,5% d'eau et 4,5% d'éthanol, par exemple, est un mélange azéotropique.
Le graphique d'un mélange azéotropique a toujours les paramètres suivants :
Les premier, deuxième, troisième et cinquième niveaux sont toujours variables, ce qui peut être prouvé par le fait qu'ils sont toujours en diagonale par rapport aux axes x et y (temps et température), c'est-à-dire qu'au fur et à mesure que le temps passe, la température augmente également ;
Le quatrième plateau (point d'ébullition) est constant, ce qui peut être prouvé en analysant l'intervalle de temps de z à w. Dans cet intervalle, on a le niveau toujours horizontal (constant) par rapport à la température PE.
Par moi Diogo Lopes Dias
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/graficos-misturas-substancias.htm


