Les réactions de nitration sont des réactions de substitution qui se produisent par l'intermédiaire de l'acide nitrique (HNO3). Ce type de réaction se produit notamment avec les alcanes et avec le benzène et ses dérivés, où l'un des atomes d'hydrogène attaché à la chaîne ou au noyau aromatique est remplacé par le groupe NO2, donnant naissance à un composé nitré et à de l'eau.
Voir quelques exemples :
1. Nitration d'un alcane :
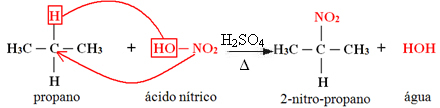
Lorsque l'alcane a plus de deux carbones, un mélange de différents composés substitués se forme. La quantité de chaque composé obtenu sera proportionnelle à l'ordre de facilité suivant avec lequel l'hydrogène est libéré dans la molécule :

Dans le cas ci-dessus, il n'y a pas de carbone tertiaire, il n'y a qu'un secondaire et deux primaires; ainsi, la plus grande quantité de composé formé en tant que produit sera le 2-nitro-propane.
S'il y a suffisamment d'acide nitrique, un autre hydrogène peut être remplacé par le groupe nitro, donnant naissance au 2-dinitropropane (structure ci-dessous), un composé largement utilisé comme additif au gazole, augmentant son indice d'octane et diminuant les émissions de suie.
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
AU2
│
H3C─C─CH3
│
AU2
2. Nitratation du benzène :
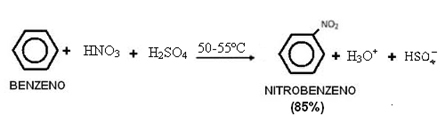
A noter que cette réaction se produit en présence de chaleur, car le benzène est chauffé avec un mélange sulfonhydrique, c'est-à-dire de l'acide nitrique concentré avec de l'acide sulfurique concentré. L'acide sulfurique est un catalyseur, provoquant une augmentation de la vitesse de réaction lorsque le benzène réagit lentement avec l'acide nitrique.
3. Nitratation des dérivés benzéniques:
Dans de tels cas, le lieu de substitution dépendra du groupe substituant ou du groupe fonctionnel attaché au noyau aromatique. Les textes "Radicaux de direction dans l'anneau de benzène" et "Effets électroniques des radicaux méta et ortho-directeurs” expliquez plus sur la façon dont cela se produit.
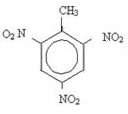
Les anneaux aromatiques peuvent subir une nitration et donner naissance à des explosifs. Un exemple est le trinitrotoluène (2-méthyl-1,3,5-trinitrobenzène), mieux connu sous le nom de TNT et il existe plusieurs pigments utilisés principalement dans les tissus.
Par Jennifer Fogaça
Diplômé en Chimie
Souhaitez-vous référencer ce texte dans un travail scolaire ou académique? Voir:
FOGAÇA, Jennifer Rocha Vargas. « Réactions de nitration organique »; École du Brésil. Disponible en: https://brasilescola.uol.com.br/quimica/reacoes-organicas-nitracao.htm. Consulté le 28 juin 2021.