En 1874, le chimiste hollandais Jacobus Henrique van't Hoff (1852-1911) et le chimiste français Joseph Achille le Bel (1847-1930), à travers des théories mathématiques, a suggéré indépendamment l'existence de carbones asymétrique.
À l'époque, ils ont été fortement critiqués, notamment van't Hoff, par le célèbre chimiste allemand Adolph Wilhelm Kolbe (1818-1884). Or, Kolbe se trompait, on sait aujourd'hui qu'il existe un carbone asymétrique, à tel point qu'en 1901, van't Hoff fut le premier chimiste à recevoir le prix Nobel.
van't Hoff (à gauche) et Kolbe (à droite)
Une des conditions nécessaires pour que la molécule ait une activité optique est qu'elle soit asymétrique. Aussi, une façon de vérifier s'il est asymétrique est d'étudier sa structure en détail pour voir s'il a au moins un carbone asymétrique.
Qu'est-ce qu'une molécule asymétrique et un carbone asymétrique?
Quelque chose de symétrique est quelque chose qui a au moins un plan de symétrie. Par exemple, si nous coupons une raquette de tennis en deux, les deux parties résultantes seront exactement les mêmes. De plus, si nous les plaçons devant un miroir plat, ils produiront une image identique.
Les structures qui ne supportent pas un plan de symétrie sont appelées asymétrique. Un exemple est notre main, car si nous la plaçons devant un miroir, elle produira une image différente d'elle-même. Si on met la main droite, l'image sera la main gauche et vice versa. Un autre point important est qu'ils ne se chevauchent pas.
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
C'est pourquoi le carbone asymétrique est aussi appelé carbone chiral, d'où vient ce mot khéir qui signifie en grec main.
Un exemple de molécule asymétrique est la thalidomide, dont la structure est illustrée ci-dessous :

Le point repéré par un astérisque (*) correspond à un carbone asymétrique, car il il a quatre liaisons covalentes qui sont faites avec différents atomes ou groupes d'atomes.
Ci-dessous, un carbone avec quatre ligands différents devant un miroir. Notez que l'image ne peut pas être superposée sur la structure d'origine :

Les deux molécules obtenues ci-dessus sont isomères optiques ou alors énantiomères.
Revenant au cas de la thalidomide, du fait qu'elle a du carbone asymétrique, le résultat est que la molécule commence à avoir une image non superposable, qui correspond à une autre substance. Nous avons donc deux isomères de la thalidomide aux propriétés extrêmement différentes.
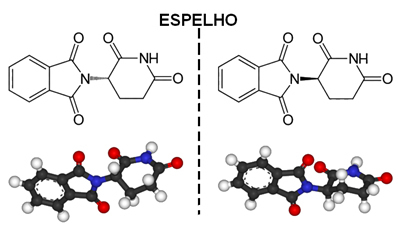
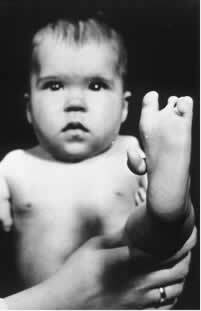
L'un de ces isomères (R) a des propriétés sédatives. Par conséquent, à la fin des années 1950, il a commencé à être utilisé comme tranquillisant et aide au sommeil pour les femmes enceintes. Cela a déclenché une tragédie, car ses énantiomères (S) ont également été mélangés au médicament. Cet isomère, à son tour, est tératogène et a conduit de nombreuses femmes enceintes à avoir leurs bébés avec des mains, des jambes, des bras et des pieds atrophiés.
Par Jennifer Fogaça
Diplômé en Chimie
Souhaitez-vous référencer ce texte dans un travail scolaire ou académique? Voir:
FOGAÇA, Jennifer Rocha Vargas. « Carbone asymétrique ou chiral »; École du Brésil. Disponible en: https://brasilescola.uol.com.br/quimica/carbono-assimetrico-ou-quiral.htm. Consulté le 27 juin 2021.
