Certains métaux ne se trouvent pas libres dans la nature et doivent être obtenus par des procédures de laboratoire. L'électrolyse est l'une des méthodes efficaces et économiques de purification des métaux. L'électrolyse a lieu dans des cellules électrolytiques, avec deux électrodes connectées aux bornes d'un générateur de courant continu.
On sait que dans une cellule électrolytique il y a une cathode et une anode, voir la définition pour chacune:
Cathode: C'est l'électrode négative qui attire les cations, et c'est là que se produit la réduction des cations.
anode: L'électrode positive qui attire les anions et, par conséquent, c'est là que l'anion s'oxyde.
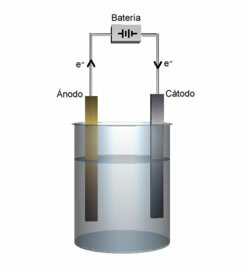
Démonstration anode et cathode.
Purification du cuivre
Le cuivre que l'on trouve dans la nature contient des impuretés telles que l'argent, le fer, l'or, le zinc. Grâce à l'électrolyse, il est possible d'isoler ce métal en l'obtenant sous forme pure, suivez le processus:
- Le cuivre impur fonctionne comme une anode et une solution aqueuse de sulfate de cuivre fonctionne comme un électrolyte, qui se trouve à l'intérieur de la cellule électrolytique. La cathode de la cellule est en Cuivre lui-même à un haut degré de pureté.
- Le cuivre est transféré de l'anode à la cathode tandis que les impuretés restent en solution. Le cuivre à l'état pur s'accumule à la cathode et peut donc être utilisé.
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
Par Líria Alves
Diplômé en Chimie
Équipe scolaire du Brésil
Voir plus!
Réactions d'électrolyse
Produits d'électrolyse
Électrolyse - Physico-chimique - Chimie - École du Brésil
Souhaitez-vous référencer ce texte dans un travail scolaire ou académique? Voir:
SOUZA, Líria Alves de. « Purification des métaux par électrolyse »; École du Brésil. Disponible en: https://brasilescola.uol.com.br/quimica/purificacao-metais-atraves-eletrolise.htm. Consulté le 28 juin 2021.


