Radioactivité est la propriété que certains atomes, comme uranium et radio, doivent émettre spontanément énergie en forme de particules et vague, devenir éléments chimiques plus stable et plus léger.
Les types
La radioactivité se présente avec deux façons rayonnements différents: particule — alpha (α) et bêta (β); et onde électromagnétique — rayons gamma (γ).
rayons alpha: ce sont des particules positives composées de deux protons et de deux neutrons et à faible pouvoir de pénétration.
rayons bêta: sont des particules négatives qui ne contiennent pas de masse constituée d'un électron (masse négligeable), et leur pouvoir de pénétration est supérieur à celui des rayons alpha, mais inférieur à celui des rayons gamma.
Gamma: ce sont des ondes électromagnétiques de haute énergie et, comme ce ne sont pas des particules, elles n'ont pas non plus de masse.
Lire aussi: Formules de radioactivité
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
lois
L'émission radioactive de particules suit certains comportements qui s'expliquent par les lois de radioactivité (une pour la particule alpha et une pour la particule bêta), qui ont été décrites par le chimiste Anglais
Frederick Soddyet par le chimiste et physicien polonais Kazimierz Fajans.Première loi de la radioactivité
Selon cette loi, lorsqu'un atome radioactif émet un rayonnement de type alpha, il donnera naissance à un nouvel atome avec noyau contenant deux protons et deux neutrons moins, totalisant une masse quatre unités plus petites. On peut représenter la première loi de la radioactivité avec l'équation générique suivante :
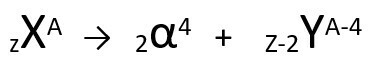
Équation générique de la première loi de la radioactivité.
Regardons un exemple :
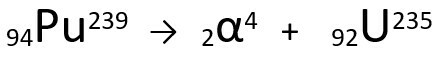
Équation représentant l'émission de particules par le Plutonium-239.
Notez que, lors de l'émission d'un rayonnement alpha, l'atome nouvellement formé, Uranium-235, a un nombre de masse quatre unités plus petit et le numéro atomique deux unités plus petit — exactement les valeurs correspondant à la particule α émise par le noyau du plutonium. Pour en savoir plus, rendez-vous sur: Première loi de la radioactivité ou première loi de Soddy.
Deuxième loi de la radioactivité
La deuxième loi parle de la problème bêta. Lorsqu'un atome émet une particule bêta, constituée d'un électron et de masse négligeable, son masse atomique restes inchangé c'est le tien le numéro atomique augmente d'une unité. Génériquement, nous représentons comme suit :
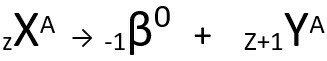
Équation générique de la deuxième loi de la radioactivité.
Voir l'exemple :
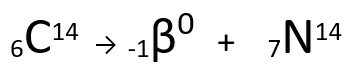
Équation représentant l'émission de particules par le carbone-14.
On peut voir que l'atome d'azote formé a la même masse que l'atome C-14, c'est-à-dire qu'ils sont isobares, et son numéro atomique augmente d'une unité. L'augmentation de numéro atomiquea été expliqué par le scientifique Henrico Fermi, qui a proposé que l'un des neutrons du noyau subit une transmutation, selon l'équation suivante, générant uneélectron(la particule bêta émise), une neutrinos(une particule subatomique sans charge électrique et sans masse, ) et une proton(P).
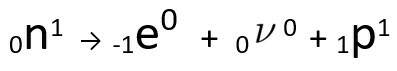
Équation représentant la transmutation neutronique, selon l'hypothèse de Fermi.
O électron C'est le neutrinos sont délivrés à hors du noyau, restant seul le proton, ce qui explique l'augmentation du numéro atomique Pour en savoir plus, rendez-vous sur: Deuxième loi de la radioactivité ou deuxième loi de Soddy.
A lire aussi: Différence entre contamination radioactive et irradiation
applications
malgré la vue négative ce dépôt sur la radioactivité, il a applications importantes dans notre vie quotidienne, par exemple, dans le production de électricitédans centrales nucléaires à travers fissiond'atomes radioactifs.
Actuellement, le Brésil n'utilise pas le énergie nucléaire comme sa principale source d'énergie, mais il dispose de centrales nucléaires (Angra 1 et 2) fonctionnant pour fournir de l'électricité au pays. On peut aussi citer le datation matérielle trouvé par les archéologues à l'aide carbone-14.

Centrale nucléaire de Rio de Janeiro, Brésil
Un autre rôle fondamental de la radioactivité est lié au domaine de la médecine, comme dans les examens de rayon Xet dans le tomodensitogrammes, et aussi dans certains types de traitement du cancer.
Lire aussi: Principaux risques de la production d'électricité nucléaire pour l'environnement
radioactivité naturelle
quotidiennement nous sommes exposé le petites quantités de rayonnement, qu'il soit artificiel ou naturel. La radioactivité naturelle se produit spontanément dans la nature. Une partie de ce rayonnement que nous recevons provient des aliments consommés quotidiennement, comme le Radon-226 et le Potassium-40, qui sont présentés dans niveaux très bas et ils ne font pas courir de risques à notre santé et ne nuisent pas aux valeurs nutritionnelles des aliments.
Ce processus d'exposition des aliments à des émissions radioactives vise à conserver les aliments et promouvoir une croissance des plantes. Voici quelques exemples d'aliments qui émettent des rayonnements: Noix du Brésil, banane, haricots, viande rouge, entre autres.
Découverte
L'étude de la radioactivité a commencé avec les recherches du physicien allemand Wilhelm Röentgen, en 1895, alors qu'il enquêtait sur effet deluminescence. Un autre scientifique important pour le développement de la radioactivité était le physicien français Antoine-Henri Becquerel, qui remarqua, en 1896, des marques faites sur une pellicule photographique par un échantillon de sel d'uranium.
Cependant, c'était le Curieux couple qui a utilisé le terme radioactivité pour la première fois. Dans 1898, Le polonais Marie Curie poursuivi les études sur la radioactivité et fait des découvertes précieuses pour la région, comme la découverte de deux nouveaux éléments radioactifs: le polonium (Po) et le radium (Ra).
Postérieurement, Ernest Rutherford découvert le rayonnement de type alpha (α) et bêta (β), ce qui a permis de mieux expliquer son modèle atomique, ainsi que l'avancée des recherches liées à la radioactivité.
A lire aussi :Marie Curie: biographie, contributions et héritage
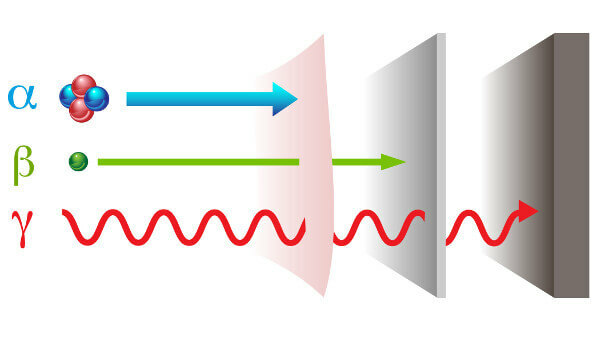
Types de rayonnement et leurs pouvoirs de pénétration.
pourriture
O désintégration radioactive (ou transmutation) est la Processus naturel où une noyau instable émet un rayonnement, successivement, afin de baisse ton énergie et devenir stable.
Cela se produit normalement avec des atomes de numéro atomique. supérieur à 84, qui sont des atomes avec grande instabilité nucléaire en raison de la quantité de charge positive (protons) accumulée dans le noyau. Dans ce processus, le les neutrons ne suffisent pas pour stabiliser tous les protons regroupés dans le noyau, puis le noyau commence à subir une désintégration radioactive jusqu'à ce que son numéro atomique soit inférieur à 84.
Dans certains cas, il peut arriver que des atomes de numéro atomique inférieur à 84 aient des noyaux instables et aussi passer par le processus de désintégration, mais pour cela, ils doivent avoir un nombre de protons bien supérieur au nombre de neutrons.
La désintégration radioactive est calculé par demi-vie (ou période de semi-désintégration, P) du radio-isotope, qui est le temps nécessaire à la moitié de la masse de l'échantillon radioactif initial pour se désintégrer, c'est-à-dire se stabiliser. Graphiquement parlant, le concept de demi-vie est représenté ci-dessous. Parce que c'est un processus continu, la courbe tend à atteindre zéro.
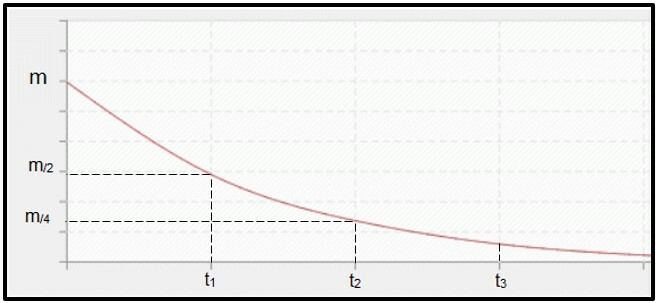
Graphique représentant le temps de demi-vie.
Les calculs impliquant la décroissance radioactive suivent les formules suivantes :
Formule de calcul de la masse restante après la demi-vie:
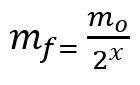
mF – masse finale
mO – masse initiale
x – nombre de demi-vies écoulées
Formule de calcul du temps de désintégration d'un échantillon radioactif :
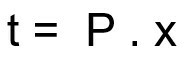
t – temps de désintégration
P - période de demi-vie
x – nombre de demi-vies écoulées
éléments radioactifs
Il existe deux types de éléments radioactifs: toi Naturel et le artificiel. Les naturels ont des éléments trouvés dans la nature, déjà avec leurs noyaux instables, tels que le uranium, ô actinium C'est le radio. Les artificiels sont produits par des processus qui déstabilisent le noyau d'un atome. Dans ce cas, on peut citer le astate C'est le francium.
Les principaux éléments radioactifs sont: l'uranium-235, le cobalt-60, le strontium-90, le radium-224 et l'iode-131. En raison de sa large utilisation dans les centrales nucléaires et les traitements contre le cancer, ces éléments ont tendance à apparaître plus fréquemment dans notre vie quotidienne. Pour en savoir plus sur ce sujet, rendez-vous sur: éléments radioactifs.
Déchets radioactifs
Déchets radioactifs ou déchets nucléaires C'est le résidu du les industries qui utilisent des matières radioactives dans leurs procédés qui n'ont plus d'application pratique. Ces déchets proviennent principalement du centrales nucléaires c'est de applications médicales.
L'importante production de déchets radioactifs a été un problème environnemental pour le monde entier, en raison de la rareté et de l'insuffisance conditions d'élimination et stockage.
Ces résidus sont associés à la contamination du sol, des cours d'eau et de l'air, ce qui destruction de l'environnement progressivement. En outre, ils présentent également des risques pour la santé humaine, tels que infections, cancer et, dans les cas plus graves de contamination, ils peuvent conduire à décès.
exercices résolus
(PUC-Camp-SP) La bombe atomique, également appelée bombe nucléaire, a des atomes d'uranium-235 comme constituant fissile, , émetteurs de particules alpha
, émetteurs de particules alpha 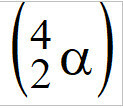 . Chaque atome d'U-235, lorsqu'il émet une particule alpha, se transforme en un autre élément, dont le numéro atomique est égal à
. Chaque atome d'U-235, lorsqu'il émet une particule alpha, se transforme en un autre élément, dont le numéro atomique est égal à
a) 231.
b) 233.
c) 234.
d) 88.
e) 90.
Modèle: Lorsqu'un atome émet une particule alpha, il y a une diminution de deux unités du numéro atomique, selon la première loi de la radioactivité. Donc: 92-2 = 90. Lettre e.
(PUC-Camp-SP) L'iode 125, une variété radioactive d'iode ayant des applications médicinales, a une demi-vie de 60 jours. Combien de grammes d'iode 125 restera-t-il après six mois, sur la base d'un échantillon contenant 2,00 g du radio-isotope ?
a) 1,50
b) 0,75
c) 0,66
d) 0,25
e) 0,10
Modèle: Tout d'abord, le nombre de demi-vies écoulées au cours des 180 jours est calculé :
t = P. X
180 = 60. X
x = 3
Une fois le nombre de demi-vies écoulées trouvé, la masse qui restera à la fin des 180 jours est calculée :
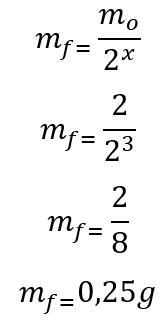
Par conséquent, 0,25 g du radio-isotope de l'iode 135 restera à la fin des six mois. Lettre D.
Par Victor Félix
Diplômé en Chimie