Avant de parler de la nomenclature d'un sel d'ammonium quaternaire correctement, il est important de se rappeler ce qu'est ce composé organique. Le sel d'ammonium quaternaire provient du remplacement des hydrogènes présents dans le cation ammonium (NH4+) par radicaux organique, comme indiqué ci-dessous:
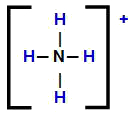
Formule structurelle du cation ammonium
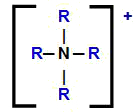
Formule développée du cation ammonium avec ses hydrogènes remplacés par des radicaux organiques
En plus de remplacer les hydrogènes, chaque sel d'ammonium quaternaire contient un anion qui accompagne le cation dérivé de l'ammonium. Ainsi, nous pouvons représenter la formule structurale générale de ce composé comme suit :
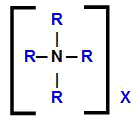
Formule développée générale d'un sel d'ammonium quaternaire
Ainsi, il est évident que, dans la formule d'un sel d'ammonium quaternaire, nous avons la présence de quatre radicaux organiques, identiques ou différents, et de tout anion (X). Pour effectuer la nomenclature de ces composés, nous devons tenir compte de ce fait.
Voyez comment le
nomenclature d'un sel d'ammonium quaternaire selon IUPAC (International Union of Pure and Applied Chemistry):Nom de l'anion + de + nom des radicaux par ordre alphabétique + ammonium
Suivez maintenant quelques exemples d'application de la règle de nomenclature des sels d'ammonium quaternaire :
Iodure de benzyl-octadécyl-diméthylammonium
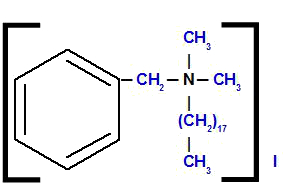
En analysant la structure, nous observons que la anion présent dans le composé est le je, qui est appelée iodure. A gauche de la structure, nous avons le radical benzyle (jonction du benzène avec le groupe CH2). En haut et à droite, nous avons deux radicaux méthyle (CH3), qui sera appelé « diméthyle ». En bas, on a le radical octadécyle, qui a dix-huit atomes de carbone dans sa chaîne.
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
Ainsi, le nom commence par iodure, suivi de la préposition de, plus le nom benzyle, suivi par octadécyle (à cause de l'ordre alphabétique) et, enfin, diméthyle avec ammonium.
Observation: Les termes oct et di ne participent pas à l'organisation séquentielle alphabétique du nom composé.
chlorure de tétraéthylammonium
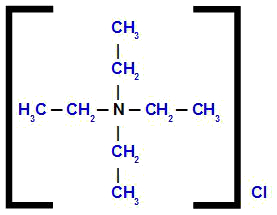
En analysant la structure, nous observons que la anion présent dans le composé est le Cl, qui est appelée chlorure. Les quatre radicaux organiques présents dans la structure sont éthyle (CH3-CH2-); par conséquent, ils reçoivent le nom de tétraéthyle.
Ainsi, le nom commence par chlorure, suivi de la préposition de, plus le nom tétraéthyle, suivi du terme ammonium.
Bromure de benzyl-tridécyl-diméthylammonium

En analysant la structure, nous observons que la anion présent dans le composé est le fr, qui est appelée bromure. A gauche de la structure, nous avons le radical benzyle (jonction du benzène avec le groupe CH2). En haut et à droite, nous avons deux radicaux méthyle (CH3), qui sera appelé « diméthyle ». En bas, on a le radical tridécile, car il y a treize atomes de carbone dans sa chaîne.
Ainsi, le nom commence par iodure, suivi de la préposition de, plus le nom benzyle, suivi par tridécyle (à cause de l'ordre alphabétique) et, enfin, diméthyle avec ammonium.
Sulfate de diphényl-diméthylammonium
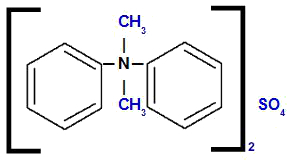
En analysant la structure, nous observons que la anion présent dans le composé est le SEUL4, qui est appelée sulfate. A gauche et à droite de la structure, nous avons le radical phényle (benzène), que l'on appellera « diphényle ». En haut et en bas, nous avons radicaux méthyle (CH3), qui sera appelé « diméthyle ».
Ainsi, le nom commence par sulfate, suivi de la préposition de, plus le nom diphényle, suivi de diméthyle (à cause de l'ordre alphabétique) et, enfin, d'ammonium.
Par moi Diogo Lopes Dias