L'étude de la force d'un acide est très important pour déterminer la capacité de la solution acide à conduire le courant électrique, en ce qui concerne la quantité d'ions que cette substance produit lorsqu'elle est en contact avec l'eau (ionisation). Lorsqu'un acide est trop fort, il produit trop de cations hydronium (H3O+) et de nombreux anions (X-). Voir l'équation d'ionisation de l'acide bromhydrique :
HBr + H2O → H3O+ + Br-
Lors de l'ionisation, l'hydrogène présent dans la molécule d'acide interagit avec la molécule d'eau et forme de l'hydronium. Mais pour que cet événement se produise, l'atome d'hydrogène doit nécessairement être ionisable. L'hydrogène ionisable est celui capable de former un cation hydronium.. Pour savoir si un hydrogène est ionisable, nous prenons en compte la classification de l'acide comme hydracide (n'a pas d'oxygène dans sa composition) ou oxyacide (a de l'oxygène dans sa composition).
a) Hidracides
Tout l'hydrogène dans un hydracide est considéré comme ionisable.
Exemples:
- HCl: Un hydrogène ionisable, produisant ainsi un hydronium ;
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
-H2S: Deux hydrogènes ionisables, puis produisent deux hydrons
b) Oxyacide
Dans un oxyacide, seul l'hydrogène lié à un atome d'oxygène dans la molécule est considéré comme ionisable. Pour cela, il est nécessaire de construire sa formule structurelle. Voir quelques exemples :
H3POUSSIÈRE4 (acide phosphorique)
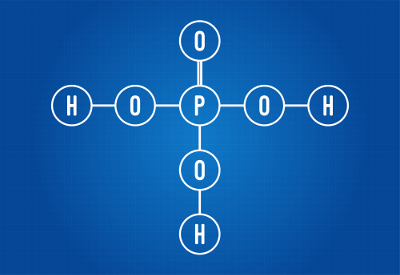
Formule développée de l'acide phosphorique
On peut voir que, dans la structure de l'acide phosphorique, il y a trois hydrogènes liés à l'oxygène, donc il y a trois hydrogènes ionisables. L'équation d'ionisation sera :
H3POUSSIÈRE4 + 3H2O → 3 H3O+ + Bon de commande4-3
H2SEUL4 (acide sulfurique)
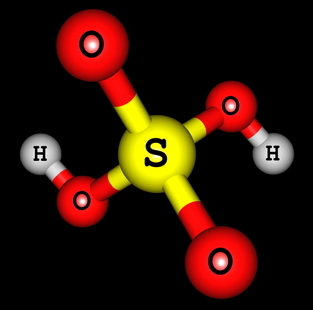
Formule développée de l'acide sulfurique
On peut voir que, dans la structure de l'acide sulfurique, il y a deux hydrogènes liés à l'oxygène, donc il y a deux hydrogènes ionisables. L'équation d'ionisation sera :
H2SEUL4 + 2H2O → 2H3O+ + système d'exploitation4-2
Par moi Diogo Lopes Dias
Souhaitez-vous référencer ce texte dans un travail scolaire ou académique? Voir:
JOURS, Diogo Lopes. « Hydrogènes ionisables »; École du Brésil. Disponible en: https://brasilescola.uol.com.br/quimica/hidrogenios-ionizaveis.htm. Consulté le 28 juin 2021.
Chimie

Dissociation et ionisation, scientifique italien Volta, courant électrique, physico-chimiste suédois Svant August Arrhenius, théorie de Arrhenius, ions positifs, cations, ions négatifs, anions, soude caustique, sel de table, molécules polaires, dissociation ionique,
