Série (ou famille) de désintégration radioactive naturelle c'est l'ensemble des éléments à noyau instable, qui suivent une séquence ordonnée de désintégrations spontanées, c'est-à-dire qu'ils émettent des particules alpha et bêta, jusqu'à la formation d'un noyau plomb stable.
Cela signifie que tous les isotopes radioactifs naturels qui se désintègrent spontanément dans la nature proviennent de trois éléments radioactifs, qui sont: thorium 232 (90232Th), uranium 238 (92238U), l'uranium 235 (92235U). La série de l'uranium 235 est appelée série d'actine, car autrefois on croyait que le premier élément de cette famille était l'actinium.
Chacun de ces éléments émet une particule alpha (24α), se transformant en un autre élément radioactif, qui émet alors également une particule alpha (24α) ou bêta (-10β), donnant naissance à un autre élément radioactif; et ainsi de suite, jusqu'à ce que la série se termine par un isotope stable de l'élément plomb (Pb).
Le premier élément de chaque série radioactive est appelé
core-parent ou alors élément parent; étant que le noyaux d'enfants ou alors éléments enfants ce sont tous les éléments qui ont été créés par le noyau parent.Voir la série complète du thorium ci-dessous :
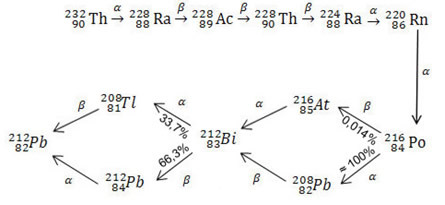
Les séries de l'uranium et de l'acticnium sont encore plus longues que celles du thorium. Le plus important d'entre eux est l'uranium 235, ou actinium, car l'uranium 235 est l'un des principaux isotopes utilisés comme combustible dans les centrales nucléaires et dans la fabrication d'armes atomiques.
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
Il est possible de déterminer à quelle série ou famille radioactive un certain isotope radioactif appartient en suivant une règle simple: on divise le nombre de masse (A) de l'élément par quatre; et, d'après le résultat, on détermine la série de l'élément. Notez comment cela se passe ci-dessous :
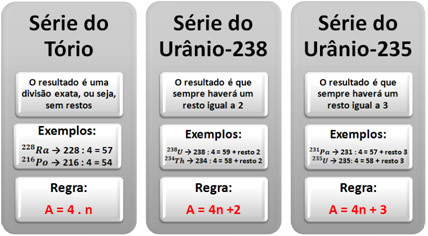
Ci-dessous, nous avons le pourcentage d'abondance dans la nature des trois éléments mentionnés qui donnent lieu à chaque série :
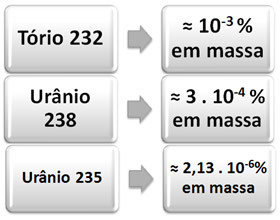
Les éléments de chaque série sont en équilibre radioactif, ce qu'on appelle équilibre séculaire. Cela signifie que lorsqu'un élément se désagrège, en formant un autre, ce deuxième élément a également sa quantité. diminué par sa propre désintégration, résultant en une quantité égale à la quantité d'isotopes naturels pendant une longue période temps.
Cependant, comme les éléments parents ne sont pas remplacés, il faut s'attendre à ce qu'ils s'épuisent un jour, ainsi que tous les autres éléments radioactifs de la série, ne laissant que le plomb stable.
Par Jennifer Fogaça
Diplômé en Chimie
Souhaitez-vous référencer ce texte dans un travail scolaire ou académique? Voir:
FOGAÇA, Jennifer Rocha Vargas. « Série radioactive »; École du Brésil. Disponible en: https://brasilescola.uol.com.br/quimica/series-radioativas.htm. Consulté le 27 juin 2021.