Yksi palautuva reaktio se tapahtuu, kun on mahdollista muuttaa tuotteet takaisin reagoiviksi aineiksi. Tällainen reaktio tulee kemiallinen tasapaino kun suoran reaktion, ts. reaktion, reagenssien kulutuksen ja reaktioiden muodostumisen nopeus tuotteet tapahtuvat samalla nopeudella kuin käänteinen reaktio - reaktanttien muodostuminen ja tuotteiden kulutus.
Tämäntyyppisiä tasapainoisia reaktioita nähdään paljon jokapäiväisessä elämässä. Esimerkki on se, mitä tapahtuu luolissa, ns. Stalaktiittien ja stalagmiittien muodostumisessa.
Pohjaveteen kohdistuu suuria paineita, joten se sisältää suuria määriä hiilidioksidia (CO2 g)) liuotettu siihen. Kun kulkee kalkkikiveä (CaCO3 (s)), tämä karbonaatti liukenee ja muodostuu luolia alla olevan reaktion mukaisesti:
CaCO3 (s) + CO2 g) + H2O(1) → Ca2+(tässä) + 2 HCO-3 (aq)
Karbonaatti- ja kalsiumionit voivat kuitenkin reagoida saostuen uudelleen kalsiumkarbonaattina. Tämän osoittaa reaktio:
Tässä2+(tässä) + 2 HCO-3 (aq)→ CaCO3 (s) + CO2 g) + H2O(1)
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Kuten olet ehkä huomannut, yksi reaktio on päinvastainen toiselle: reagoivista aineista tulee tuotteita ja tuotteista reagoivia. Joten voimme edustaa tätä reaktiota tasapainossa seuraavasti:
CaCO3 (s) + CO2 (aq) + H2O(1) Tässä2+(tässä) + 2 HCO-3 (aq)
Tässä2+(tässä) + 2 HCO-3 (aq)
Luolien katon mineralisoituneista pisaroista muodostuva hidas ja jatkuva karbonaatin poistuminen valuu alas, niiden vesi haihtuu ja vapautuu CO2. Niin, että kemiallinen tasapaino siirtyy vastakkaiseen suuntaan (reaktanttien muodostuminen), siis CaCO3 (s) muodostuu, eli tippukivipuikot luolien katolla. Putoamisen aikana pisara on vielä liuottanut luolan lattialle kerrostuneen karbonaatin muodostaen stalagmitit.
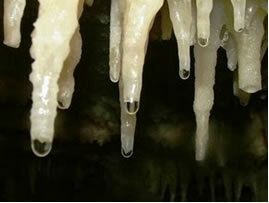
Vesi, josta tippuu tippukiveä kalkkikivestä muodostamaan tippukivipylväitä
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Kemiallinen tasapaino luolissa"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/equilibrio-quimico-nas-cavernas.htm. Pääsy 28. kesäkuuta 2021.