Yleensä reaktiot vesipitoinen elektrolyysi ja magma-elektrolyysi ne suoritetaan grafiitti- ja platinaelektrodeilla, jotka eivät osallistu reaktioon; ne johtavat vain sähkövirtaa. On kuitenkin joitain erityistapauksia, joissa se on tarpeen käyttää aktiiviset elektrodit, toisin sanoen, jotka läpikäyvät pelkistyksen ja hapettumisen.
Näiden redox-prosessiin osallistuvien elektrodien pääasialliset käyttötapaukset ovat: a elektrolyyttinen metallin puhdistuskuten sinkki, koboltti, nikkeli ja erityisesti kupari; ja myös galvanointi. Katsotaanpa, miten kukin tapaus tapahtuu:
• Kuparin elektrolyyttinen puhdistus: tämä elektrolyyttinen kuparijalostus voi tuottaa noin 99,9%: n puhtauden ja sitä käytetään pääasiassa valmistukseen kuparilangat, joilla voi olla kyky johtaa hyvin sähkövirtaa, jos niissä on vähiten epäpuhtauksia vähentynyt.
Tarkkaile kuinka tämä prosessi tapahtuu, näkemällä kaavio alla kootusta elektrolyyttisäiliöstä:

Kuparisulfaatin vesiliuokseen (CuSo4 (aq)) - joka johtaa sähköä - niin, että epäpuhdas metallikupari anodi menettää elektroneja, toisin sanoen hapetetaan ja vapautetaan kationit (Cu
2+), jotka kerrostuvat negatiiviselle levylle. Tämä voi olla inertti platinalevy tai parempi puhdas kuparilevy. Se muodostaa katodin, joka pelkistyy kuparin kerrostuessa siihen. Siten elektrodeissa esiintyvät puolireaktiot ovat:Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
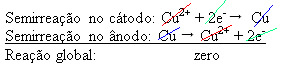
Se, että se antoi nollatuloksen, osoittaa, että kemiallista reaktiota ei tapahtunut, vaan vain kuparin kuljetus. Säiliön pohjassa on muita epäpuhtauksia, jotka olivat kuparissa, kuten kulta, hopea, piidioksidi (hiekka) ja muut mineraalit, joita voidaan jopa myydä.
• Galvanointi: metallipinnoite levitetään materiaalille, joka on suojattava korroosiolta.
Pinnoitteeksi valittu metalli - joka voi olla kromi (kromaus), nikkeli (nikkelöinti), hopea (hopeapinnoitus), kulta (kultaus) tai sinkki (galvanointi) - on anodi, positiivinen elektrodi, joka läpikäy hapettumisen ja menettää elektroneja. Se hapettuu suojatun materiaalin sijasta, koska sen pelkistyspotentiaali on suurempi.
Negatiivinen elektrodi, ts. Katodi, joka vastaanottaa nämä elektronit ja käy läpi pelkistyksen, on itse päällystetty materiaali. Tällä tavoin se pysyy suojattuna, vaikka sen pintaa loukataan.
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Elektrolyysi aktiivielektrodeilla"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/eletrolise-com-eletrodos-ativos.htm. Pääsy 28. kesäkuuta 2021.

