Ennen kuin ymmärrämme magneettisen kvanttiluvun ja kvanttiluvun pyöriä, on tarpeen muistaa, mitä sana kiertorata tarkoittaa.
Orbitaali on avaruuden alue ytimen ympärillä, missä todennäköisyys löytää tietty elektroni on suurin.
Ajattele pesää ymmärtääksesi paremmin. Jokaisen mehiläisen liikerataa ja sijaintia ei voida sanoa varmuudella, mutta voimme osoittaa alueen pesän ympärille, missä mehiläiset todennäköisimmin löytyvät. Vastaavasti kiertorata osoittaa alueen atomin ytimen ympärillä, jossa elektronien sijainti todennäköisesti määritetään.
Koska elektronilla on kaksi ominaisuutta eli se käyttäytyy hiukkasena ja myös aallona; tutkijat haluavat mieluummin tunnistaa sen energiasisällön perusteella. Matemaattisten laskelmien avulla tutkija Erwin Schrödinger, vuonna 1927, kertoi elektronin korpuskulaarisen luonteen, energian, varauksen ja massan. Siten jokaiselle elektronille tuli tunnusomaista kvanttiluvut.
Kvanttiluvut ovat matemaattisia koodeja, jotka liittyvät elektronienergiaan.
Kaksi tunnetuinta kvanttilukua ovat
pääkvanttiluku (n) ja toissijainen tai atsimutaalinen (siellä).Tärkein osoittaa kerroksen tai energiatason (K, L, M, N, O, P, Q), jossa elektroni löytyy, menen vastaavasti välillä 1-7. Atsimutaali edustaa energian alatasoja (s, p, d, f), jotka ovat vastaavasti 0,1,2,3. Molemmat esiintyvät alla olevassa energiakaaviossa, jossa pääkvanttiluku edustaa seitsemää "portaita" ja toissijaista kvanttilukua edustaa portaiden "portaat".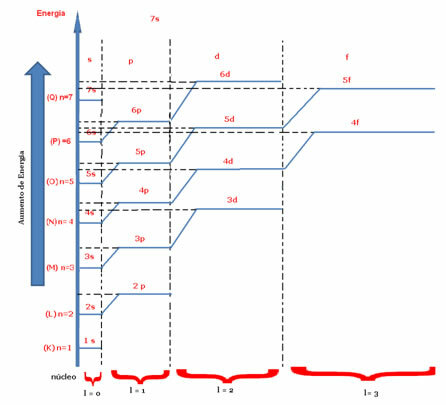
Tarkastellaan nyt magneettista kvanttilukua ja pyöritä:
- Magneettinen kvanttiluku (m tai msiellä) → osoittaa orbitaalien suunnan avaruudessa.
Alla olevan energiakaavion mukaan m: n arvot esitetään pieninä neliöinä (tai palloina tekijästä riippuen). Jokaisella kiertoradalla on magneettisen kvanttiluvun arvo, joka vaihtelee -siellä +1.
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)

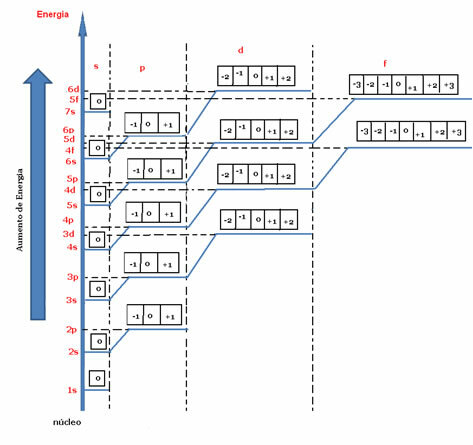
Energiakaavio, joka osoittaa magneettisen kvanttiluvun
-
Kvanttinumero pyöritä (s tai ms)→Kiertoradalle mahtuu enintään kaksi elektronia. Ne eivät hylkää toisiaan, koska ne pyörivät vastakkaisiin suuntiin luoden magneettikentät, jotka houkuttelevat toisiaan. Joten vetovoima, joka on magneettinen; ja vastenmielisyyttä, joka on sähköistä, tasapainotetaan.

Vastakkaiset tai antiparalleeliset pyörivät, elektronit pyöriivät vastakkaisiin suuntiin.
Edustamme siis jokaisessa pienessä neliössä korkeintaan kahta elektronia, jotka on esitetty nuolilla ja joiden arvot ovat +1/2 ja -1/2.
↑ |
Se edustaa sopimuksen mukaan elektronia, jonka spin on negatiivinen s = -1/2.
↓ |
Se edustaa yleisesti elektronia, jolla on positiivinen spin s = +1/2.
Tarkastellaan esimerkiksi helium-alkuaine, jolla on kaksi elektronia ja vain yksi energiataso; sen symboli on: 2hän
↑↓ |
Sen symbolisen esityksen antaa:
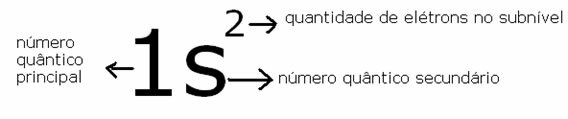
Esitys heliumin energisimmän elektronin asemasta
Joten meillä on heidän kvanttiluvut ensimmäiselle ja toiselle elektronille:
1. elektroni: 2. elektroni:
n = 1 n = 1
l = 0 l = 0
m = 0 m = 0
s = -1/2 s = +1/2
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Kvanttiluvut: magneettinen (m tai ml) ja spin (s tai ms)"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/numeros-quanticos-magnetico-m-ou-ml-spin-s-ou-ms.htm. Pääsy 28. kesäkuuta 2021.