Sulfonointireaktiot alkaaneissa he ovat orgaanisten substituutioiden reaktiot, jonka tarkoituksena on tuottaa sulfonihapot (orgaaniset yhdisteet, joilla on SO-ryhmä3H kiinnittynyt hiiliatomiin tai hiiliketjuun) ja veteen (H2O).
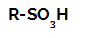
Sulfonihapon rakennekaava
Sulfonointireaktion suorittamiseksi alkaanit, meidän on sekoitettava alkaani (yhdiste, jonka muodostaa hiiliketju, joka on kyllästetty vain hiili- ja vetyatomilla) ja rikkihappo (H2VAIN4) väkevöidään, kuumennetaan (∆).
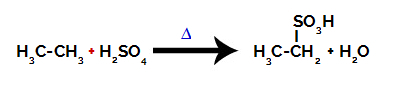
Kemiallinen yhtälö, joka edustaa kahden hiilen alkaanin sulfonointia
Alkaanien sulfonointireaktion periaatteet
Kuten alkaanisulfonointireaktio se on korvausreaktio, meillä on siinä vaihto pienempien komponenttien välillä elektronegatiivisuus reagoivista aineista, toisin sanoen alkaanin ja rikkihapon välillä. Alkaanissa on vety ja rikkihappo, sulfoniryhmä.
Alla on askel askeleelta a-mekanismi sulfonointireaktio alkaaneissa. Esimerkkinä käytämme yksinkertaisinta alkaania, metaania (CH4):
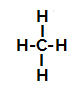
Metaanin rakennekaava
1. vaihe: Hydroksyylin (OH) ja rikin (S) välisen sidoksen rikkoutuminen rikkihapossa.
Jokaiselle rikkihapossa läsnä olevalle hydroksyyliryhmälle on tunnusomaista se, että se on elektronegatiivisempi. Kuumennettaessa reaktion aikana on taipumus, että hydroksyyliryhmän ja rikin välinen sidos katkeaa:
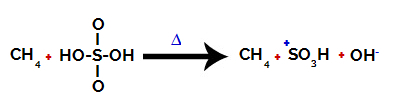
Rikin ja hydroksyylin välisen sidoksen hajoaminen
Kaikkien hydroksyylien sidoksen katkeamista ei kuitenkaan tapahdu, koska rakenne muuttuu elektronisesti. Sitten saadaan hydroksidianioni (OH).-) ja sulfonikationi.
2. vaihe: Hydroksyyliryhmä hyökkää alkaanimolekyyliin.
Sitten hydroksiryhmä (OH-) hyökkää alkaaniin aiheuttaen hiilen ja vedyn välisen sidoksen (joka on hauraampi niiden välisen elektronegatiivisuuden eron takia) rikkoutumisen.
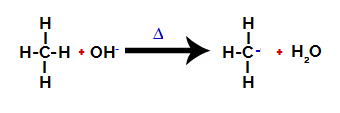
Hiilen ja vedyn välisen sidoksen katkaiseminen alkaanissa
merkintä: Hiilen ja vedyn välisen sidoksen katkeaminen tapahtuu aina useimmiten pienemmällä elektronisella tiheydellä tai varauksella olevalla hiilellä. Mitä vähemmän vetyjä hiiltä on tai mitä enemmän ryhmiä siihen on kiinnittynyt, sitä pienempi sen elektronitiheys. Joten meillä on:
Tertiäärinen hiili
Kun sidos on katkennut, alkaanista tulee elektronipuutteinen hiili (karbokatio). Hydroksidiryhmä (OH)-) on vuorovaikutuksessa vapautuneen vedyn kanssa ja muodostaa vesimolekyylin.
3. vaihe: Muodostuneen radikaalin hyökkäys sulfoniryhmään.
Lopuksi alkaanin hyökkää sulfoniryhmä muodostaen sulfonihapon.
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
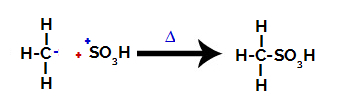
Rakenteet, jotka ovat vuorovaikutuksessa ja muodostavat sulfonihappoa
Esimerkkejä yhtälöistä, jotka edustavat alkaanien sulfonointireaktioita
1. esimerkki: Propaanin sulfonointi.
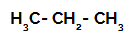
Propaanin rakennekaava
Propaanilla on kaksi primaarista hiiltä ja yksi sekundäärinen hiili, joilla on erilaiset varaukset, koska ne ovat sitoutuneet erilaisiin vetymääriin. Koska hiili on enemmän elektronegatiivista kuin vety, näillä hiileillä on erilaiset elektronitiheydet.
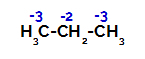
Varojen jakautuminen propaanin jokaiselle hiiliatomille
Primaarihiileillä varaus on -3 (koska se on sitoutunut kolmeen vetyyn) ja sekundäärisen hiilen varaus on -2 (koska se on sitoutunut kahteen vetyyn). Täten hiilin ja vedyn välisessä sidoksessa tapahtuu katkos, joskus hiilellä 1 (molekyylissä), joskus hiilellä 2 (toisen molekyylin).
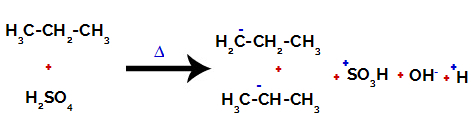
Hiilen ja vedyn välisen sidoksen katkaiseminen eri hiileillä
Sekä rikkihapossa että alkaanissa olevien sidosten rikkoutumisen jälkeen muodostuu tuotteet korvaamalla vety hiilessä 1 sulfoniryhmällä, ja sama tapahtuu hiilellä 2.
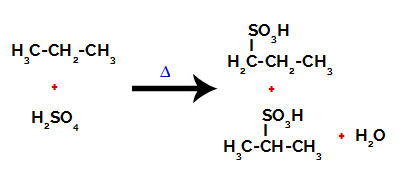
Propaanin sulfonoitumisesta muodostuneet tuotteet
2. esimerkki: 2-metyylibutaanin sulfonointi.

2-metyylibutaanin rakennekaava
2-metyylibutaanissa on kolme primaarista hiiltä, toissijainen hiili ja tertiäärinen hiili, joilla on erilaiset varaukset ja siten erilaiset elektroniset tiheydet, kuten voidaan nähdä seuraavasta rakenteesta:
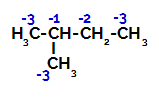
Elektronisten varausten jakautuminen 2-metyylibutaanissa
Siksi 2-metyylibutaanissa on useita mahdollisuuksia katkaista hiili ja vety, joita voi esiintyä hiili 1 (molekyyli), hiili 2 (toinen molekyyli), hiili 3 tai hiili 4. On kuitenkin huomionarvoista, että häiriöt hiililuvulla 2 ovat yleisempiä.
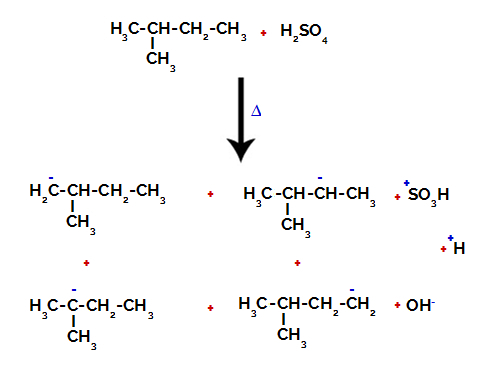
Hiilen ja vedyn välisen sidoksen katkaiseminen eri hiileillä
Sekä rikkihapossa että alkaanissa olevien sidosten välisten katkosten jälkeen muodostuu tuotteet korvaamalla hiilen 1 vety sulfoniryhmällä, ja sama tapahtuu hiili 2.

Tuotteet, jotka muodostuvat 2-metyylibutaanin sulfonoitumisesta
Minun luona Diogo Lopes Dias
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
PÄIVÄT, Diogo Lopes. "Sulfonointireaktiot alkaaneissa"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/reacoes-sulfonacao-alcanos.htm. Pääsy 28. kesäkuuta 2021.


