THE suola silta ehdotti englantilainen kemisti Frederic Daniell vuonna 1836, kun tämä tutkija perusti akku nimetty hänen mukaansa (Danill's Pile). tämä silta on U-muotoinen putki, jolla on kaksi huokoista päätä. (koostuu puuvillasta tai agar-agarista) ja sisältää vesiliuoksen, jonka muodostaa vesi ja suola. Se yhdistää epäsuorasti solun kahden puolisolun (anodin ja katodin) liuokset.
Havainto: Anodi on pariston negatiivinen napa ja siellä tapahtuu hapettumista, ja katodi on positiivinen napa ja missä tapahtuu pelkistymistä.
Suolasillan merkityksen ymmärtämiseksi on aluksi tarpeen ymmärtää kasan toiminta. Katso alla oleva kaavio:
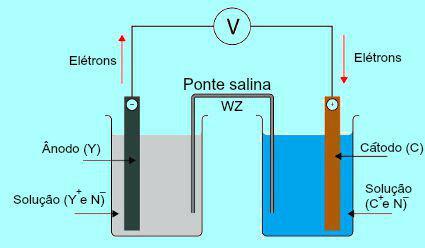
Daniell-pinon yleinen kaavio
Aluksi anodissa olevan levyn metalli (Y) hapettuu. Hapetessaan metalli muuttuu kationiksi, joka putoaa liuokseen, jossa levy on. Tästä syystä anodiliuoksessa alkaa olla suurempi kationikonsentraatio (Y+). Tässä tapauksessa havaitaan anodimetallilevyn väheneminen.
Y → ja- + Y+
Sitten anodilevyn metallin hapetuksessa menetetyt elektronit kulkevat ulkoisen sähköjohdon läpi ja menevät katodissa olevaan metallilevyyn. Siten katodissa oleva levy latautuu elektronilla.
-
Esillä olevat kationit (C+) liuoksessa siirtyä kohti katodilevyä, koska se on varautunut elektronilla. Kun kationit saavat levyssä olevia elektroneja, neutraali (vakaa ja kiinteä) ja tarttuu siihen. Tästä syystä katodiliuoksessa on suurempi anionipitoisuus kuin kationeissa. Tässä tapauksessa havaitaan katodimetallilevyn koon kasvu.
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Ç+ + ja- → C
Ymmärtämisestä miten Daniellin kasa, on mahdollista havaita, että anodissa oleva liuos vastaanottaa suuremman määrän Y-kationeja+ johtuen X-levyn metallin hapettumisesta. Katodissa oleva liuos puolestaan menettää kationinsa (C+), koska ne kärsivät plakin vähenemisestä.
Suolasillan työtä korostetaan juuri tässä asiassa. Tämän sillan päätehtävänä on edistää sekä anodi- että katodiliuoksissa olevien varausten tasapainoa. Suolasillassa meillä on aina suola (yleensä kaliumkloridi tai ammoniumnitraatti) dissosioitunut veteen. Katso yhtälön esitys suolasillassa:
WZ + H2O → W+ + Z-
Suolasillassa on kaksi ionia (W+ ja Z-), jotka siirretään katodille ja anodille seuraavasti:
) Anodi vastaanottaa anionit (Z-), jota esiintyy suolasillassa alkuaineen (Y) hapettumisen vuoksi, mikä aiheuttaa kationien määrän (Y+) liuoksessa.
B) Katodi vastaanottaa kationeja (W+), koska kationi (C+) liuoksessa läsnä oleva määrä vähenee levyllä. Siten katodiliuoksessa on suurempi määrä anioneja (N-) ja siten vastaanottaa suolasillassa olevan kationin.
Minun luona. Diogo Lopes Dias
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
PÄIVÄT, Diogo Lopes. "Purjesilta"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/ponte-salina.htm. Pääsy 28. kesäkuuta 2021.


