THE yksinkertainen tislaus ei ole muuta kuin menetelmä seosten erottaminen, käytetään erityisesti, kun meillä on homogeeninen seos muodostuu nesteeseen liuotetusta kiinteästä aineesta, kuten vedessä olevasta natriumkloridista (NaCl).

Natriumkloridia voidaan saada yksinkertaisella tislauksella
On tarpeen ymmärtää, että yksinkertainen tislaus, tapahtuu aina kaksi perustavanlaatuista fyysisen tilan muutosta, höyrystyminen (siirtyminen nesteestä kaasuun) ja tiivistyminen (siirtyminen höyrystä nesteeseen).
Laboratoriossa suorittaa a yksinkertainen tislaus, tarvitaan seuraavat laitteet:
Bunsen-poltin tai -levy (1): seoksen lämmittämiseen käytettävät laitteet;
Tislauspullo (2): astia, johon seos pakataan lämmitystä varten;
Yleinen tuki (3): kynnen kiinnittämiseen käytettävät laitteet;
Kynsi (4): laitteet, joita käytetään tislauspullon pitämiseen;
Lämpömittari (5): laitteet, joita käytetään lämpötilan mittaamiseen kokeen aikana;
Tulppa (*): puumateriaali tislauspullon yläosan sulkemiseksi;
Veden ulostulo (6): polku, jonka läpi lämmitetty vesi poistuu;
Veden sisääntulo (7): polku, jonka läpi kylmä vesi pääsee;
Lauhdutin (8): laitteet, joissa kondensaatiota esiintyy kokeen aikana;
Erlenmeyer tai dekantterilasi (9): astia, johon tislattu neste kerätään.
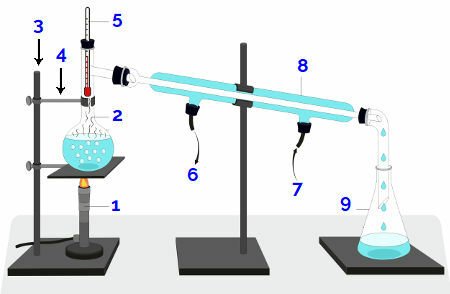
Kaavamainen esitys tislaajasta
Suorituksen aikana yksinkertainen tislaus, meillä on seuraavat tapahtumat:
Ensimmäinen: tislauslaitteet on järjestetty;
Toinen: seos (esim. vesi ja natriumkloridi) lisätään tislauspulloon;
Kolmas: seoksen lämmitys aloitetaan tislauspullossa Bunsen-polttimella tai kuumennuslevyllä;
Huone: vesi alkaa höyrystyä tislauspullon sisällä;
Viides: vesihöyry joutuu väistämättä tislaajaan, koska ilmapallon yläosa on suljettu ja muuttuu taas nesteeksi;
Kuudes: Tiivistetty neste kerätään sitten dekantterilasiin tai erlenmeyerpulloon.

Tislatun nesteen esitys
Minun luona. Diogo Lopes Dias
Lähde: Brasilian koulu - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-destilacao-simples.htm

