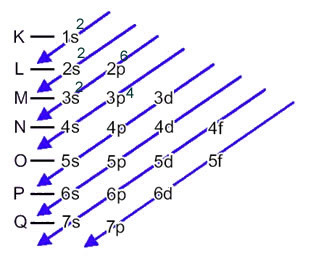
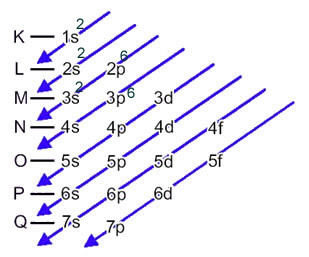
Atomin elektronien elektroninen jakelu neutraalissa tai perustilassa tapahtuu yleisesti Pauling-kaavio, nähtävissä alapuolella:
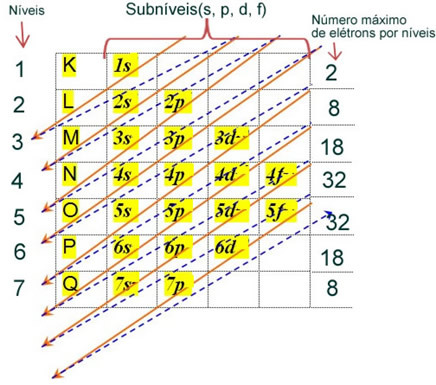
Tämän jakelun yksityiskohtaiset säännöt löytyvät seuraavista kahdesta verkkosivustomme tekstistä: “Elektronien elektroninen jakelu"ja"Sähköisen jakelun säännöt”.
Ionien sähköinen jakelu toimii aluksi samalla tavalla kuin neutraalissa tilassa olevien atomien kohdalla; vain yhdellä erolla. Koska ioni on atomi, joka on saanut tai menettänyt elektroneja, meidän on otettava tämä huomioon ja tehtävä seuraava:

Tärkeä havainto on: muutos tehdään uloimmassa alatasossa eikä eniten energinen.
jos ioni on a kationia, meidän täytyy poista elektronit että hän menetti. Katsotaanpa esimerkkiä:
Rautatomilla (atomiluku = 26) on seuraava elektroninen jakauma alatasoilla energeettisessä järjestyksessä: 1s2 2s2 2p6 3s2 3p6 4s2 3d6. Mitä tulee elektronisiin kerroksiin, meillä on: K =2; L = 8; M = 14; N = 2.
Tämä jakauma on esitetty alla olevassa Pauling-kaaviossa:
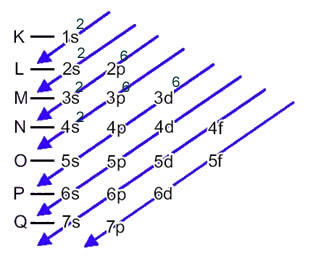
Kun rautatomi menettää 2 elektronia, se muuttuu Fe-kationiksi.
2+. Joten, kun teemme sähköistä jakelua, meidän on poista 2 elektronia viimeisestä kuoresta(N) eikä eniten energinen alataso, kuten alla: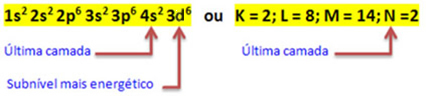
Siten Fe-kationin sähköinen jakelu2+ antaa:
1s2 2s2 2p6 3s2 3p6 3d6 tai K = 2; L = 8; M = 14
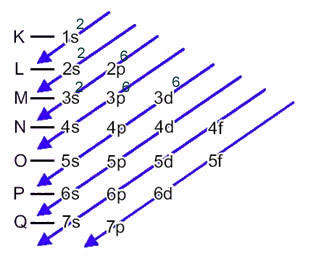
Nyt, jos meidän on suoritettava a anioni, meidän täytyy lisää vastaanotetut elektronit.Katso, miten tämä tapahtuu seuraavassa esimerkissä:
Rikkianioni (16s2-) muodostuu rikkiatomista (16S) 2 elektronin vahvistuksella, kuten varaus 2 osoittaa. Sen perustilan sähköisen jakelun antaa:
1s2 2s2 2p6 3s2 3p4 tai K = 2; L = 8; M = 6
Tässä tapauksessa viimeinen alataso on sama kuin energian alataso 3p. Joten lisätään siihen kaksi rikki-anionin elektronia:
1s2 2s2 2p6 3s2 3p6 tai K = 2; L = 8; M = 8
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Lähde: Brasilian koulu - https://brasilescola.uol.com.br/quimica/distribuicao-eletronica-ions.htm
