THE kulmageometria on yksi monista molekyyligeometria, joka voi silti olla lineaarinen, pyramidinen, tasainen trigonaalinen, tetraedrinen, jne. Kulmageometria löytyy vain molekyyleistä, joilla on seuraavat ominaisuudet:
Triatomiikka eli heillä on vain kolme atomia;
Keskiatomissa on vähintään kolme elektronipilveä.
merkintä: sähköinen pilvi on kaikki kovalenttisidos (yksi-, kaksinkertainen, kolminkertainen tai koordinaatti) atomien ja elektroniparien välillä valenssikerros jotka eivät osallistu puheluun.
Katso joitain esimerkkejä molekyyleistä, joilla on kulmageometria:
1. esimerkki: vesi (H2O)

tavanomainen vesirakenne
Veden rakenteessa meillä on:
Kolme atomia: kaksi vetyä ja yksi happi;
Happi on keskeinen atomi, koska se muodostaa enemmän sidoksia (kaksi, koska se kuuluu VIA-perheeseen);
Kaksi yksittäistä sidosta hapen ja vetyjen välillä. Tämä johtuu siitä, että kukin vety voi muodostaa vain yhden sidoksen ja happi kaksi sidosta;
Neljä sitoutumatonta elektronia hapessa, koska sen valenssikuoressa on kuusi elektronia ja sidoksissa käytetään vain kahta.
Siksi, kuten vesimolekyylissä, keskiatomissa on kolme atomia ja neljä elektronista pilviä (kaksi yksittäistä sidosta ja kaksi sitoutumatonta elektroniparia), geometria on kulmikas.
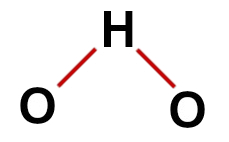
Oikea veden rakennekaava
merkintä: Aina kun molekyylillä on nämä kuviot, atomien väliin muodostuva kulma on noin 109º28'.
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
2. esimerkki: Rikkidioksidi (SO2)

Rikkidioksidin tavanomainen rakenne
Rikkidioksidin rakenteessa meillä on:
Kolme atomia: kaksi oksigeeniä ja yksi rikkiatomi;
Rikki on keskeinen atomi, koska se on molekyylin pienin alkuaine, koska kaikkien alkuaineiden on tehtävä sama määrä sidoksia (kaksi);
Kaksoissidos rikin ja yhden hapen välillä. Tämä johtuu siitä, että molemmat tarvitsevat kaksi liitäntää;
Yksi koordinaatti tai datatiivinen kovalenttinen sidos, koska rikki oli vakaa pariliitoksen tekemisen jälkeen toisen hapen kanssa, mutta silti on happiatomi, joka tarvitsee kaksi elektronia;
Neljä sitoutumatonta elektronia hapessa. Tämä johtuu siitä, että hapessa on kuusi elektronia valenssikuoressa ja se käyttää vain kahta sidoksissa.
Siten, kuten rikkidioksidimolekyylissä, keskiatomissa on kolme atomia ja neljä elektronista pilviä (kaksi yksittäistä sidosta ja kaksi paria sitoutumattomia elektroneja), geometria on kulmikas.
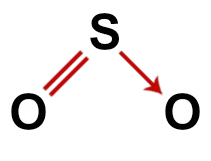
Rikkidioksidin oikea rakennekaava
merkintä: Aina kun molekyylillä on nämä kuviot, atomien väliin muodostuva kulma on noin 120O.
Minun luona. Diogo Lopes Dias
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
PÄIVÄT, Diogo Lopes. "Mikä on kulmageometria?"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-geometria-angular.htm. Pääsy 27. kesäkuuta 2021.

