vuonna lisäysreaktiotsisään alkeenit(hiilivedyt, joilla on kaksoissidos kahden hiiliatomin välillä), kahden hiilen välinen pi-sidos rikkoutuu ja kukin hiilistä kiinnittyy uuteen atomiin. Katso:
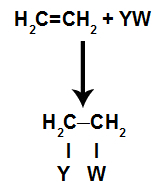
Yleinen kaavamainen malli additioreaktiosta
Lisäysreaktion periaatteet
a) pi-linkin rikkoutuminen
Pi-sidos hajoaa helposti, koska se on heikompi sidos kuin sigmasidos. Kuitenkin, jotta tämä tapahtuisi, on välttämätöntä, että alkeenille altistetaan olosuhteet, jotka aikaansaavat tämän häiriön. Rikkoutuneen pi -sidoksen kahden hiilen välillä, sitoutumiskohta (uusille atomille) ilmestyy aina jokaiselle mukana olevalle hiilelle.
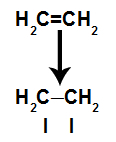
Kaaviokuva, joka kuvaa pi-linkin rikkoutumista
b) Edellytykset pi-sidoksen rikkoutumiselle
Pi-sidoksen rikkoutumista suosivat tekijät ovat:
Katalyyttien käyttö;
Lämmitys;
Hapon läsnäolo reaktioväliaineessa.
c) Lisäysreaktion esiintyminen
Sitoutumiskohdat, jotka syntyvät pi-sidoksen rikkoutumisen jälkeen, ovat aina al- kaanin kanssa samassa säiliössä olevan reagenssin atomeilla. Lisäysreaktio on nimetty alkeeniin sekoitetun reagenssityypin mukaan.
Lisäysreaktioiden tyypit alkeeneissa
a) Hydraus
Alekseeni sekoitetaan vetykaasun (H2) astiassa ja altistetaan kiinteälle katalyytille (nikkeli, platina tai palladium) ja kuumennetaan (A).
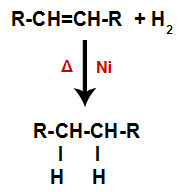
Alkeeenien hydrausreaktion yleinen kaavio
Katalyytin läsnäolo ja lämmitys aiheuttavat alkeenin pi-sidoksen ja sigma-sidoksen H-vetyjen välillä2 rikki nopeammin. Tämän avulla meillä on kaksi sitoutumiskohtaa alkeeniin ja kaksi vapaata vetyatomia reaktioväliaineeseen.

Atomin sitoutumis- ja erotuspaikkojen luominen
Täten heti sen jälkeen kukin vapaa vetyatomi vie yhden alkeeniin muodostuneista sitoutumiskohdista. Koska muodostuneessa aineessa on vain hiilejä ja vetyjä sekä vain yksinkertaisia sidoksia hiilien välillä, se on a alkaani.
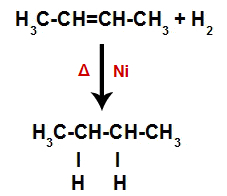
Yhtälö, joka edustaa alkaanin muodostumista hydrauksessa
B) Halogenointi
Alekseeni sekoitetaan yksinkertaisten aineiden kanssa (F2Cl2, br2 Hei2) muodostama halogeenit (kloori, fluori, jodi ja bromi) astiassa ja altistetaan valolle (λ) ja kuumennukselle (A).

Alkeenien halogenointireaktion yleinen kaavio
Valon ja lämmityksen vaikutus saa alkeenin pi-sidoksen ja halogeenin muodostamien aineiden välisen sigmasidoksen hajoamaan nopeammin. Tämän avulla meillä on kaksi sitoutumiskohtaa alkeeniin ja kaksi vapaata halogeeniatomia reaktioväliaineeseen.

Atomin sitoutumis- ja erotuspaikkojen luominen
Täten heti sen jälkeen kukin vapaa halogeeniatomi vie yhden alkeeniin muodostuneista sitoutumiskohdista. Koska muodostuneessa aineessa on halogeeni, joka on sitoutunut hiileistä ja vetyistä koostuvaan rakenteeseen, se on a orgaaninen halogenidi.

Yhtälö, joka edustaa orgaanisen halogenidin muodostumista halogenoinnissa
c) Nesteytys
Alkoheeni sekoitetaan veteen (H2O) astiassa ja alistettu katalyytin (tässä tapauksessa rikkihapon) vaikutukselle.
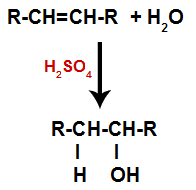
Alkeeenien hydraatioreaktion yleinen kaavio
Rikkihapon läsnäolo reaktiossa saa alkeenin pi-sidoksen ja vedyn (H) ja hydroksyylin (OH) välisen sigmasidoksen hajoamaan nopeammin. Tämän myötä olemme muodostaneet kaksi sitoutumiskohtaa alkeeniin ja yhden vapaan vetyä ja yhden hydroksyylin reaktioväliaineeseen.
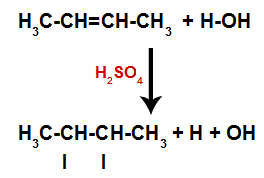
Atomin sitoutumis- ja erotuspaikkojen luominen
Siten pian sen jälkeen vety ja hydroksyyli vievät yhden alkeeniin muodostuneista sitoutumiskohdista. Koska muodostuneessa aineessa on hydroksyyli sitoutunut tyydyttyneeseen hiileen (se muodostaa vain yksinkertaisia sidoksia), se on alkoholi.
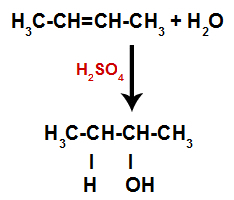
Yhtälö, joka edustaa alkoholin muodostumista nesteytyksessä
d) Lisäys vetyhalogenideilla
Alekseeni sekoitetaan halogenoidun epäorgaanisen hapon (HF, HI, HCl, HBr) kanssa astiassa.

Happohalogenidireaktion yleinen kaava alkeeneissa
Hapon läsnäolo reaktiossa aiheuttaa alkeenin pi-sidoksen hajoamisen nopeammin. Yksittäinen sidos hapossa hajoaa, koska nämä aineet luonnollisesti ionisoituvat. Siten alkeeniin luodaan kaksi sitoutumiskohtaa ja reaktioväliaineessa on vapaata vetyä ja halogeenia.
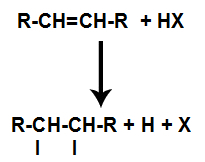
Atomin sitoutumis- ja erotuspaikkojen luominen
Siten pian sen jälkeen vety ja halogeeni vievät yhden alkeeniin muodostuneista sitoutumiskohdista. Koska muodostuneessa aineessa on halogeenia, joka on sitoutunut hiileistä ja vetyistä koostuvaan rakenteeseen, se on orgaaninen halogenidi.
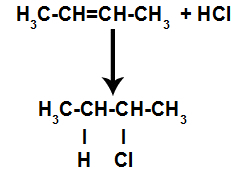
Yhtälö, joka edustaa orgaanisen halogenidin muodostumista halogenoinnissa
Minun luona. Diogo Lopes Dias
Lähde: Brasilian koulu - https://brasilescola.uol.com.br/quimica/reacoes-adicao-alcenos.htm



