Joidenkin yhdisteiden ei tarvitse olla kahdeksan elektronia valenssikuoressa vakauden saavuttamiseksi, joten niitä pidetään poikkeuksina Octet-säännöstä. Opi nyt, miksi jotkut elementit välttävät velvollisuutta pitää elektronien oktetti viimeisessä kuoressa.
Beryllium (Olla)
Se on poikkeus oktettisäännöstä, koska se pystyy muodostamaan yhdisteitä kahdella yksittäisellä sidoksella, joten se vakautuu vain neljän elektronin kanssa valenssikuoressa. 
Koska vedyn (H) on luovuttava kahdesta elektronista sidoksen muodostamiseksi (H - No - H), beryllium (Be) -atomi jakaa elektroninsa ja saavuttaa vakauden.
Alumiini (Al)
Se on poikkeus Octet-säännöstä, koska se saavuttaa vakauden kuuden elektronin kanssa valenssikuoressa. Alumiiniatomi pyrkii luovuttamaan elektronejaan ja voi siten muodostaa kolme yksittäistä sidosta muiden atomien kanssa: 
Tässä tapauksessa alumiini (Al) muodosti kolme sidosta kolmella fluoriatomilla.
Boori (B)
Se muodostaa molekyyliaineita kolmella yksittäisellä sidoksella. 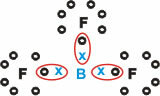
Huomaa, että boori (B) yleensä lahjoittaa elektroninsa fluori (F) -atomille, joka noudattaa oktettisääntöä ja vaatii kahdeksan elektronia valenssikuoressa. Kun boori luopuu elektronistaan, fluori stabiloituu muodostuneen oktetin kanssa.
Kirjoittanut Líria Alves
Valmistunut kemian alalta
Brasilian koulutiimi
Katso lisää!
Oktettiteoria
Yleinen kemia - Kemia - Brasilian koulu
Lähde: Brasilian koulu - https://brasilescola.uol.com.br/quimica/excecoes-regra-octeto.htm
