Happooksidit ovat niitä oksideja, jotka reagoidessaan veden kanssa tuottavat happoa tuotteena. Reagoiden emäksen kanssa tuotteet ovat suolaa ja vettä.
Näillä yhdisteillä on yleensä kovalenttinen luonne, toisin sanoen ne ovat molekyylimuotoisia, veteen liukenevia ja muodostuvat enimmäkseen ei-metalleista, jotka ovat elementtejä, joilla on korkea elektronegatiivisuus. Metalleilla muodostuessaan niillä on korkea hapetusluku (sähkövaraus).
Esimerkkejä:
CO2, VAIN2, VAIN3, P2O5Cl2O6,2, ei2O4, ei2O5, jne.
Seuraava on yleinen kaavio happooksidien tyypillisistä reaktioista ja esimerkki:
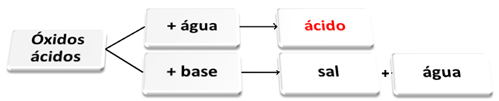
Hapon oksidit, jotka reagoivat veden ja emäksen kanssa
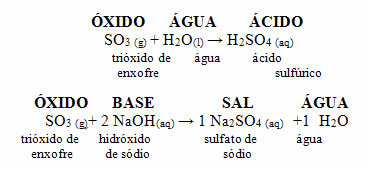
Hapan oksideja kutsutaan myös anhydridit, koska tämä sana tulee kreikan kielestä anhydros, joka tarkoittaa "ei vettä"ja happo-oksideja voidaan pitää "vedettömänä happona".
Joidenkin happooksidien ominaisuudet ja sovellukset:
• Hiilidioksidi (hiilidioksidi) - CO2:
Tätä yhdistettä käytetään kaasuna virvoitusjuomissa ja kivennäisvesissä, koska korkean paineen alaisena se muuttuu vesiliukoiseksi. Se tuottaa näissä tuotteissa happaman väliaineen, koska se on hapan oksidi, joka reagoi veden kanssa tuottaen happoa alla olevan reaktion mukaisesti:

Alle 78 ° C: n lämpötilassa se on kiinteässä tilassa ja tunnetaan kuivajäänä, joka saa nimensä, koska sen ulkonäkö muistuttaa jäätä. yleinen, mutta se ei sula, siirtyy nestemäiseen tilaan huoneen lämpötilassa, mutta se menee höyrytilaan, ts. ylevää. Siksi tätä ominaisuutta käytetään luonnonkauniina resursseina konserteissa, elokuvissa, teattereissa, juhlissa jne.

Hiilidioksidi on happooksidi
Sitä esiintyy myös ilmakehässä ihmisen hengityksen, fossiilisten polttoaineiden (hiili, öljytuotteet, alkoholi jne.) Polttamisen ja metsäpalojen seurauksena. Siksi hän on yksi niistä, jotka ovat vastuussa happosateista.
• Rikkioksidit - SO2 ja niin3
Näitä oksideja esiintyy myös ilmakehässä, jotka ovat luonnollista ja keinotekoista alkuperää. Luonnollinen tapahtuu tulivuorenpurkausten ja kasvien ja eläinten hajoamisen kautta. Keinotekoinen vastaa suurinta määrää näitä oksideja ilmakehässä sellaisina kuin ne ovat karkotetaan polttamalla fossiilisia polttoaineita, pääasiassa dieselöljyä, joka sisältää rikkiä, kuten epäpuhtaus.
Rikkidioksidi (SO2) reagoi ilmakehän hapen kanssa tuottaen rikkitrioksidia (SO3). Kun tämä viimeinen oksidi reagoi sadeveden kanssa, muodostuu rikkihappoa, joka on erittäin voimakas ja aiheuttaa vahinkoa.
• Rikin polttaminen polttoaineista: S + O2 → käyttöjärjestelmä2
• SO2: n muuntaminen SO3: ksi: SO2 + ½2 → käyttöjärjestelmä3
SO2: n ja SO3: n reaktiot hapon antavan veden kanssa: SO2 + H2O → H2VAIN3
VAIN3 + H2O → H2VAIN4
• Dinityppitetroksidit (typpi-typpi-anhydridi) - N2O4
Tämän yhdisteen kiehumispiste on 22ºC, sillä on keltainen väri ja se on melko haihtuva. Se muodostuu ilmakehässä hapen hapettumisen seurauksena ja voi olla nestemäisessä muodossa monotyyppidioksidin tai typpioksidin (NO2). Tämän lämpötilan yläpuolella se saa NO: n muodon2:
N2O4 ↔ EI2
Se on erittäin myrkyllinen kaasu ja sen hengittäminen on kohtalokasta. Sitä käytetään myös rakettipolttoaineiden koostumuksessa.
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta

