THE yhteinen keskittyminen, jota kutsutaan myös pitoisuudeksi g/l, on liuenneen aineen massan suhde liuoksen tilavuudessa.
Matemaattisesti yhteinen pitoisuus ilmaistaan kaavalla:
C = m/v
Missä,
C: yhteinen konsentraatio;
m: liuenneen aineen massa;
V: liuoksen tilavuus.
Yleisimmin käytetty yhteisen pitoisuuden yksikkö on g/l, koska liuenneen aineen massa lasketaan grammoina (g) ja liuoksen tilavuus litroina (L).
Esimerkiksi merivedessä on suuri määrä liuenneita suoloja ja yksi niistä on natriumkloridi (NaCl), joka tunnetaan myös pöytäsuolana.
Meriveden natriumkloridin pitoisuus on keskimäärin 2,5 g/l. Joten jokaisessa 1 litrassa merivettä, joka on liuos, on 2,5 grammaa suolaa, joka on liuennutta ainetta.
Miten lasketaan yhteinen pitoisuus?
Liuos on homogeeninen seos, jonka muodostaa pienempi määrä aine, nimeltään liuennut aine, joka on liuennut liuottimeen, jota on suurempi määrä.
Näin ollen yleinen pitoisuus viittaa liuenneen aineen määrään tietyssä liuostilavuudessa. Mitä enemmän liuennutta ainetta on liuennut liuokseen, sitä väkevämpi se on. Muutoin eli alhainen liuennut aine osoittaa, että liuos on laimennettu.
Esimerkki 1: Mikä on hopeajodidiliuoksen (AgI) pitoisuus g/l, joka sisältää 2,6 g 1 litrassa liuosta?
Kun annetaan liuenneen aineen määrä ja liuoksen tilavuus, yhdistämme arvot yhteiseen pitoisuuskaavaan löytääksemme sen arvon.
Siksi 2,6 g/l hopeajodidiliuoksessa on 2,6 g liuennutta ainetta jokaisessa litrassa liuosta.
Esimerkki 2: Mikä on liuenneen aineen massa, kun liuotin haihdutetaan 500 ml: sta suolaliuosta, jonka pitoisuus on 6 g/l?
Huomaa, että joissakin laskelmissa voimme löytää kuvatun yhteisen pitoisuuden, jotta voimme laskea liuenneen aineen massan.
On myös syytä kiinnittää huomiota yksiköihin. Koska yleinen pitoisuus on annettu g/l, tässä tapauksessa tilavuusyksikkö on muutettava ennen kaavan soveltamista.
Koska 1 litra sisältää 1000 ml, niin 500 ml vastaa 0,5 litraa.
Siten, kun liuotin haihdutettiin liuoksesta, jonka pitoisuus oli 6 g/l, saatiin 12 g liuennutta ainetta.
Hanki lisää tietoa sisällöstä:
- Liuoksen pitoisuus
- molaarinen pitoisuus
- Liuosten laimentaminen
Ratkaistiin yleisiä keskittymisharjoituksia
Käytä seuraavia kysymyksiä tarkistaaksesi aiemmin hankitut tiedot.
Kysymys 1
(Unicamp) Liuotin haihdutetaan kokonaan 250 ml: sta MgCl: n vesiliuosta2 pitoisuus 8,0 g/l. Kuinka monta grammaa liuennutta ainetta saadaan?
a) 8.0
b) 6.0
c) 4.0
d) 2.0
e) 1.0
Oikea vaihtoehto: d) 2.0.
kysymys 2
Katso alla oleva kuva.
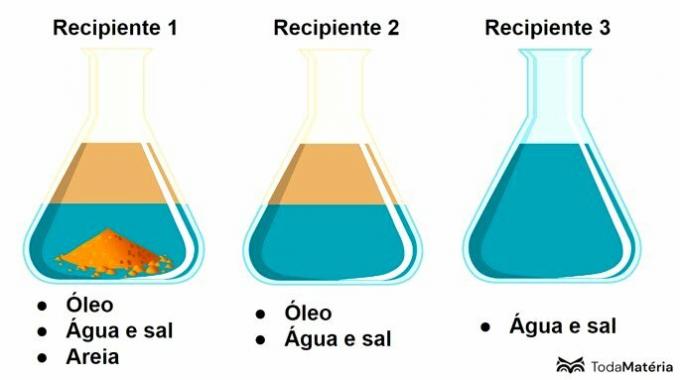
Tässä kaaviossa säiliö 3 sisältää a
a) heterogeeninen seos
b) puhdas aine
c) Ratkaisu
d) kolloidiseos
Oikea vaihtoehto: c) Ratkaisu.
Säiliö 3 sisältää liuoksen, joka on liuenneen aineen ja liuottimen muodostama homogeeninen seos, jossa liuenneena aineena on suola ja liuottimena vesi.
Yleisesti voidaan sanoa, että liuennutta ainetta on komponentti pienimmässä määrin ja liuotinta on läsnä suurin määrä.
Säiliö 1 on heterogeeninen seos, jossa on 3 faasia ja säiliö 2 vastaa heterogeenista 2 faasin seosta.
kysymys 3
Liuos valmistettiin liuottamalla 4,0 g magnesiumkloridia MgCl2 kunnes saavutetaan pitoisuus 2,0 g/l. Mikä tilavuus liuosta valmistettiin?
a) 1 l
b) 2 litraa
c) 4 litraa
d) 6 litraa
Oikea vaihtoehto: b) 2 L.
Katso lisää kommentoituun ratkaisuun liittyviä ongelmia osoitteessa yleisiä keskittymisharjoituksia.
Bibliografiset viittaukset
FONSECA, M. R. M. Kemia, 1. 1. toim. São Paulo: Attika, 2013.
SANTOS, W.L.P; MOL, G.S. Kansalaiskemia, 1. 2. toim. São Paulo: Editora AJS, 2013.
USBERCO, J. Yhdistä kemia, 1. 2. toim. São Paulo: Saraiva, 2014.
- Harjoituksia yhteisestä keskittymisestä kommentoidulla palautteella
- kemiallisia liuoksia
- Liuotin ja liuotin: mitä ne ovat, erot ja esimerkit
- Liuoksen pitoisuus
- Liukoisuus
- Molaarisuus tai molaarinen pitoisuus: mikä se on, kaava ja kuinka laskea
- Liuosten laimentaminen
- Harjoitukset aineen ominaisuuksista



