THE nihonium, atominumero 113 ja symboli Nh on jaksollisen järjestelmän ryhmään 13 kuuluva alkuaine. Lisäksi se on superraskas alkuaine, jota ei löydy luonnosta. Siten sen saaminen voidaan tehdä vain keinotekoisesti ydinfuusioreaktioiden avulla. Nihoniumin kemialliset ominaisuudet ovat vielä epäselviä, mutta sen arvellaan käyttäytyvän joissain tapauksissa samalla tavalla kuin kevyempi vastineensa tallium.
Nihonium saatiin alun perin sulattamalla 70Zn kanssa 209Bi, Riken Institute, Japani, vuonna 2003. Vaikka myös venäläiset ja amerikkalaiset tutkijat pyysivät tulla tunnustetuiksi alkuaineen 113 löytäjiksi, IUPAC tunnusti japanilaiset tiedemiehet. Nimi viittaa sanaan Nihon, kuten japanilaiset kutsuvat kotimaataan.
Lue myös: Gallium — toinen kemiallinen alkuaine, joka kuuluu jaksollisen järjestelmän ryhmään 13
Tämän artikkelin aiheet
- 1 - Yhteenveto nihoniumista
- 2 - Nihoniumin ominaisuudet
- 3 - Nihoniumin ominaisuudet
- 4 - Nihoniumin saaminen
- 5 - Nihonion historia
- 6 - Ratkaistiin nihoniumia koskevia harjoituksia
yhteenveto nihoniumista
Se on synteettinen kemiallinen alkuaine, joka sijaitsee ryhmässä 13 Jaksollinen järjestelmä.
Sen tuotanto alkoi vuonna 2003 Riken Institutessa, Japanissa.
Se muodostaa elementtien ryhmän, jotka viimeksi sisällytettiin jaksolliseen järjestelmään vuonna 2015.
Hänen tutkimuksensa ovat vielä hyvin tuoreita, mutta jotkut pyrkivät yhdistämään sen muihin ryhmän 13 elementteihin, kuten talliumiin.
Sen tuotanto on Ydinfuusio, käyttämällä isotooppeja 70Zn ja sen atomit 209Bi.
Älä lopeta nyt... Mainoksen jälkeen on muutakin ;)
Nihoniumin ominaisuudet
Symboli: Ei
Atominumero: 113
Atomimassa: välillä 278–286 c.u. (epävirallinen, Iupac)
Sähköinen konfigurointi: [Rn] 7s2 5f14 6d10 7p1
Vakain isotooppi:286Nh (9,5 sekuntia puolikas elämä, joka voi kasvaa 6,3 sekuntia tai laskea 2,7 sekuntia)
Kemiallinen sarja: ryhmä 13, erittäin raskaat elementit
nihoniumin ominaisuudet
Nihonium, symboli Nh ja atominumero 113, oli yksi viimeisistä jaksollisen järjestelmän elementeistä. Sen virallistaminen tapahtui 30. joulukuuta 2015 Kansainvälisen puhtaan ja sovelletun kemian liitossa (IUPAC), kun taas sen nimi tehtiin viralliseksi vasta vuoden 2016 puolivälissä.
Tämän jaksollisen järjestelmän alueen elementit ovat erittäin epävakaita, mikä tarkoittaa, että niitä ei löydy luonnosta. Siten väitetyn olemassaolon edessä ne joutuisivat lähes välittömästi radioaktiiviseen hajoamiseen – ydinhiukkasten, kuten α: n ja β: n, päästöjen saavuttamiseksi suuremman vakauden saavuttamiseksi.
Kuitenkin, kun ne lähettävät ydinhiukkasia, ne päätyvät ydintransmutaatioon, eli niistä tulee uusi kemiallinen alkuaine. Siten superraskaita alkuaineita, kuten Nh, on tuotettava laboratoriossa, mikä tekee siitä a synteettinen kemiallinen alkuaine.
Nh, kuten muutkin erittäin raskaat elementit, vaikuttaa relativistisia vaikutuksia — yksinkertaisella tavalla etäisyydet havaitusta odotettuun suhteellisuusteorian vuoksi. Niinpä teoreettisen alan matemaattiset tutkimukset, jotka simuloivat relativistisen vaikutuksen seurauksia, huomauttivat, että nihonium voisi olla heikosti vuorovaikutuksessa kvartsin kanssa, mutta olla hyvä adsorptio kulta-, kuten sen kevyempi vastine, tallium (Tl).
Alustavat teoreettiset tutkimukset osoittivat myös volatiliteetti alkaen Nh. Mitä tulee adsorptioon kvartsiin, tallium muodostaa helposti esimerkiksi TlOH: ta, ja nihoniumin epäillään tekevän samoin.
Silti kuinka tutkimukset ovat vielä hyvin alustavia ja tuoreita, suuri osa tuotteista on avoin keskustelulle, ja on vaikea määrittää tarkasti nihoniumin fysikaalis-kemiallisia ominaisuuksia.
Nihoniumin hankkiminen
Elementti 113 on tähän päivään asti saatu kahdella tavalla: kautta kylmäfuusioreaktiot, sinkin (Zn, Z = 30) ja vismutin (Bi, Z = 83) fuusiossa sekä myös alkuaineen 115 alfa-hajoaminen.
Ensimmäisessä esimerkissä sinkki nopeutetaan 10 prosenttiin valonnopeus, voittaakseen kahden ytimen hylkivät voimat. Sitten syntyy isotooppi 279Nh, joka päätyy emittoimaan neutronin ja tuottamaan neutronin 278Nh.

Puoliintumisajalla noin 34 millisekuntia, isotooppi 278Nh käy läpi kuusi alfahajoamista (alfahiukkaspäästöt) elementiksi mendeleviumiksi (Md).
Toisessa tapauksessa elementti 113 syntyy elementin 115 (nykyisin muskoviumina) alfahajoamisesta sen syntetisoinnin jälkeen. Yksi tapa on ionien kuumafuusioreaktio 48Ca isotooppien kanssa 243ah, tuottaa 288Mc ja sitten alfahajoamisen kautta 284Nh, joka jatkaa alfahajoamista.
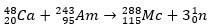
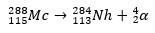
Katso myös: Hassium – raskain synteettinen kemiallinen alkuaine, jonka ominaisuudet on analysoitu
nihoniumin historiaa
Elementin 113 etsinnät aloitettiin vuonna 2003. Japanilaiset tutkijat Riken-instituutissa kiihdyttivät isotooppeja 70Zn 10% valon nopeudella törmätäkseen 209Bi, fuusioreaktion kautta. Siten he onnistuivat tuottamaan sen, mitä me nyt tunnemme 278Nh.
Se tapahtui kuitenkin vasta vuonna 2012 Japanilaiset tutkijat pystyivät havaitsemaan täydellisen alfahajoamissarjan elementistä 113, ottamalla yhteyttä IUPAC: iin löydön vaatimiseksi.
Samanaikaisesti japanilaisten ponnistelujen kanssa venäläiset tiedemiehet Juri Oganessianin johdolla yhteistyössä Amerikkalaiset tutkijat tulivat myös tunnistamaan alkuaineen 113 alkuaineen alfahajoamisen kautta 115. Tällaiset kokeet asettivat myös venäläiset ja amerikkalaiset tutkijat kilpailemaan elementin 113 tunnistamisesta.

IUPAC kuitenkin piti Riken-instituutin todisteita vankempana ja antoi siten japanilaisille oikeuden nimetä elementti 113. Nimeksi valittiin nihônio, symboli Nh viitaten maahan Japani. Japanilaiset kirjoittavat sanan Japan käyttämällä kahta kiinalaista kirjainta, jotka tarkoittavat "nousevan auringon maata", ja niitä luetaan nimellä Nihon tai Nippon.
Nimi nihonium valittiin myös, koska vuonna 1908 japanilainen kemisti Masataka Ogawa julkaisi, että oli löytänyt alkuaineen 43 ja nimesi sen japaniksi, symbolilla Np (joka nykyään kuuluu neptuniumille, Z = 93). Myöhemmin kuitenkin osoitettiin, että elementti 43 oli epästabiili, sitä ei löydetty luonnosta ja se syntetisoitiin vasta vuonna 1937, jolloin se sai nimen teknetium (Tc).
Siten japanilaiset katosivat jaksollisesta järjestelmästä. Kuitenkin vuosia myöhemmin todistettiin, että itse asiassa Ogawa oli löytänyt elementin 75 (nykyisin nimellä renium). Siihen mennessä alkuaine renium oli kuitenkin jo virallisesti löydetty vuonna 1925 ja kastettu.
Ratkaistiin harjoituksia nihoniumilla
Kysymys 1
Nihonium, symboli Nh ja atominumero 113, on kemiallinen alkuaine, jota ei löydy luonnosta sen lyhyen puoliintumisajan vuoksi. Kestävin niistä, 286Nh, on noin 9,5 sekuntia. Tietäen, että puoliintumisaika on aika, joka tarvitaan lajin määrän pudotukseen puoleen, kuinka monta sekuntia kestää, että yllä olevan isotoopin määrä on 1/16 määrästä alkukirjain?
A) 9.5
B) 19
C) 28.5
D) 38
E) 47,5
Resoluutio:
Vaihtoehto D
9,5 sekunnin välein isotoopin määrä putoaa puoleen. Joten 9,5 sekunnin kuluttua sen määrä on puolet alkuperäisestä määrästä. Vielä 9,5 sekuntia, yhteensä 19 sekuntia, määrä putoaa jälleen puoleen ja on 1/4 alkuperäisestä.
28,5 sekunnin kohdalla, toisen puoliintumisajan jälkeen, määrä putoaa jälleen puoleen saavuttaen 1/8 alkuperäisestä määrästä. Lopulta 38 sekunnin kuluttua määrä putoaa jälleen puoleen ja on 1/16 alkuperäisestä määrästä, kuten lausunnossa pyydetään. Tarvittava aika on siis 38 sekuntia.
kysymys 2
Vuonna 2003 alkuaineen 113 etsintä aloitettiin Riken Institutessa Japanissa. Tuolloin tiedemiehet pystyivät tuottamaan 278Nh sinkki- ja vismuttiatomien fuusion kautta.
Kuinka monta neutronia on lainatussa isotoopissa?
A) 113
B) 278
C) 391
D) 170
E) 165
Resoluutio:
Vaihtoehto E
Lukumäärä neutroneja voidaan laskea seuraavasti:
A = Z + n
missä A on numero pasta atomi-, Z on atomiluku ja n on neutronien lukumäärä. Arvot korvaamalla meillä on:
278 = 113 + n
n = 278 - 113
n = 165
Kirjailija: Stefano Araújo Novais
Kemian opettaja