Mitä korkeampi lämpötila, sitä suurempi reaktion nopeus.
Tämä näkyy helposti monissa jokapäiväisen elämämme tilanteissa, kuten seuraavissa esimerkeissä:
- Kun haluamme hidastaa ruoan hajoamisreaktiota, laskemme lämpötilaa asettamalla sen jääkaappiin;

- Jos haluamme nopeuttaa ruoan kypsennysreaktiota, laita se vain kattilaan. paine, joka paineen kasvaessa nostaa myös nestemäisen veden kiehumislämpötilaa, jossa ruoka on;

- Tulipalot ovat yleensä tuhoisia, koska ympäristön lämpötila nousee, mikä lisää palamisreaktion nopeutta;
- Hidastaa metabolisia kemiallisia prosesseja, mikä vähentää aivovaurioiden mahdollisuutta hapen puute, jotkut leikkaukset tehdään alentamalla potilaan ruumiinlämpöä saavuttaen noin 15 ° C;
- Jos laitamme kuohuviinitabletin lasilliseen kuumaa vettä ja toisen lasilliseen kylmää vettä, ensimmäinen liukenee paljon nopeammin.
Mutta mikä selittää lämpötilan suoraan suhteellisen vaikutuksen reaktionopeuteen?
Tämä johtuu siitä, kutenEdellytykset kemiallisten reaktioiden esiintymiselle", Jotta reaktio etenisi, on välttämätöntä täyttää jotkut ehdot, kuten hiukkaset niiden on törmättävä tehokkaasti ja vaadittavan vähimmäisenergian kanssa, jota kutsutaan aktivointienergiaksi.
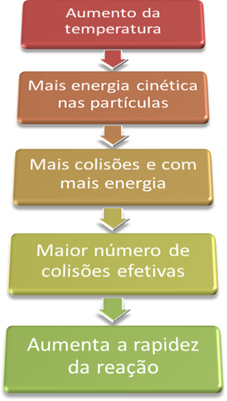
Siten, kun nostamme järjestelmän lämpötilaa, lisäämme myös reagoivien hiukkasten sekoitusta ja annamme niille enemmän kineettistä energiaa. Tämän seurauksena tapahtuu enemmän törmäyksiä ja enemmän energiaa, mikä lisää reagoivien hiukkasten määrää ja siten lisää reaktionopeutta.
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Lähde: Brasilian koulu - https://brasilescola.uol.com.br/quimica/temperatura-velocidade-das-reacoes.htm
