kutsutaan Rutherford malli tiedemies Ernest Rutherfordin vuonna 1911 tekemä ehdotus atomille, jonka tarkoituksena oli osoittaa aineen ideaalin muoto ja koostumus: atomi.
O Rutherford malli Se tunnetaan yleisesti aurinkokunnan mallina, koska sen rakennetta ja toimintaa on verrattu auringon ja sitä ympärillä pyörivien planeettojen väliseen suhteeseen.
Mallissaan Rutherford vertasi aurinkoa atomin ytimeen ja atomin elektroneja aurinkokunnan planeetoihin, kuten seuraavasta esityksestä voidaan nähdä:
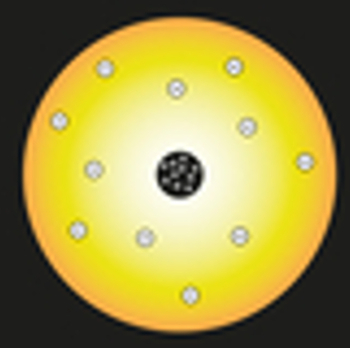
Rutherfordin atomimallin esitys
Ytimen sisällä sijoitettaisiin positiivisesti varautuneita hiukkasia, joita kutsutaan protoneiksi (löytäjä Eugen Goldstein). Tämä ydin olisi pieni ja tiheä ja sillä olisi atomin suurin massa.
Rutherfordin suorittama kokeilu
Kaikki Rutherfordin ehdotukset hänen atomimallinsa luomiseksi olivat tulosta kokeesta, jossa hän fokusoi alfasäteilyn säteet (alkuperäinen lyijylaatikossa olevaa radioaktiivista poloniumia) ohuella kultalevyllä, jonka takana ja sivuilla on sinkkisulfidilla peitetty metallilevy. sivut. Sinkkisulfidi on suola, joka säteilyä vastaanottaessaan loistaa.
Rutherford totesi sitten, että erityisesti kolme pistettä (a, b, c) hehkuivat tämän kokeen aikana:
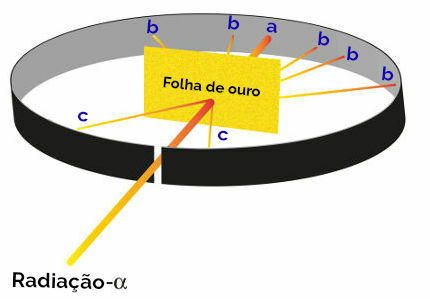
Rutherfordin kokeen esitys
-
kohta a (suurempi kiilto): osoitti, että alfa-säteily ylitti kultalevyn ilman ongelmia, koska se olisi lyijylohkon avautumisreiän suuntaan;
Älä lopeta nyt... Mainonnan jälkeen on muutakin ;)
kohta b (pieni hehkun esiintyvyys): osoitti, että alfasäteily ylitti kultalevyn, mutta että se olisi poikennut ylityksen aikana;
kohta c (erittäin pieni määrä hehkua): sijaitsee kultaterän edessä, osoitti, että alfasäteily ei kulkenut läpi.
Rutherford katsoi, että nämä havaitut tulokset johtuvat atomeista, jotka muodostavat kultalevyn, tulkitseen näin:
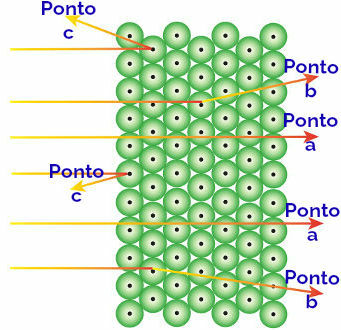
Esitys alfasäteilyn ja atomien käyttäytymisestä
Alfa-säteily saavuttaa osoittaa: alfasäteily on positiivista ja kulkee valtavien tyhjien tilojen atomin alueen läpi. Joillakin kiertoradoilla on myös elektroneja.
Alfa-säteily saavuttaa kohta b: alfasäteily kulkee kultalevyn atomien läpi, mutta saavuttaa tietyn hetken, jolloin se kulkee lähellä atomin pientä ydintä, joka on positiivisesti varautunut ja synnyttää hylkimisen säteilyä.
Alfa-säteily saavuttaa kohta c: alfasäteily kulkee kultalevyn atomien läpi, mutta osuu pieneen ytimeen, joka on positiivisesti varautunut ja synnyttää säteilyssä hylkimistä.
Rutherford-mallin ongelmat
Monet fyysikot huomauttivat joitakin ongelmia Rutherfordin ehdottamassa mallissa:
Ensimmäinen ongelma: kuinka positiivisesti varautunut ydin olisi mahdollinen, jos positiivisesti varautuneet hiukkaset hylkivät toisiaan?
Toinen ongelma: miksi ytimessä olevat protonit eivät vedä puoleensa sähköpallojen elektroneja?
3. ongelma: miksi elektronit, jotka ovat jatkuvasti liikkuvia pieniä kappaleita, eivät menetä energiaa ja putoa ytimeen?
* Kuvien tekijät: Svic / Shutterstock
Kirjailija: Me. Diogo Lopes Dias
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
PÄIVÄT, Diogo Lopes. "Mikä on Rutherfordin malli?"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-modelo-rutherford.htm. Käytetty 27.7.2021.

