Reaktiot lisäys ovat tärkeitä toimia orgaanisten synteesien kannalta, koska niiden kautta voidaan kehittää mielenkiintoinen määrä orgaanisia aineita.
Jotta additioreaktio tapahtuisi, on välttämätöntä luoda kaksi sitoutumiskohtaa hiiliketjuun, mikä tapahtuu yksinkertaisesti, kun ketju on tyydyttymätön (läsnäolo pi linkki). Siten, kun pi-linkki katkeaa, sivustot ilmestyvät ketjuun.
Ryhmä aineita, joita voidaan käyttää synteesin lisäksi, ovat sykloalkaanit tai syklaaneja, hiilivetyjen ryhmä syklisillä ja tyydyttyneillä ketjuilla. Ne välttyvät yleisen summaussäännön noudattamisesta, koska niillä ei ole pi-linkkiä, mutta ne ovat tietyistä ehdoista riippuen (lämpö, katalyyttimetalli, hapan väliaine) ne voivat läpikäydä ketjun katkeamisen kahden hiiliatomin välillä, jolloin kaksi sitoutumiskohtaa ilmaantuu lisäyksen tapahtumista varten. On kuitenkin olemassa tosiasia, joka rajoittaa näiden yhdisteiden käyttöä. Tosiasia on kutsu rengasjännitysteoria, ehdotti Adolf V. Bayer vuonna 1885.
Jotta hiilten välinen sigma-sidos katkeaisi, hiilen välillä on oltava tietty epävakaus. Tämä epävakaus liittyy hiilen välisten sidosten kulmaan. Bayerin mukaan kulma, joka tarjoaa a
suuri vakaus sigma-linkkiä varten on 109,47O. Siten ketjut, joiden hiilen välinen kulma on pienempi kuin 109,47O niillä on taipumus olla epävakaita sigmasidoksissa ketjujen muodostavien hiilen välillä, mikä suosii niiden katkeamista ihanteellisen ulkoisen tilan yhteydessä.Ainoat sykloalkaanit, joiden kulma on pienempi kuin 109,47O sen hiilien joukossa ovat syklopropaani (60O), syklobutaani (90O) ja syklopentaani (108O). Syklopentaanin kulma on hyvin lähellä 109,47O siinä on erittäin stabiilit sigmasidokset, joten se ei voi käydä läpi mitään additioreaktiota. Alla on näiden kolmen sykloalkaanin rakenteet:

Syklopropaanin, syklobutaanin ja syklopentaanin rakennekaava, vastaavasti
Havainto: Mikä tahansa sykloalkaani, jonka ketjussa on enemmän kuin 5 hiiltä, suorittaa substituutioreaktion esimerkki, eikä koskaan lisäystä, koska niiden hiiliatomien väliset sigmasidokset ovat äärimmäisiä vakaa.
Lisäysreaktiot, joita sykloalkaanien kanssa voi tapahtua, ovat periaatteessa kaikki, mutta syklopentaanin kanssa ainoat reaktiot, jotka se voi käydä läpi, ovat hydraus ja halogenointi. Alla on esimerkkejä lisäyksistä sykloalkaaneilla ja niiden esiintymisolosuhteista:
a) Hydraus
Sykloalkaanin reaktio vetymolekyylin kanssa jauhemaisen metallikatalyytin (sinkki, nikkeli tai platina) läsnä ollessa lämmityksen (noin 180 °C) läsnä ollessaOÇ). Tässä reaktiossa sykloalkaani saa aikaan a alkaani. Tässä reaktiossa, kun sykli on katkennut, yksi vetyatomi lisätään kuhunkin katkenneen sigmasidoksen hiileen.
Älä lopeta nyt... Mainonnan jälkeen on muutakin ;)

Lisäysreaktio syklobutaanissa käyttäen vetyä
b) Halogenointi
Sykloalkaanin reaktio halogeenimolekyylin (esim. kloori, bromi, jodi) kanssa rauta III -kloridi-katalyytin (FeCl) kanssa3). Tässä reaktiossa sykloalkaani saa aikaan a orgaaninen halogenidi jossa on kaksi halogeeniatomia ketjussa. Kun sykli on katkennut, meillä on lisätty halogeeniatomi jokaiseen katkenneen sigma-sidoksen hiileen.

Lisäysreaktio syklobutaanissa käyttäen bromia
c) Reaktio halogeenihydridien (happohalogenidien) kanssa
Sykloalkaanin reaktio halogeenia sisältävän epäorgaanisen hydraattimolekyylin (HCl. HBr, HI) kanssa. Koska happoa käytetään lähtöaineena, katalyyttiä ei käytetä. Tässä reaktiossa sykloalkaani saa aikaan a orgaaninen halogenidi vain yksi halogeeniatomi ketjussa. Kun sykli on katkennut, meillä on lisätty vetyatomi yhteen katkenneen sigmasidoksen hiilestä ja halogeeni toiseen hiileen. Markovnikovin sääntöä noudattaen (H eniten hydratulla hiilellä ja halogeeni vähiten hydratulla hiilellä).
Huomautus: Sitä esiintyy vain syklopropaanin ja syklobutaanin kanssa.
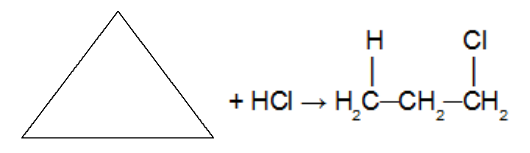
Lisäysreaktio syklopropaanissa käyttäen suolahappoa
Huomautus: Sitä esiintyy vain syklopropaanin ja syklobutaanin kanssa.
d) Nesteytys
Sykloalkaanin reaktio vesimolekyylin kanssa rikkihapon läsnä ollessa ja kuumennus. Tässä reaktiossa sykloalkaani saa aikaan a monoalkoholi (alkoholi, jonka ketjussa on vain yksi OH-ryhmä). Kun sykli on katkennut, meillä on lisätty vetyatomi yhteen katkenneen sigmasidoksen hiilestä ja hydroksyyli (OH) toiseen hiileen. Markovnikovin sääntöä noudattaen (H eniten hydratulla hiilellä ja hydroksyyli vähiten hydratulla hiilellä).
Huomautus: Sitä esiintyy vain syklopropaanin ja syklobutaanin kanssa.

Lisäysreaktio syklopropaanissa käyttäen suolahappoa
Kirjailija: Me. Diogo Lopes Dias
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
PÄIVÄT, Diogo Lopes. "Lisäykset syklaaneissa"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/adicoes-ciclanos.htm. Käytetty 27.7.2021.
Kemia

Hydroksyylifunktionaalinen ryhmä, primaariset alkoholit, sekundaariset alkoholit, tertiääriset alkoholit, metanoli, glyseroli, etanoli, nitroglyseriinin valmistus, maalien valmistus, alkoholijuomien valmistus, etikkahappo, polttoaine autot.


