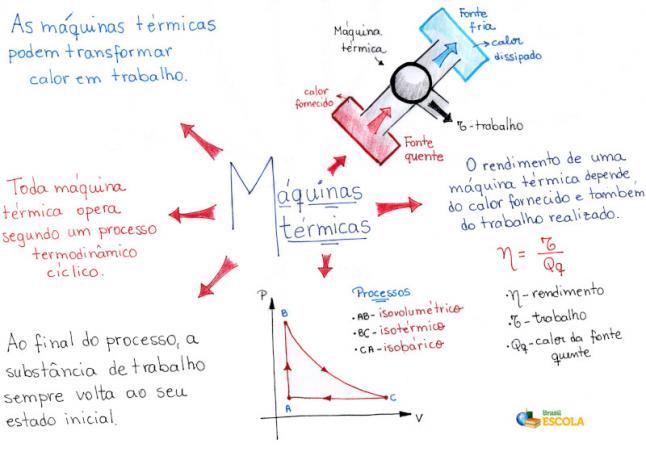
Termodynamiikka on fysiikan alue, joka tutkii energiansiirtoja. Se pyrkii ymmärtämään lämmön, energian ja työn väliset suhteet, analysoimalla vaihdetun lämmön määrän ja fyysisessä prosessissa suoritetun työn.
Termodynaamisen tieteen kehitti alun perin tutkijat, jotka etsivät tapaa parantaa koneita teollisen vallankumouksen aikana parantamalla niiden tehokkuutta.
Tätä tietoa käytetään tällä hetkellä jokapäiväisen elämämme eri tilanteissa. Esimerkiksi: lämpökoneet ja jääkaapit, automoottorit ja prosessit mineraalien ja öljytuotteiden muuntamiseksi.
Termodynamiikan lait
Termodynamiikan perustavat lait säätelevät sitä, kuinka lämmöstä tulee työtä, ja päinvastoin.
Ensimmäinen termodynamiikan laki
THE Ensimmäinen termodynamiikan laki liittyy energiansäästön periaate. Tämä tarkoittaa, että energiaa järjestelmässä ei voida tuhota tai luoda, vain muuttaa.
Termodynamiikan ensimmäistä lakia edustava kaava on seuraava:

Lämmön määrällä, työllä ja sisäisen energian vaihtelulla on vakio mittayksikkö Joule (J).
Käytännön esimerkki energiansäästöstä on, kun henkilö käyttää pumppua puhallettavan esineen täyttämiseen, ja hän käyttää voimaa pumppaamaan ilmaa esineeseen. Tämä tarkoittaa, että liike-energia saa männän laskemaan. Osa energiasta muuttuu kuitenkin lämmöksi, joka häviää ympäristölle.
THE Hessin laki on erityinen tapaus energiansäästön periaatteesta. Tietää enemmän!
Toinen termodynamiikan laki
Klo lämmönsiirrot niitä esiintyy aina lämpimimmästä kehosta kylmimpään, se tapahtuu spontaanisti, mutta ei päinvastoin. Toisin sanoen lämpöenergiansiirtoprosessit ovat peruuttamattomia.
Niinpä Toinen termodynamiikan laki, ei ole mahdollista, että lämpö muuttuu täysin muuksi energiamuodoksi. Tästä syystä lämpöä pidetään huonontuneena energiamuotona.

Termodynamiikan toiseen lakiin liittyvä fyysinen määrä on haje, joka vastaa järjestelmän häiriötasoa.
Lue myös:
- Carnot-sykli
- Lämpölaajeneminen
Termodynamiikan nolla laki
THE Termodynamiikan nolla laki käsittelee ehtoja terminen tasapaino. Näistä olosuhteista voidaan mainita sellaisten materiaalien vaikutus, jotka tekevät lämmönjohtavuudesta korkeamman tai pienemmän.
Tämän lain mukaan
- jos runko A on termisessä tasapainossa kosketuksessa rungon B ja
- jos tämä runko A on termisessä tasapainossa kosketuksessa rungon C kanssa, niin
- B on termisessä tasapainossa kosketuksissa C: n kanssa.
Kun kaksi elintä, joilla on eri lämpötilat, saatetaan kosketukseen, lämpimämpi siirtää lämmön viileämpään. Tämä saa lämpötilat tasaantumaan terminen tasapaino.
Sitä kutsutaan nollalakiksi, koska sen ymmärtäminen osoittautui tarpeelliseksi kahdelle jo olemassa olevalle laille, ensimmäiselle ja toiselle termodynamiikan laille.
Kolmas termodynamiikan laki
THE Kolmas termodynamiikan laki se näyttää yrittävän luoda absoluuttisen vertailupisteen, joka määrittää entropian. Entropia on itse asiassa termodynamiikan toisen lain perusta.
Sen ehdottanut fyysikko Walther Nernst totesi, että puhtaalla aineella, jonka lämpötila oli nolla, ei ollut mahdollista saada entropiaa likimääräisellä nollan arvolla.
Tästä syystä se on kiistanalainen laki, jota monet fyysikot pitävät pääsääntöisesti eikä lakina.
termodynaamiset järjestelmät
Termodynaamisessa järjestelmässä voi olla yksi tai useampi toisiinsa liittyvä kappale. Ympäröivä ympäristö ja maailmankaikkeus edustavat järjestelmän ulkopuolista ympäristöä. Järjestelmä voidaan määritellä seuraavasti: avoin, suljettu tai eristetty.
 termodynaamiset järjestelmät
termodynaamiset järjestelmät
Kun järjestelmä avataan, massa ja energia siirtyvät järjestelmän ja ulkoisen ympäristön välillä. Suljetussa järjestelmässä tapahtuu vain energiansiirtoa (lämpöä), ja kun se on eristetty, sitä ei tapahdu.
kaasujen käyttäytyminen
Kaasujen mikroskooppinen käyttäytyminen on helpommin kuvattu ja tulkittavissa kuin muissa fysikaalisissa tiloissa (nestemäinen ja kiinteä). Siksi kaasuja käytetään eniten näissä tutkimuksissa.
Termodynaamisissa tutkimuksissa käytetään ihanteellisia tai täydellisiä kaasuja. Se on malli, jossa hiukkaset liikkuvat kaoottisesti ja ovat vuorovaikutuksessa vain törmäyksissä. Lisäksi katsotaan, että nämä hiukkasten, niiden ja säiliön seinämien väliset törmäykset ovat joustavia ja kestävät hyvin lyhyen aikaa.
Suljetussa järjestelmässä ihanteellinen kaasu omaksuu käyttäytymisen, joka sisältää seuraavat fyysiset määrät: paine, tilavuus ja lämpötila. Nämä muuttujat määrittävät kaasun termodynaamisen tilan.
 Kaasujen käyttäytyminen kaasulakien mukaisesti
Kaasujen käyttäytyminen kaasulakien mukaisesti
Paine (p) syntyy kaasupartikkeleiden liikkeestä säiliön sisällä. Säiliön sisällä olevan kaasun käyttämä tila on tilavuus (v). Ja lämpötila (t) liittyy liikkuvien kaasupartikkelien keskimääräiseen kineettiseen energiaan.
Lue myös Kaasulaki ja Kaasujen tutkimus.
sisäinen energia
Järjestelmän sisäinen energia on fyysinen määrä, joka auttaa mittaamaan, kuinka kaasun läpi tapahtuvat muunnokset tapahtuvat. Tämä suuruus liittyy hiukkasten lämpötilan ja kineettisen energian vaihteluun.
Ihanteellisella kaasulla, joka koostuu vain yhdestä atomityypistä, on sisäinen energia, joka on suoraan verrannollinen kaasun lämpötilaan. Tätä kuvaa seuraava kaava:

Ratkaistut harjoitukset termodynamiikasta
Kysymys 1
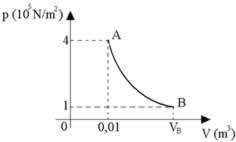
Liikkuvalla männällä varustettu sylinteri sisältää kaasua paineessa 4.0.104N / m2. Kun järjestelmään syötetään 6 kJ lämpöä vakiopaineessa, kaasutilavuus laajenee 1.0.10-1m3. Määritä tässä tilanteessa tehty työ ja muutos sisäisessä energiassa.
Oikea vastaus: tehty työ on 4000 J ja sisäinen energiamuutos 2000 J.
Tiedot:
P = 4,0.104 N / m2
Q = 6KJ tai 6000J
ΔV = 1,0.10-1 m3
T =? ΔU =?
1. vaihe: Laske työ ongelmadatan kanssa.
T = P. ΔV
T = 4,0,104. 1,0.10-1
T = 4000 J
2. vaihe: Laske sisäisen energian vaihtelu uusilla tiedoilla.
Q = T + AU
ΔU = Q - T
ΔU = 6000 - 4000
ΔU = 2000J
Siksi suoritettu työ on 4000 J ja sisäinen energiamuutos 2000 J.
kysymys 2
(Mukautettu ENEM 2011: stä) Moottori voi työskennellä vain, jos se saa paljon energiaa toisesta järjestelmästä. Tällöin polttoaineeseen varastoitu energia vapautuu osittain palamisen aikana, jotta laite voi toimia. Kun moottori käy, osaa palamisen aikana muunnetusta tai muunnetusta energiasta ei voida käyttää työn tekemiseen. Tämä tarkoittaa, että energiaa vuotaa toisessa muodossa.
Tekstin mukaan moottorin käytön aikana tapahtuvat energiamuutokset johtuvat:
a) lämmön vapautuminen moottorin sisällä on mahdotonta.
b) moottorin suorittama työ on hallitsematonta.
c) lämmön muuntaminen työhön on mahdotonta.
d) lämpöenergian muuttuminen kinetiikaksi on mahdotonta.
e) polttoaineen mahdollista energiankulutusta ei voida hallita.
Oikea vaihtoehto: c) lämmön muuntaminen työhön on mahdotonta.
Kuten aikaisemmin nähtiin, lämpöä ei voida täysin muuttaa työksi. Moottorin käytön aikana osa lämpöenergiasta menetetään ja siirtyy ulkoiseen ympäristöön.
Katso myös: Harjoituksia termodynamiikasta