Kemia on biologian ja fysiikan ohella osa luonnontieteitä ja sen tekniikkaa.
Kolmen oppiaineen kesken on jaettu 45 kysymystä, joita sovelletaan testin toisena päivänä matematiikan ja sen tekniikoiden kanssa.
Enemissä eniten tutkitaan kemian aloja: yleiskemia, fysikaalinen kemia, orgaaninen kemia ja ympäristökemia.
Kysymysten lausunnot on kontekstualisoitu tapa yhdistää osaamisalueet arjen asioihin.
Enemissä eniten kuuluvia kemian aiheita
Jotta testi sujuisi hyvin, sinun on luettava kysymykset huolellisesti, tulkittava tiedot ja liitettävä ne tutkittaviin käsitteisiin.
Testin kemiallinen sisältö kattaa pääyhdisteet, niiden ominaisuudet, niitä luonnehtivat kemialliset toiminnot ja reaktiot, joita ne voivat tehdä.

Reaktioiden kvantifioimiseksi tarvitaan laskelmia, ja käytetyt esimerkit ovat jokapäiväisiä asioita; olipa kyseessä merkityksellisen kemiallisen yhdisteen tuotantoprosessi tai jopa käyttö muilla aloilla, kuten fossiilinen dataus.
Seuraavassa kuvataan vaativimmat aiheet ja mitä niistä tulisi tutkia.
Yleinen kemia
Yleinen kemia esittelee kemian alan tutkimusten evoluution, laadulliset suhteet ja kvantitatiiviset reaktiot ja sellaisten käsitteiden ja termien käyttöönotto, jotka ovat perusta muiden ymmärtämiselle alueilla.
Periaatteessa tämä haara kattaa kemian periaatteet aineen koostumuksen, ominaisuuksien ja reaktiivisuuden ymmärtämiseksi.

THE Yleinen kemia Enemissä tutkia lisää:
| Teema | Pääaiheet |
|---|---|
| Jaksollinen järjestelmä | Kemialliset alkuaineet ja niiden organisointi, aineosien luokittelu ja aineen ominaisuudet. |
| Jaksolliset ominaisuudet | |
| Seokset | Saatujen seosten tyypit, pääerotusmenetelmät ja jakeet. |
| erotustekniikat | |
| Stökiometria | Kemialliset saannon ja puhtauden laskelmat. |
| Stökiometriset laskelmat | |
| Kemialliset sidokset | Kuinka atomit yhdistyvät muodostaen erilaisia aineita ja vuorovaikutusta molekyylien välillä. |
| molekyylien väliset voimat | |
| Molekyyligeometria | Tärkeimpien yhdisteiden ominaisuudet. |
| Liukoisuus |
Yleinen kemian kysymys
(Enem / 2018) Kreikkalaisessa mytologiassa Niobia oli Tantaloksen tytär, kaksi kärsimyksestään tunnettua hahmoa. Kemiallisella elementillä, jonka atominumero (Z) on 41, on kemialliset ja fysikaaliset ominaisuudet, jotka ovat niin samanlaisia kuin alkuaineen, joiden atominumero on 73, että ne sekoittuivat.
Siksi näiden kahden hahmon kunniaksi kreikkalaisessa mytologiassa näille elementeille annettiin niobiumin (Z = 41) ja tantaalin (Z = 73) nimet. Nämä kaksi kemiallista alkuaineita ovat saaneet suuren taloudellisen merkityksen metallurgiassa, metallin valmistuksessa suprajohteissa ja muissa huippuluokan teollisuuden sovelluksissa nimenomaan kemiallisten ja fysikaalisten ominaisuuksiensa vuoksi molemmille yhteisiä.
KEAN, S. Katoava lusikka: ja muita todellisia tarinoita hulluudesta, rakkaudesta ja kuolemasta kemiallisista alkuaineista. Rio de Janeiro: Zahar, 2011 (mukautettu).
Näiden alkuaineiden taloudellinen ja tekninen merkitys johtuu niiden kemiallisten ja fysikaalisten ominaisuuksien samankaltaisuudesta
a) elektronien on oltava alatasolla f.
b) olla sisäisen siirtymän elementtejä.
c) kuuluvat samaan ryhmään jaksollisessa taulukossa.
d) uloimpien elektroniensa tasot 4 ja 5, vastaavasti.
e) sijaittava maa-alkalimetalli- ja emäksisissä perheissä.
Oikea vaihtoehto: c) kuuluvat samaan ryhmään jaksollisessa taulukossa.
Jaksotaulukko on jaettu 18 ryhmään (perheeseen), joissa jokainen ryhmä yhdistää kemialliset alkuaineet, joilla on samanlaiset ominaisuudet.
Nämä yhtäläisyydet tapahtuvat, koska ryhmän elementeillä on sama määrä elektroneja valenssikuoressa. Niobiumin ja tantaalin sähköinen jakelu meillä on:
| Elementti | Eletroninen jakautuminen | elektronien summa |
Ryhmä |
| Niobium (41) | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d3 | 4d3 + 5 sekuntia2= 5 elektronia | 5 |
| Tantaali (73) | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d3 | 5d3 + 6 s2 = 5 elektronia | 5 |
Elementit niobium ja tantaali kuuluvat jaksollisen taulukon ryhmään 5, vastaavasti 5. ja 6. jaksossa.
Lue myös: Niobium ja Jaksolliset taulukot.
Tämän kysymyksen ratkaiseminen edellyttää tietoa ryhmän (perheen) määritelmästä jaksollisessa taulukossa.
Siksi on erittäin tärkeää opiskella käsitteiden korjaamiseksi, se auttaa sinua tulkitsemaan kysymyksiä ja helpottamaan ratkaisua.
Fysikaalis-kemiallinen
Järjestelmien ominaisuudet tulkitaan fysikaalisten ja kemiallisten ominaisuuksien havainnoinnilla.
Kemiallisten muunnosten energiaa ja dynamiikkaa tutkitaan tällä kemian alalla.

THE Fyysinen kemia Enemissä tutkia lisää:
| Teema | Pääaiheet |
|---|---|
| Ratkaisut | Laske liuosten pitoisuus (molaarinen, tavallinen, PPM ja prosenttiosuus). |
| Sähkökemia | Erota katodi ja anodi, vertaa tavanomaisia pelkistyspotentiaaleja, hapetus- ja pelkistysreaktioita, korroosioilmiötä, akkua ja elektrolyysiä. |
| lämpökemia | Laske energiamuutos, reaktion entalpian käsite ja Hessin laki. |
| Hapot ja emäkset | Laske pH ja neutralointireaktio. |
| Kemiallinen tasapaino | Yleiset käsitteet, tasapainovakio ja tasapainosiirtymä. |
| Le Chatelierin periaate | |
| Radioaktiivisuus | puoliintumisaika, fissio ja ydinfuusio. |
Fysikaalisen kemian kysymys
(Enem / 2009) Analysoi luku.
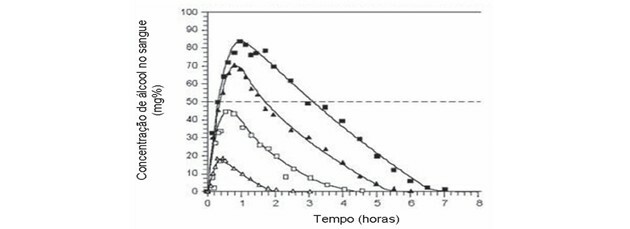
Saatavilla osoitteessa: http:// www.alcoologia.net. Pääsy: 15. heinäkuuta 2009 (mukautettu).
Olettaen, että tälle luvulle on annettava otsikko, vaihtoehto, joka parhaiten kääntäisi edustetun prosessin, olisi:
a) Keskimääräinen veren alkoholipitoisuus koko päivän ajan.
b) Alkoholin saannin tiheyden vaihtelu tuntien aikana.
c) Pienin veren alkoholipitoisuus eri annoksilla.
d) Arvio eri alkoholimäärien metaboloitumiseen tarvittavasta ajasta.
e) Graafinen esitys alkoholin taajuusjakaumasta tiettynä vuorokaudenaikana.
Oikea vaihtoehto: d) Arvio eri alkoholimäärien metaboloitumiseen tarvittavasta ajasta.
Kaaviossa on esitetty neljä käyrää, joilla on erilaiset veren alkoholipitoisuudet ja ne liittyvät aikaan.
On havaittu, että riippuen alkoholin pitoisuudesta veressä, eri aikoja tarvitaan pitoisuuden laskemiseksi verenkierrossa.
Tämä väheneminen johtuu siitä, että alkoholi ja muut nauttimamme aineet metaboloituvat kehossamme muuttamalla ne pienemmiksi aineiksi, jotka imeytyvät.
Kaaviot ovat yksi tapa, jolla Enem esittää tietoja ja arvioi ehdokkaan tulkkauskykyä. Siksi on tärkeää työskennellä edellisten kokeiden läpi ja tutustua kokeen esittämiin kysymyksiin.
Orgaaninen kemia
Huomaten, että kaikkien elävistä lähteistä peräisin olevien yhdisteiden rakenteessa oli alkuaine hiiltä, tämä merkittävä tosiasia johti määritelmään, että orgaaninen kemia on tutkimus yhdisteistä hiili.
Kokeita suorittamalla Friedrich Wöhler onnistui syntetisoimaan ureaa ammoniumsyanaatista eli orgaanisesta aineesta epäorgaanisesta yhdisteestä.
Siitä lähtien miljoonia yhdisteitä on keinotekoisesti saatu mineraalireagensseista ja yksinkertaisemmista luonnollisen alkuperän lähteistä.
Orgaanisten yhdisteiden lukemattoman määrän vuoksi tämä on Enemissä hyvin toistuva teema.
THE Orgaaninen kemia Enemissä tutkia lisää:
| Teema | Pääaiheet |
|---|---|
| Hiili | Hiilen ominaisuudet ja ominaisuudet. |
| Orgaaniset toiminnot | Tärkeimmät orgaaniset toiminnot ja yhdisteet. |
| Nimikkeistö | Hiiliketjujen nimikkeistö ja hiililuokitus. |
| Isomeria | Erota orgaaniset rakenteet isomerismin tyypin mukaan. |
| orgaaniset reaktiot | Tärkeimmät orgaaniset reaktiot. |
Orgaanisen kemian kysymys
(Enem / 2014) Vanilja eräänlaiseen orkideaan. Sen kukasta tuotetaan vanilliinia (kemiallisen esityksen mukaan), mikä saa aikaan vaniljaaromin.
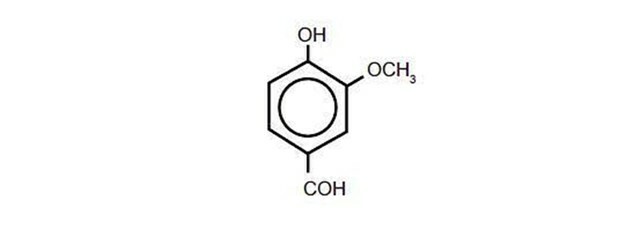
Vanilliinissa orgaaniset toiminnot ovat läsnä
a) aldehydi, eetteri ja fenoli.
b) alkoholi, aldehydi ja eetteri.
c) alkoholi, ketoni ja fenoli.
d) aldehydi, ketoni ja fenoli.
e) karboksyylihappo, aldehydi ja eetteri.
Oikea vaihtoehto: a) aldehydi, eetteri ja fenoli.
| orgaaninen toiminta | Edustus |
| Aldehydi | R — COH |
| Eetteri | R - O - R ' |
| Fenoli | Air-OH |
Muut orgaaniset toiminnot, jotka näkyvät muissa vaihtoehdoissa, ovat:
| Alkoholi | R-OH |
| ketoni | |
| karboksyylihappo | R-COOH |
Tässä kysymyksessä ruoanlaitossa laajalti käytetty aromi esitettiin kontekstina orgaanisten toimintojen tuntemuksen arvioimiseksi.
On tavallista, että kysymykset liittyvät yhdisteiden nimikkeistöön ja pyytävät niiden rakennetta tai päinvastoin.
Siksi on tärkeää tutkia tärkeimmät orgaaniset toiminnot ja niiden väliset erot.
Ympäristökemia
Pitkän ajan tekninen kehitys tapahtui ilman asianmukaista huomiota ympäristöön. Ajan myötä ihmisen toiminnan, lähinnä teollisen, tulokset alkoivat näkyä. Esimerkkejä tästä ovat happosateet ja kasvihuoneilmiö.
Vihreän kemian käsitettä on tutkittu paitsi uudeksi poluksi myös keinona edistää yhteiskunnan tottumusten muutos ja edistyminen vähemmän vaarallisten ja ympäristölle haitallisten aineiden kanssa.

THE Ympäristökemia Enemissä tutkitaan tekniikan, yhteiskunnan ja ympäristön suhdetta.
On tavallista kohdata asioita, jotka raportoivat:
| Teema | Pääaiheet |
|---|---|
| Saastuminen | Saastumistyypit: radioaktiivinen, ilma, vesi ja maaperä. |
| Biogeokemialliset syklit | Typen ja hiilen kierto sekä muutokset. |
| Kasvihuoneilmiö | Syyt, tärkeimmät kasvihuonekaasut ja ilmaston lämpeneminen. |
| Hapan sade | Syyt ja seuraukset. |
| Ilmastonmuutokset | Syyt ja seuraukset. |
| Fossiiliset polttoaineet | Uusiutuvien energialähteiden alkuperä, tyypit ja vaihtoehdot. |
Ympäristökemian kysymys
(Enem / 2010) Yksi suurimmista vesilähteiden (jokien, purojen ja muiden) pilaantumisongelmista on - tapana heittää paistamiseen käytetty öljy putkijohtoihin, jotka ovat yhteydessä toisiinsa Viemäri. Jos näin tapahtuu, jokainen 10 litraa öljyä voi saastuttaa 10 miljoonaa (107) litraa juomavettä.
Tarran käyttöopas. Erottamaton osa Veja-lehtiä (toim. 2055), Claudia (toim. 555), National Geographic (toim. 93) ja Uusi koulu (toim. 208) (mukautettu).
Oletetaan, että kaikki kaupungin kotitaloudet hävittävät paistoöljyt putkistojen kautta ja kuluttavat 1000 litraa paistoöljyä viikossa.
Mikä on litraina saastuneen juomaveden määrä viikossa tässä kaupungissa?
a) 102
b) 103
c) 104
d) 106
e) 109
Oikea vaihtoehto: e) 109
Kolmen säännön avulla voimme löytää arvon, joka perustuu kolmeen annettuun tietoon.
Kysymyksen tiedot ovat:
- 10 l öljyä
- 107 L juomavettä
- 1000 l öljyä
Näillä numeroilla voimme löytää tuntemattoman määrän seuraavasti:
10 litraa öljyä voi saastuttaa 107 litraa juomavettä, 1000 litran öljyn kulutus viikossa voi aiheuttaa 109 litraa.
Joten näemme, että tulokset ovat suhteellisia: mitä enemmän öljyä heitetään pois, sitä enemmän juomavettä voi saastua.
Kodeistamme lähtevä vesi menee jätevedenpuhdistamoihin (ETE). Läsnä olevat öljyjäämät tekevät saapuneiden roskien ja jälkien poistamisprosessista entistäkin vaikeammaksi jokien, purojen ja muiden kohdalla ne kerääntyvät veden pinnalle estäen auringonvalon ja happi.
Planeetallamme olevasta vedestä alle 1% esiintyy jokissa ja järvissä. Siksi on tärkeää olla tietoinen veden pilaantumisen muodoista ja säilyttää vesivaramme.
Uskomme, että nämä tekstit ovat erittäin hyödyllisiä valmistauduttaessa tenttiin.:
- Kemian ongelmat, jotka putosivat Enemiin
- Enemiin kaatuvat aiheet
- Simuloitu vihollinen: testiin jääneet kysymykset
- Enem-kysymykset: testiin kuuluneet kysymykset
- Uutiset, jotka voivat pudota Enemiin ja pääsykokeisiin



