Kemiallisten alkuaineiden jaksolliset ominaisuudet ovat niitä ominaisuuksia.
Huomaa, että jaksollisen taulukon kemiallisilla alkuaineilla on erityinen sijainti, joka vaihtelee niiden jaksollisten ominaisuuksien mukaan. Ne on lajiteltu nousevaan järjestykseen atomiluvun mukaan.
Moseleyn lain mukaan:
“Monet alkuaineiden fysikaaliset ja kemialliset ominaisuudet vaihtelevat ajoittain alkuaineiden atomiluvun järjestyksessä..”
Tärkeimmät jaksolliset ominaisuudet
atomisäde
Atomien kokoon nähden tämä ominaisuus määritetään saman elementin kahden atomin ytimien keskipisteiden välisellä etäisyydellä.
Siksi atomisäde vastaa puolta kahden vierekkäisen atomin ytimien välisestä etäisyydestä ilmaistuna seuraavasti:
r = d / 2
Missä:
r: salama
d: ydinvälinen etäisyys
Se mitataan pikometrit (pm). Tämä mittaus on mittarin osaerä:
1 pm = 10-12 m
Jaksollisessa taulukossa atomisäde kasvaa ylhäältä alas pystysuorassa asennossa. Vaakatasossa ne kasvavat oikealta vasemmalle.
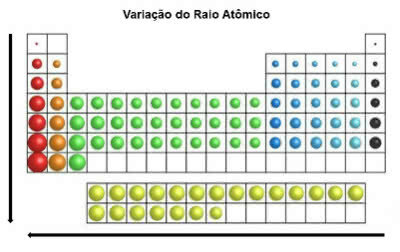
Atomisäteen vaihtelu
Kemiallinen alkuaali, jolla on suurin atomisäde, on cesium (Cs).
Atomic Volume
Tämä jaksollinen ominaisuus osoittaa tilavuuden, jonka kiinteä olomuoto on 1 mol: lla elementistä.
On syytä huomata, että atomitilavuus ei ole yhden atomin tilavuus, vaan joukko 6,02. 1023 atomit (1 mol arvo)
Atomin atomitilavuus määritetään paitsi kunkin atomin tilavuudella myös näiden atomien välisellä etäisyydellä.
Jaksollisessa taulukossa atomimäärät kasvavat ylhäältä alas (pystysuora) ja keskeltä reunalle (vaaka).

Atomisen tilavuuden vaihtelu
Atomitilavuuden laskemiseen käytetään seuraavaa kaavaa:
V = m / d
Missä:
V: atomitilavuus
m: massa 6,02. 1023 alkuaineatomit
d: kiinteän tilan elementtien tiheys
Absoluuttinen tiheys
THE tiheys absoluuttinen, jota kutsutaan myös ”ominaismassaksi”, on jaksottainen ominaisuus, joka määrittää aineen massan (m) ja kyseisen massan käyttämän tilavuuden (v) välisen suhteen.
Se lasketaan seuraavalla kaavalla:
d = m / v
Missä:
d: tiheys
m: pasta
v: äänenvoimakkuus
Jaksollisessa taulukossa tiheysarvot kasvavat ylhäältä alas (pystysuora) ja reunoilta keskelle (vaaka).
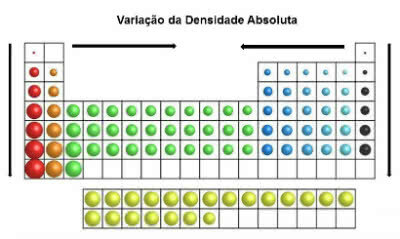
Absoluuttisen tiheyden vaihtelu
Tiheimmät elementit ovat siis taulukon keskellä ja alareunassa:
Osmium (Os): d = 22,5 g / cm3
Iridium (Ir): d = 22,4 g / cm3
Sulamispiste ja kiehumispiste
Toinen tärkeä jaksollinen ominaisuus liittyy lämpötiloihin, joihin alkuaineet pääsevät sulaminen ja kiehuminen.
Sulamispiste (MP) on lämpötila, jossa aine siirtyy kiinteästä aineesta nestefaasiin. Kiehumispiste (PE) on lämpötila, jossa aine siirtyy nesteestä kaasumaiseen faasiin.
Jaksollisessa taulukossa PF: n ja PE: n arvot vaihtelevat taulukossa olevien sivujen mukaan.
Pystysuunnassa ja pöydän vasemmalla puolella ne kasvavat alhaalta ylös. Oikealla puolella ne kasvavat ylhäältä alas. Vaakasuunnassa ne ulottuvat päistä keskustaan.

Sulamis- ja kiehumispisteen vaihtelu
Sähköinen suhde
Kutsutaan myös "elektroaffiniteetiksi", se on pienin energia, jota kemiallinen alkuaine tarvitsee elektronin poistamiseksi anionista.
Tuo on sähköinen suhde ilmaisee vapautuneen energian määrän, kun atomi vastaanottaa elektronin.
Huomaa, että tämä epävakaa atomi on yksin ja kaasumaisessa tilassa. Tällä ominaisuudella se saavuttaa vakauden, kun se vastaanottaa elektronin.
Toisin kuin atomisäde, jaksollisen järjestelmän elementtien elektroafiinisuus kasvaa vasemmalta oikealle vaakasuunnassa. Pystysuunnassa se kasvaa alhaalta ylös.
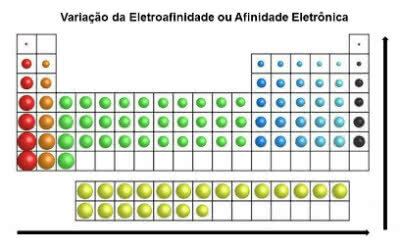
Elektroninen suhde-vaihtelu
Kemiallinen alkuaine, jolla on suurin elektroniaffiniteetti, on kloori (Cl), jonka arvo on 349 KJ / mol.
Ionisointienergia
Kutsutaan myös "ionisaatiopotentiaali”, Tämä ominaisuus on elektronisen affiniteetin vastainen.
Se on vähimmäisenergia, jota kemiallinen alkuaine tarvitsee elektronin poistamiseksi neutraalista atomista.
Siten tämä jaksollinen ominaisuus osoittaa, kuinka paljon energiaa tarvitaan elektronin siirtämiseen perustilassa olevasta atomista.
Niin kutsuttu "atomin perustila" tarkoittaa, että sen protonien lukumäärä on yhtä suuri kuin elektronien lukumäärä (s+ = ja-).
Siten, kun elektroni on poistettu atomista, se ionisoidaan. Toisin sanoen se saa enemmän protoneja kuin elektroneja, ja siksi siitä tulee kationi.
Jaksollisessa taulukossa ionisaatioenergia on ristiriidassa atomisäteen energian kanssa. Joten se kasvaa vasemmalta oikealle ja alhaalta ylös.
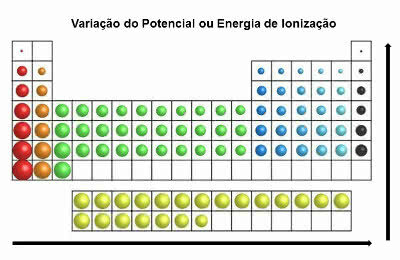
Ionisointienergian vaihtelu
Elementit, joilla on suurin ionisaatiopotentiaali, ovat fluori (F) ja kloori (Cl).
elektronegatiivisuus
Niiden alkioiden atomien ominaisuus, joilla on taipumus vastaanottaa elektroneja kemiallisessa sidoksessa.
Se tapahtuu kovalenttisissa sidoksissa elektroniparien jakamisen aikana. Vastaanottaessaan elektroneja atomiin jää negatiivinen varaus (anioni).
Muista, että tätä pidetään jaksollisen järjestelmän tärkeimpänä ominaisuutena. Tämä johtuu siitä, että elektronegatiivisuus indusoi atomien käyttäytymistä, joista molekyylit muodostuvat.
Jaksollisessa taulukossa elektronegatiivisuus kasvaa vasemmalta oikealle (vaakasuunnassa) ja alhaalta ylös (pystysuora)
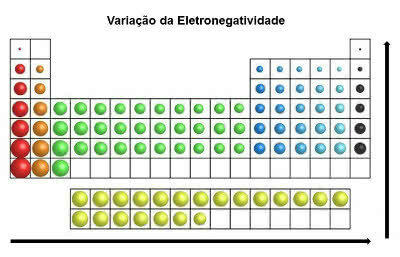
Elektronegatiivisuuden vaihtelu
Siten jaksollisen järjestelmän elektronegatiivisin elementti on fluori (F). Toisaalta, cesium (Cs) ja Francium (Fr) ovat vähiten elektronegatiivisia elementtejä.
sähköpositiivisuus
Toisin kuin elektronegatiivisuus, tämä alkuaatomien ominaisuus osoittaa taipumusta menettää (tai luovuttaa) elektroneja kemiallisessa sidoksessa.
Menetettäessä elektroneja alkioiden atomit saavat positiivisen varauksen muodostaen siten kationin.
Samassa suunnassa kuin atomisäde ja toisin kuin elektronegatiivisuus, jaksollisessa taulukossa a sähköpositiivisuus kasvaa oikealta vasemmalle (vaaka) ja ylhäältä alas (pystysuora).
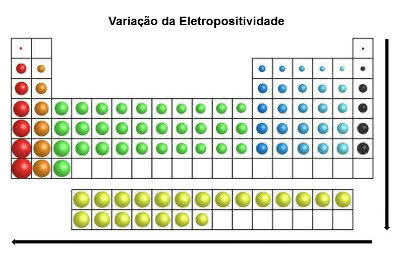
Sähköpositiivisuuden vaihtelu
Kemialliset alkuaineet, joilla on korkein sähköpositiivisuus, ovat metalleja, ja tästä syystä tätä ominaisuutta kutsutaan myös "metalliseksi luonteeksi". Elektropositiivisin alkuaine on frangiumi (Fr), jolla on suurin taipumus hapettumiseen.
Huomio!
Sinä "jalokaasut”Ovat inerttejä alkuaineita, koska ne eivät sitoudu kemiallisiin sidoksiin ja tuskin luovuttavat tai vastaanottavat elektroneja. Heillä on myös vaikeuksia reagoida muiden elementtien kanssa.
Siksi näiden elementtien elektronegatiivisuutta ja sähköpositiivisuutta ei oteta huomioon.
Lue myös:
- Kemialliset sidokset
- Jaksollisen taulun historia
- Jaksolliset perheet
Aperiodiset ominaisuudet
Jaksollisten ominaisuuksien lisäksi meillä on aperiodisia ominaisuuksia. Tässä tapauksessa arvot kasvavat tai laskevat alkuaineiden atomimäärän mukaan.
He saavat tämän nimen, koska he eivät noudata asemaansa jaksollisessa taulukossa kuin jaksolliset. Eli niitä ei toisteta säännöllisin väliajoin.
Tärkeimmät aperiodiset ominaisuudet ovat:
- Atomimassa: Tämä ominaisuus kasvaa atomiluvun kasvaessa.
- Ominaislämpö: tämä ominaisuus pienenee atomiluvun kasvaessa. Muista, että ominaislämpö on lämmön määrä, joka tarvitaan lämpötilan nostamiseen 1 ° C: lla 1 g: sta elementtiä.
Valintakokeen harjoitukset palautteella
1. (PUC-RJ) Harkitse jaksollisen ryhmän IA elementtejä koskevia lausuntoja
I. Niitä kutsutaan alkalimetalleiksi.
II. Sen atomisäteet kasvavat atomiluvun mukana.
III. Sen ionisaatiopotentiaali kasvaa atomiluvun myötä.
IV: Sen metallinen luonne kasvaa atomiluvun myötä.
Yksi väitteistä on totta:
a) I ja II
b) III ja IV
c) I, II ja IV
d) II, III ja IV
e) I, II, III ja IV
Vaihtoehto c
2. (UFMG) Vertaamalla klooria ja natriumia, kahta kemiallista alkuaineita, jotka muodostavat pöytäsuolan, voit sanoa, että kloori:
a) on tiheämpi.
b) on vähemmän haihtuva.
c) sillä on suurempi metallinen luonne.
d) on pienempi ionisaatioenergia.
e) sen atomisäde on pienempi.
Vaihtoehtoinen ja
3. (UFC-CE) Valosähköinen vaikutus koostuu elektronipäästöistä metallipinnoilta tarkoituksenmukaisen taajuuden valossa. Tähän ilmiöön vaikuttaa suoraan metallien ionisaatiopotentiaali, joka on ollut suurelta osin käytetään valosähköisten laitteiden valmistuksessa, kuten: julkisen valaistuksen valokennot, kamerat valokuvaus jne. Merkitse jaksollisen järjestelmän alkuaineiden ionisaatiopotentiaalin vaihteluihin perustuen vaihtoehto, joka sisältää metallia, jolla on todennäköisin valosähköinen vaikutus.
a) Fe
b) Hg
c) Cs
d) Mg
e) Ca
Vaihtoehto c
Tarkista pääsykokeen kysymykset kommentoidulla tarkkuudella Jaksollisen harjoitukset ja julkaisemattomat kysymykset aiheesta Harjoitukset jaksollisen järjestelmän järjestämiseen.
Lue myös:
- Jaksollinen järjestelmä
- Eletroninen jakelu
- Kemialliset alkuaineet
- Molekyylien väliset voimat

