Adsorptio on nestemäisten, kaasumaisten ja kiinteiden aineiden molekyylien fysikaalis-kemiallinen ominaisuus.
Prosessi tapahtuu, kun nestemäiset tai kaasumaiset hiukkaset ovat loukussa kiinteiden aineiden pinnalla. Jos kiinteät aineet ovat huokoisia, adsorptiokyky kasvaa vielä enemmän.
Prosessiin osallistuville komponenteille on kaksi luokitusta:
- Adsorbaatit: Se on nestemäinen tai kaasumainen aine, joka pidetään adsorboivan kiinteän aineen pinnalla.
- Adsorbentit: Se on kiinteä aine, joka edistää muiden aineiden kertymistä.
THE desorptio se on käänteinen adsorptioprosessi, toisin sanoen se on adsorbaatin vapautuminen adsorbentin pinnalta.
Tyypit
Prosessiin osallistuvien voimien luonteesta riippuen adsorptio voi olla kahden tyyppistä: fysisorptio ja kemisorptio.
Joissakin tapauksissa molemmat adsorptiotyypit voivat tapahtua samassa prosessissa.
fyysinen imeytyminen
Fyysinen fyysinen imeytyminen tai adsorptio adsorbaatin ja adsorbentin välillä tapahtuu Van der Waallsin voimien (dipoli-dipoli tai indusoitu dipoli) kautta.
Tässä tapauksessa prosessissa mukana olevissa aineissa ei ole minkäänlaista molekyylimuutosta. Toisin sanoen aine säilyttää kemiallisen luonteensa.
Fyysinen adsorptio on palautuva prosessi.
Kemisorptio
Kemisorptio tai kemiallinen adsorptio koostuu a kemiallinen reaktio. Ottamalla mukaan elektronit, pidetään vahvempana kemiallisena sidoksena kuin fysorptio.
Kemisorptiossa prosessissa mukana olevien aineiden molekyylimuutos tapahtuu. Eli aine voidaan muuntaa toiseen.
Koska tämä on kemiallinen reaktio, adsorbentin ja adsorbaatin komponenttien on oltava spesifisiä. Heidän on kyettävä tunnistamaan ja reagoimaan.
Kemiallinen adsorptio on peruuttamaton prosessi.
Lue myös:
- Molekyylien väliset voimat
- Kemialliset sidokset
Adsorptio ja imeytyminen
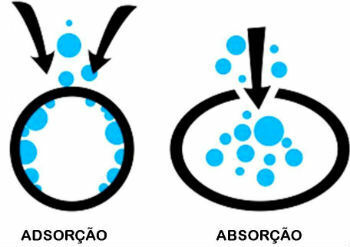
Ero adsorptiossa ja imeytymisessä
Adsorptio ja absorptio ovat kaksi erillistä prosessia. Tunne ero niiden välillä:
- adsorptio: Aine pysyy toisen pinnalla ilman, että se on osa sen tilavuutta.
- Imeytyminen: Yksi aine imeytyy toiseen aiheuttaen muutoksen tilavuudessa.
Yleinen esimerkki imeytymisestä on sieni, joka imee vettä. Näin tekemällä veden määrä lisätään sienen tilavuuteen.
Aktiivihiili
Aktiivihiili on esimerkki tunnetusta adsorboivasta aineesta. Sen rakenteessa on lukuisia huokosia, jotka tehostavat aineiden pidättymistä ja lisäävät niiden adsorptiokykyä.
Siksi aktiivihiiltä käytetään orgaanisten aineiden, öljyjen, värien ja hajujen poistamiseen. Sitä käytetään myös vedenkäsittelyyn sekä kosmetiikan ja lääkkeiden valmistukseen.

Aktiivihiili
Lue myös:
- Kromatografia
- Seosten erottaminen
- Liuotin ja liuotin
- Kemian laboratoriossa käytetyt materiaalit



