Hiilivedyt, kutsutaan myös vetykarbiditovat orgaanisia yhdisteitä, joiden koostumuksessa on vain hiili (C) ja alkaen vety (H), jolla on siten yleinen kaava CxHy.
Hiilivety koostuu hiilirakenteesta, johon vetyatomit sitoutuvat kovalenttisidos.
Se on orgaanisen kemian tärkein yhdiste.
Kaikentyyppiset hiilivedyt hapettuvat helposti vapauttaen siten lämpöä. Suurin osa niistä ei ole vesiliukoisia.
Luonnolliset hiilivedyt ovat kemiallisia yhdisteitä, jotka muodostuvat maapallon sisällä (yli 150 km päässä syvyys) korkeassa paineessa ja saavuta matalamman paineen vyöhykkeitä geologisten prosessien kautta.
Mistä löytyy hiilivetyjä?
Tärkein hiilivetyjen lähde on öljy. Tämän vuoksi hiilivetyä on läsnä useissa johdannaisissa, kuten kerosiini, parafiini, maakaasu, Bensiini, Vaseliini, diesel öljy, Nestekaasu (Nestekaasu), polymeerit (kuten muovia ja kumia).
Tämä orgaaninen yhdiste muodostaa 48% Brasilian energiamatriisista.
Hiiliketju, joka muodostaa osan hiilivedyn koostumuksesta, on neliarvoineneli se voi muodostaa neljä yhteyttä.
Hiili pystyy sitoutumaan muiden hiiliatomien ja vetyjen läpi yksinkertaisia linkkejä, tuplaa tai kolminkertaiset.
Hiilivetyjen luokitus
Hiilivetyjen luokitus perustuu kolmeen erityispiirteeseen: a muodossa hiilen pääketjun, Liitännät hiiliketjuista, alkyyliradikaalien läsnäolo hiiliketjussa ja heteroatomien läsnäolo jakamalla hiiliketju.
tietää enemmän vety.
Tärkein hiiliketjun muoto
Hiilivetyjen luokitus on jaoteltu päähiiliketjun muodon osalta alifaattinen ja syklinen.
Tarkista, mistä kukin näistä hiiliketjun muodoista koostuu.
alifaattiset hiilivedyt
Alifaattiset hiilivedyt muodostuvat hiiliketjuista avata tai asyklinen. Näissä ketjuissa hiilet ovat terminaaleja.
Esimerkkejä:
alkaani
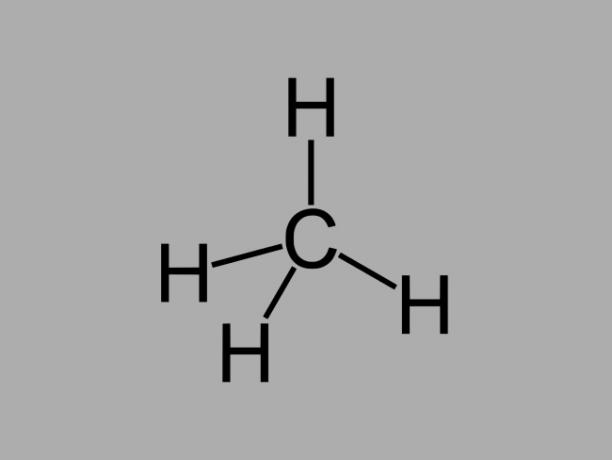
Alkaanihiilivedyt, kutsutaan myös parafiinit tai parafiininenovat öljyisiä yhdisteitä, joissa hiilien välillä on vain yksittäisiä sidoksia.
Alkaanin yleinen kaava on CeiH2ei + 2 (n = mikä tahansa kokonaisluku).
alkeeni
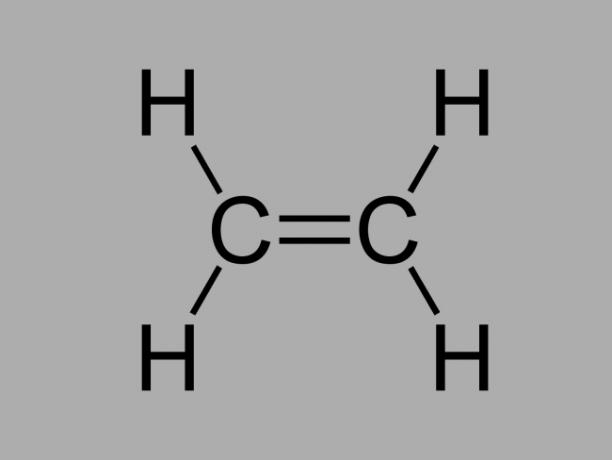
Kutsutaan myös olefiini, alkeeni tai eteenihiilivety, alkeeni on huonosti reaktiivinen yhdiste, jossa hiilien välillä on kaksoissidos.
Alkeeenin yleinen kaava on CeiH2ei.
alkyni
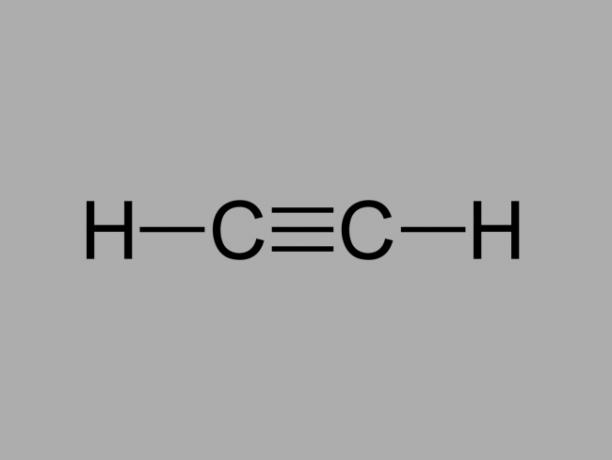
Kutsutaan myös metyyliasetyleeni, alkyni on hiilivety, jossa hiilen väliset sidokset ovat kolminkertaiset.
Alkyylin yleinen kaava on CeiH2ei-2.
alkadieeni

Kutsutaan myös dieeneiksi tai diolefiineiksi, alkadieenit ovat hiilivetyjä, joissa hiilien väliset sidokset ovat kaksinkertaiset.
Alkadieenin yleinen kaava on CeiH2ei-2.
Sykliset hiilivedyt
Sykliset hiilivedyt muodostuvat suljetuista tai syklisistä hiiliketjuista. Näissä ketjuissa ei ole terminaalisia hiiliä.
Esimerkkejä:
Cyclan
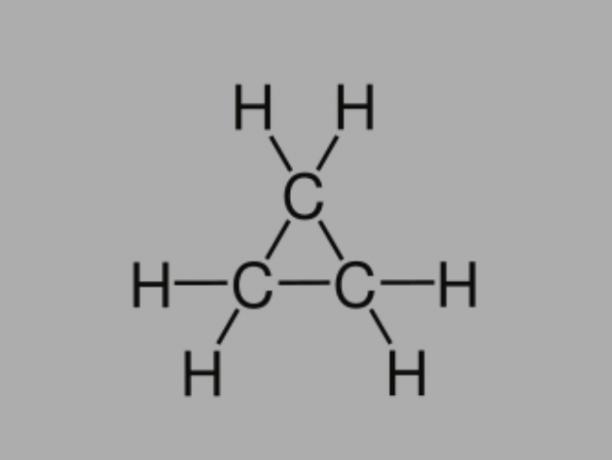
Kutsutaan myös sykloalkaani, sykloparafiini tai nafteeninen hiilivety, syklaani on tyydyttynyt hiilivety, joka koostuu yksittäisistä sidoksista.
Sillä on suljettu hiiliketju ja sen yleinen kaava on CeiH2ei.
Sykloninen

Kutsutaan myös sykloalkeenit, syklenit ovat tyydyttymättömiä hiilivetyjä, jotka koostuvat kaksoissidoksista.
Sykleenillä on suljettu hiiliketju ja sen yleinen kaava on CeiH2ei−2.
pyöräilijä
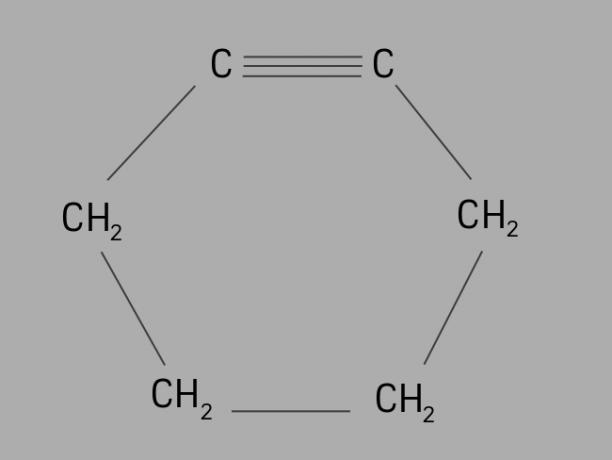
Kutsutaan myös sykloalkyni tai sykloalkyni, sykliini on syklinen ja tyydyttymätön hiilivety.
Sen muodostaa suljettu hiiliketju, jossa on kolmoissidokset, ja sen yleinen kaava on CeiH2ei-4.
Aromaattinen

tai

Kutsutaan myös areenoillaaromaattiset hiilivedyt ovat tyydyttymättömiä yhdisteitä, jotka muodostuvat kaksoissidoksista.
Aromaattisella on suljettu tai syklinen hiiliketju ja sen yleinen kaava on C6H6.
Hiiliketjujen sidostyyppi
Hiiliketjujen kytkentätyypistä riippuen hiilivedyt voidaan luokitella tyydyttynyt tai tyydyttymätön.
Katso alla, mistä kukin näistä luokituksista koostuu.
Tyydyttyneet hiilivedyt
Tyydyttyneitä hiilivetyjä muodostuu yksinkertaisia linkkejä.
Esimerkkejä: alkaanit, syklaanit.
tyydyttymättömät hiilivedyt
Tyydyttymättömät hiilivedyt muodostuvat kaksoissidokset tai kolminkertaiset.
Esimerkkejä: alkeenit, alkyynit, alkadieenit.
Alkyyliradikaalien läsnäolo
Alkyyliradikaalien läsnäolon osalta hiilivedyillä voi olla hiiliketju normaalia tai haarautunut.
normaali hiiliketju
Normaalissa hiiliketjussa olevassa hiilivedyssä ei ole alkyyliradikaaleja.
Esimerkki: pentaani
haarautunut hiiliketju
Kun hiilivedyllä on haarautunut hiiliketju, se tarkoittaa, että sen päähiiliketjussa on alkyyliradikaaleja.
Esimerkki: metyylipropaani
Hiiliketjua jakavien heteroatomien läsnäolo
Peräkkäinen hiiliketju voi jakautua tai olla jakamatta heteroatomien läsnäolon mukaan.
Homogeeninen hiiliketju
Kun hiilivedyllä on homogeeninen päähiiliketju, se tarkoittaa, että tämä ketju ei ole jaettu heteroatomien avulla.
Heterogeeninen hiiliketju
Jos hiilivedyllä on heterogeeninen päähiiliketju, tällä ketjulla oli sen jaettu hiiliketju heteroatomin avulla.
Hiilivetyjen nimikkeistö
Hiilivetyjen nimikkeistö määritellään yhdistämällä kolme osaa:

Etuliite tunnistaa hiilien määrän, välituote identifioi sidoksen tyypin ja loppuliite osoittaa toiminnon, johon yhdiste kuuluu (tässä tapauksessa hiilivetyjen luokka).
Alla on luettelo etuliitteistä ja välituotteista, jotka yhdistetään hiilivetyjen osoittamiseksi.
Etuliiteluettelo
| Hiilien määrä | Etuliite |
|---|---|
| 1 | Tavannut- |
| 2 | Et- |
| 3 | Ehdotus |
| 4 | Mutta- |
| 5 | pent- |
| 6 | Hex- |
| 7 | Hept- |
| 8 | Loka- |
| 9 | Ei- |
| 10 | Joulu- |
Välittäjien luettelo
| Yhteystyyppi | Välittäjä |
|---|---|
| Vain yksittäiset puhelut | -on- |
| Pari | -en- |
| kolminkertaistaa | -sisään- |
| kaksi paria | -dien- |
Katso joitain esimerkkejä hiilivetyjen nimeämisestä.
Esimerkkejä:
CH3 - CH2 - CH2 - CH3
Yllä olevassa rakennemuodossa voimme nähdä 4-hiiliyhdisteen, jolla on vain yksittäisiä sidoksia (merkitty symbolilla "-").
- 4 hiilen etuliite = but-
- Yksittäisen sitoutumisen välituote = -an-
- Hiilivedyn loppuliite = -o
Katso, että etuliite + väli + loppuliite synnyttää nimen BUTAANI.
CH2 = CH2
Yllä olevassa rakennemuodossa on 2 hiiltä ja 1 kaksoissidos (merkitty symbolilla “=”).
- 2 hiilen etuliite = et-
- Kaksinkertaisten joukkovelkakirjojen välituote = -en-
- Hiilivedyn loppuliite = -o
Katso, että etuliite + väli + loppuliite synnyttää nimen JUOMAINEN.
CH2 = CH - CH2 - CH3
CH3 - CH = CH2 - CH3
Huomaa, että molemmissa yllä olevissa rakennemuodoissa on 4 hiiltä ja 1 kaksoissidos (merkitty symbolilla “=”).
Siksi meillä on:
- 4 hiilen etuliite = but-
- Kaksinkertaisten joukkovelkakirjojen välituote = -en-
- Hiilivedyn loppuliite = -o
Katso, että etuliite + väli + loppuliite aiheuttaisi nimen BUTENE kahdelle rakennemuodolle.
Huomaa kuitenkin, että rakennemuodot eivät ole identtisiä, joten nimikkeistöt eivät voi olla kumpaakaan.
Kahden rakenteellisen muodon ero on kaksoissidoksen sijainnissa.
Tällöin meidän on numeroitava ketjun hiilet kaksoisosaa lähinnä olevasta päästä. Siksi meidän on kyseisissä tapauksissa numeroitava vasemmalta oikealle.
Sisään CH2 = CH - CH2 - CH3:
- CH2 tulee olemaan 1
- CH on 2
- CH2 tulee olemaan 3
- CH3 tulee olemaan 4
Huomaa, että kaksoissidos on hiili 1 se on hiili 2.
Meidän on käytettävä pienintä lukua (1) kaksoissidoksen löytämiseksi: Buteeni -1
Sisään CH3 - CH = CH2 - CH3:
- CH3 tulee olemaan 1
- CH on 2
- CH2 tulee olemaan 3
- CH3 tulee olemaan 4
Huomaa, että kaksoissidos on hiili 2 se on hiili 3.
Meidän on käytettävä pienintä lukua (2) kaksoissidoksen löytämiseksi: BUTENE -2
Mukaan IUPAC (Kansainvälinen puhtaan ja sovelletun kemian liitto - Kansainvälinen puhtaan ja sovelletun kemian liitto), sijainti tulisi ilmoittaa hieman ennen sijaitsee (edellä olevien rakennemuotojen tapauksessa kaksoissidos, jota edustaa välituote "-En-").
Sen avulla meillä on toinen tapa, joka on muuten oikeampi, kirjoittaa käytettävissä olevien rakennemuotojen nimikkeistö.
CH2 = CH - CH2 - CH3: BUTENE -1 tai BUT-1-ENO (oikeampi muoto)
CH3 - CH = CH2 - CH3: BUTENE -2 tai BUT-2-ENE (oikeampi muoto)
Lisätietoja IUPAC ja nimikkeistö.
