O ammoniumnitraatti on kiinteä aine, jolla on molekyylikaava NH4AT3 ja valkoinen ulkonäkö (puhtaana). muodostuu mukaan ioneja NH4+ (ammonium) ja NO3- (nitraatti), ei ole syttyvää, mutta on erittäin hapettava ja reaktiivinen. Sen hajoamisreaktio tuottaa tuotteena suuren määrän kaasuja, mikä tekee tuotteen epäasianmukaisesta varastoinnista vakavan ongelman, koska voi esiintyä räjähdyksiä. Ja myös käytetään laajalti maataloudessa lannoitteena.
Lue myös: Luonnolliset aineet - molekyylit ovat peräisin luonnosta
Mikä on ammoniumnitraatti?

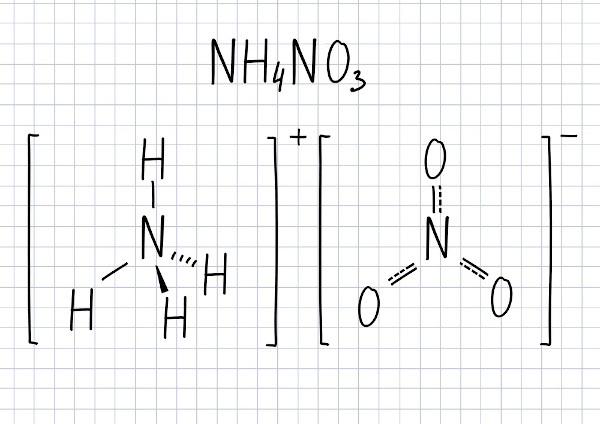
Ammoniumnitraatti se on suola muodostuu NH-ioneista4+ (ammonium) ja NO3- (nitraatti). Se on kiinteä yhdiste, kun puhdas, se on valkoista. Sitä käytetään laajalti maatalouslannoitteena, mutta sitä voidaan käyttää myös räjähteiden valmistuksessa se on erittäin hapettava ainesitten hapettava. Ammoniumnitraatin tunkeutuva reaktio tuottaa suuren määrän kaasuja, aiheuttaen räjähtävä vaikutus.
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Ammoniumnitraatin ominaisuudet
Moolimassa: 80,04336 g / mol.
Suola, joka koostuu ioneista: ammonium (NH4+) ja nitraatti (NO3-).
Ulkonäkö: valkoinen kiinteä aine.
Se on voimakkaasti hapettava.
Reagoi helposti muiden aineiden kanssa.
Se ei ole syttyvää.
Normaaleissa lämpötila- ja paineolosuhteissa:
- tiheys: 1,73 g / cm3;
- kiehumispiste: 210 ° C;
- sulamispiste: 169,6 ° C;
- liukoisuus veteen: 216 g / 100 ml;
- pH: 5,5 (0,2 M).
Ammoniumnitraattikaava
Tämän yhdisteen molekyylikaava on NH4AT3.
Ammoniumnitraatin hajoaminen
a aine, jolla on suuri reaktiivisuus ja korkea hapettumispotentiaali, ammoniumnitraatti, kun se altistetaan korkealle lämpötilalle, laukaisee a hajoamisreaktioja päätuotteita ovat kaasut, typpi, happi ja vesihöyry. Hajoaminen tapahtuu kahdessa vaiheessa:
→ 1. vaihe:
2NH4AT3 (s) → 2N2O (g) + 4H2O (g)
→ 2. vaihe:
2N2O → 2N2(g) + O2(g)
→ Globaali yhtälö:
2NH4AT3 (s) → 2N2(g) + O2(g) + 4H2O (g)
Huomaa, että ensimmäisessä yhtälössäyksi tuotteista hajoamisessa saatu on typpioksidi (N2O), tunnetaan myös ilokaasu. Sitä käytetään lisäämään autojen moottoreiden tehoa polttamaan polttoainetta ja anestesia-aineena, pääasiassa hammaslääkäreiden toimesta. Se on myös yksi tärkeimmistä vastuussa olevista kaasuista kasvihuoneilmiö.
Katso myös: Mitkä ovat kemiallisten reaktioiden tyypit?
Ammoniumnitraatin tuotanto
Ammoniumnitraattia voidaan saada reaktio ammoniumsulfaatin (NH4) välillä2VAIN4 ja kalsiumnitraatti Ca (NO3)2. Katso alempaa:
(NH4)2VAIN4 + Ca (NO3)2 → 2 NH4AT3+ Asia4
Sitä voidaan valmistaa myös kaasumaisesta ammoniakista, jota kuplitaan typpihappoliuoksessa, jossa reaktiotuotteena on ammoniumnitraatin vesiliuos. Katso:
NH3 g) + HNO3 (aq) → NH4AT3(tässä)
Ammoniumnitraatin käyttö

- Lannoitteiden valmistus
- Räjähteet kaivoksissa, louhoksissa ja rakentamisessa
- Herbisidit ja hyönteismyrkyt
- Dityppioksidin saaminen teolliseen käyttöön
- Oksidien absorbentit
- Oksidantti rakettien ponneaineille
- Isotermisten pussien valmistus
- Puudutussavun tuottaminen mehiläispesien pesien hallintaan
Pääsy myös: Kuinka taistella tulta vastaan?
Ammoniumnitraattivaarat
Yksi tärkeimmistä ammoniumnitraattiin liittyvistä riskeistä on riittämätön varastointi. Koska se on erittäin hapettava aine ja reagoi useiden muiden yhdisteiden kanssa, se laukaisee a reaktio vapauttamalla suuri määrä kaasua. Virheellinen varastointi on alttiita syttyville tuotteille, altistuminen lämmön tai kaasun kertymiselle mikä voi aiheuttaa räjähdyksiä.
Näin on jo tapahtunut esimerkiksi Texasissa Yhdysvalloissa, kun Ranskasta tullut rahtilaiva kuljetti 2086 tonnia ammoniumnitraattia. onnettomuus tapahtui vuonna 1947 ja tunnettiin Texas Cityn katastrofina. Tragedia aiheutti 581 ihmisen kuoleman ja se tapahtui tulipalossa, jota ei ollut aluksessa ja joka saavutti ammoniumlasti, joka laukaisi räjähdyksen.
Toinen esimerkki oli räjähdysjärjestys joka tapahtui 4. elokuuta 2020 Portugalin satamassa Beirutin kaupunki, Libanon, jolloin yli 100 ihmistä kuoli ja 5000 loukkaantui. Räjähdyksen suuruus johtui siellä varastoidun 2750 tonnin ammoniumnitraatin lastin ketjureaktiosta.
On myös syytä huomata, että ammoniumnitraatti voi aiheuttaa ihon ja silmien ärsytys ja hengitettynä hengitysongelmia. Verenkierrossa aineella on myrkyllistä voimaa, koska se reagoi kehon nesteiden kanssa, ja tämän reaktion tuotteet, kuten nitraatti, voivat vahingoittaa terveyttä, kuten sininen vauvan tauti, tunnetaan myös nimellä infantiili methemoglobinemia (matala veren hemoglobiini). Tämä tauti on toistuva maaseutualueiden perheissä johtuen viljelyalueen vesistöjen lannoitteissa esiintyvästä ammoniumnitraatista.
kirjoittanut Laysa Bernardes
Kemian opettaja
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
ARAúJO, Laysa Bernardes Marques de. "Ammoniumnitraatti"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/nitrato-de-amonio.htm. Pääsy 27. kesäkuuta 2021.
Biologia
Lue lisää typpisyklistä, tärkeästä biogeokemiallisesta kierrosta, joka varmistaa tämän elementin liikkeen. Tässä tekstissä käsittelemme typpisyklin kutakin vaihetta, keskustelemme sen merkityksestä ja keskitymme bakteerien rooliin tässä prosessissa. Esittelemme myös aiheeseen liittyviä harjoituksia.